إن التحكم عن بعد في التفاعلات الكيميائية في البيئات البيولوجية يمكن أن يتيح مجموعة متنوعة من التطبيقات الطبية. على سبيل المثال، يمكن أن تساعد القدرة على إطلاق أدوية العلاج الكيميائي على الهدف في الجسم في تجاوز الآثار الجانبية الضارة المرتبطة بهذه المركبات السامة. ولهذا الهدف، توصل باحثون في معهد كاليفورنيا للتكنولوجيا (معهد كاليفورنيا للتكنولوجيا) أنشأوا نظامًا جديدًا تمامًا لتوصيل الأدوية يستخدم الموجات فوق الصوتية لإطلاق مركبات تشخيصية أو علاجية بدقة متى وأينما تكون هناك حاجة إليها.
المنصة التي تم تطويرها في مختبرات ماكسويل روب و ميخائيل شابيرو، يعتمد على جزيئات حساسة للقوة تُعرف باسم الميكانيكا والتي تخضع لتغيرات كيميائية عندما تتعرض للقوة الفيزيائية وتطلق جزيئات شحن أصغر. يمكن توفير التحفيز الميكانيكي عبر الموجات فوق الصوتية المركزة (FUS)، التي تخترق الأنسجة البيولوجية بعمق ويمكن تطبيقها بدقة أقل من المليمتر. ومع ذلك، تطلبت الدراسات السابقة على هذه الطريقة شدة صوتية عالية تسبب التسخين ويمكن أن تلحق الضرر بالأنسجة المجاورة.
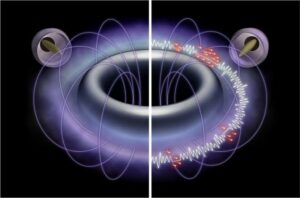
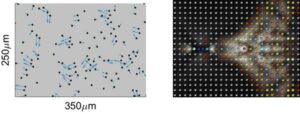
لتمكين استخدام الموجات فوق الصوتية ذات شدة أقل وأكثر أمانًا، تحول الباحثون إلى حويصلات الغاز (GVs)، وهي هياكل نانوية بروتينية مملوءة بالهواء والتي يمكن استخدامها كعوامل تباين بالموجات فوق الصوتية. لقد افترضوا أن الكرات الأرضية يمكن أن تعمل كمحولات طاقة صوتية ميكانيكية لتركيز طاقة الموجات فوق الصوتية: عند تعرضها لـ FUS، تخضع الكرات الأرضية للتجويف مع تنشيط الطاقة الناتجة للحامل الميكانيكي.
"يعتمد تطبيق القوة من خلال الموجات فوق الصوتية عادة على ظروف شديدة للغاية تؤدي إلى انفجار فقاعات الغاز الصغيرة الذائبة"، كما يوضح المؤلف الأول المشارك. مولي مكفادين في تصريح صحفي. "انهيارها هو مصدر القوة الميكانيكية التي تنشط الميكانيكا. زادت حساسية الحويصلات للموجات فوق الصوتية. وباستخدامها، وجدنا أن نفس التنشيط الميكانيكي يمكن تحقيقه تحت الموجات فوق الصوتية الأضعف بكثير.
الإبلاغ عن النتائج التي توصلوا إليها في وقائع الاكاديمية الوطنية للعلومأثبت الباحثون أن هذا النهج يمكن أن يؤدي عن بعد إلى إطلاق جزيئات الشحن من البوليمرات ذات الوظائف الميكانيكية باستخدام FUS المتوافق حيويًا.
تطوير توصيل الدواء
حدد مكفادين وزملاؤه في البداية معلمات الموجات فوق الصوتية الآمنة للتطبيقات الفسيولوجية. كشفت التجارب التي أجريت على FUS بتردد 330 كيلو هرتز عن حد أعلى متوافق حيويًا يبلغ 1.47 ميجا باسكال ذروة الضغط السلبي مع دورة تشغيل بنسبة 4.5% (3000 دورة لكل نبضة)، مما يؤدي إلى كثافة صوتية تبلغ 3.6 واط/سم2. في هلام وهمي يحاكي الأنسجة، أدت هذه المعلمات إلى زيادة درجة الحرارة القصوى بمقدار 3.6 درجة مئوية فقط.
ثم قام الباحثون بالتحقيق فيما إذا كان بإمكان FUS تنشيط البوليمرات المحتوية على الميكانيكا باستخدام هذه المعلمات المتوافقة حيوياً. لقد قاموا بدراسة البوليمر PMSEA الذي يحتوي على حامل ميكانيكي متمحور حول سلسلة محمل بجزيء صغير فلوروجيني. أدى تعريض المحلول المخفف لهذا البوليمر إلى FUS المتوافق حيوياً في وجود GVs إلى زيادة قوية في التألق، مما يشير إلى الإطلاق الناجح للحمولة النافعة - إطلاق حوالي 15% بعد 10 دقائق من التعرض لـ FUS. الأهم من ذلك، أن التعرض لـ FUS بدون GVs لم يؤدي إلى استجابة فلورية، مما يؤكد أن GVs تلعب دورًا أساسيًا كمحولات طاقة صوتية ميكانيكية.
بعد ذلك، فحص الباحثون ما إذا كان النظام مناسبًا لإطلاق الأدوية المحفزة ميكانيكيًا. قاموا بربط عامل العلاج الكيميائي الكامبتوثيسين بالحامل الميكانيكي متبوعًا بالبلمرة لتكوين PMSEA-CPT، واستخدموا FUS لتوفير إطلاق متحكم فيه. بعد التعرض لمدة 10 دقائق لـ FUS المتوافق حيويًا بالإضافة إلى GVs، تم إطلاق ما يقرب من 8٪ من الكامبتوثيسين. كما وجد بالنسبة للجزيء الفلوري، لم يتم الكشف عن أي إطلاق للأدوية في غياب الصور العامة.
وفقا للمؤلف الأول المشارك يوشينغ ياوهذه هي المرة الأولى التي يثبت فيها FUS قدرته على التحكم في تفاعل كيميائي محدد في بيئة بيولوجية. يقول ياو: "في السابق، تم استخدام الموجات فوق الصوتية لتعطيل الأشياء أو تحريكها". "لكنه الآن يفتح لنا هذا المسار الجديد باستخدام الكيمياء الميكانيكية."
ولتقييم الإمكانات المستقبلية للمنصة في العلاج الكيميائي المستهدف لدى المرضى، قام الباحثون بالتحقيق في سميتها للخلايا المختبر على خلايا راجي الشبيهة بالأورام اللمفاوية. أظهرت الخلايا المحتضنة لمدة يومين باستخدام PMSEA-CPT التي تعرضت سابقًا لـ FUS وGVs انخفاضًا كبيرًا في قابلية البقاء. في المقابل، لم يُلاحظ أي سمية خلوية كبيرة في الخلايا المحتضنة بـ PMSEA-CPT والتي لم تتعرض لـ FUS أو PMSEA-CPT المعرضة لـ FUS ولكن بدون GVs.

يوفر الجهاز القابل للزرع الذي يتم تشغيله بالضوء توصيل دواء قابل للبرمجة
كتب الباحثون: "إن الإطلاق الميكانيكي للحمولات الجزيئية من البوليمرات في الوسائط المائية يوضح قوة هذا النهج في التصوير الحيوي غير الجراحي والتطبيقات العلاجية للكيمياء الميكانيكية للبوليمر". "على نطاق أوسع، توضح هذه الدراسة نهجًا لتحقيق التحكم عن بعد في تفاعلات كيميائية محددة في ظل ظروف طبية حيوية ذات صلة بالدقة الزمانية المكانية واختراق الأنسجة التي يوفرها FUS."
وبعد هذه الاختبارات الأولية في ظل ظروف معملية خاضعة للرقابة، يخطط الباحثون الآن لاختبار منصتهم على الكائنات الحية. "نحن نعمل على ترجمة هذا الاكتشاف الأساسي إلى في الجسم الحي يقول روب: "تطبيقات توصيل الأدوية والتقنيات الطبية الحيوية الأخرى". عالم الفيزياء.
- محتوى مدعوم من تحسين محركات البحث وتوزيع العلاقات العامة. تضخيم اليوم.
- PlatoData.Network Vertical Generative Ai. تمكين نفسك. الوصول هنا.
- أفلاطونايستريم. ذكاء Web3. تضخيم المعرفة. الوصول هنا.
- أفلاطون كربون، كلينتك ، الطاقة، بيئة، شمسي، إدارة المخلفات. الوصول هنا.
- أفلاطون هيلث. التكنولوجيا الحيوية وذكاء التجارب السريرية. الوصول هنا.
- المصدر https://physicsworld.com/a/biocompatible-focused-ultrasound-delivers-cancer-drugs-on-target/
- :لديها
- :يكون
- :ليس
- :أين
- 1
- 10
- 15%
- 3000
- a
- القدرة
- الأكاديمية
- تحقق
- تحقيق
- تفعيل
- تفعيل
- أتاحت
- بعد
- الوكيل
- عملاء
- هدف
- an
- و
- التطبيقات
- تطبيقي
- نهج
- ما يقرب من
- هي
- حول
- AS
- تقييم
- أسوشيتد
- At
- المؤلفة
- على أساس
- BE
- كان
- الطبية الحيوية
- الجسدي
- مقيد
- بصورة عامة
- لكن
- by
- كاليفورنيا
- CAN
- السرطان.
- سبب
- خلايا
- التغييرات
- مادة كيميائية
- انهيار
- الزملاء
- الشروط
- يحتوي
- تباين
- مراقبة
- ذو شاهد
- استطاع
- خلق
- خلق
- دورة
- دورات
- إتلاف
- أيام
- تخفيض
- عميق
- يسلم
- التوصيل
- شرح
- تظاهر
- يوضح
- الكشف عن
- المتقدمة
- جهاز
- تشخيصي
- فعل
- اكتشاف
- تعطيل
- عدة
- عقار
- المخدرات
- في وقت سابق
- الآثار
- تمكين
- طاقة
- تماما
- البيئات
- أساسي
- مثال
- تجارب
- ويوضح
- مكشوف
- تعرض
- النتائج
- الاسم الأول
- لأول مرة
- تركز
- ركز
- يتبع
- في حالة
- القوة
- وجدت
- تبدأ من
- وظيفة
- أساسي
- مستقبل
- GAS
- كان
- يملك
- تزايد
- مساعدة
- مرتفع
- لكن
- HTTPS
- محدد
- يوضح
- صورة
- انهيار
- الأهم
- in
- القيمة الاسمية
- محتضن
- معلومات
- في البداية
- معهد
- إلى
- قضية
- انها
- JPG
- معروف
- مختبر
- مختبرات
- ليد
- اليسار
- مما سيحدث
- لينكدين:
- الذين يعيشون
- خفض
- ماكس العرض
- أقصى
- ميكانيكي
- الوسائط
- طبي
- التطبيقات الطبية
- طريقة
- دقيقة
- جزيئي
- جزيء
- خطوة
- كثيرا
- محليات
- بحاجة
- سلبي
- جديد
- لا
- الآن
- of
- on
- فقط
- افتتاح
- or
- أخرى
- المعلمات
- مسار
- المرضى
- قمة
- اختراق
- إلى
- وهمي
- مادي
- فيزياء
- عالم الفيزياء
- خطة
- المنصة
- منصات التداول
- أفلاطون
- الذكاء افلاطون البيانات
- أفلاطون داتا
- بلايستشن
- المزيد
- البوليمرات
- محتمل
- قوة
- على وجه التحديد
- دقة
- وجود
- صحافة
- الضغط
- سابقا
- برمجة
- بروتين
- تزود
- المقدمة
- ويوفر
- نبض
- نطاق
- رد فعل
- ردود الفعل
- الافراج عن
- صدر
- ذات الصلة
- عن بعد
- مطلوب
- الباحثين
- استجابة
- مما أدى
- أظهرت
- حق
- النوع
- خزنة
- أكثر أمانا
- نفسه
- يقول
- رأيت
- حساسية
- ضبط
- جانب
- هام
- صغير
- الأصغر
- حل
- مصدر
- محدد
- ملخص الحساب
- حافز
- قوي
- مدروس
- دراسات
- دراسة
- ناجح
- مناسب
- نظام
- الهدف
- المستهدفة
- التكنولوجيا
- تكنولوجيا
- يروي
- تجربه بالعربي
- اختبارات
- أن
- •
- المصدر
- من مشاركة
- منهم
- then
- تشبه
- هم
- الأشياء
- عبر
- صورة مصغرة
- الوقت
- إلى
- ترجمه
- يثير
- أثار
- صحيح
- تحول
- اثنان
- مع
- خضع
- us
- تستخدم
- مستعمل
- يستخدم
- استخدام
- عادة
- جدا
- بواسطة
- بقاء
- وكان
- we
- متى
- سواء
- التي
- مع
- في غضون
- بدون
- عامل
- العالم
- اكتب
- زفيرنت