العلاج بالجسيمات – علاج السرطان باستخدام حزم من البروتونات أو الأيونات الأثقل – يوفر توصيل جرعة متوافقة للغاية مع الحفاظ على الأنسجة الطبيعية بشكل أكبر من العلاج الإشعاعي التقليدي المعتمد على الفوتون. ولكن بالنسبة للناجين من السرطان على المدى الطويل، فإن خطر الإصابة بالسرطان الثانوي الناجم عن الإشعاع أمر مهم، وينبغي أخذه في الاعتبار عند اختيار طريقة علاجهم.
ومع ندرة البيانات الوبائية الخاصة بالعلاجات الأحدث مثل العلاج بالبروتونات وأيونات الكربون، فقد ترأس فريق من الباحثين في مركز GSI Helmholtz لأبحاث الأيونات الثقيلة تقوم بتطوير نموذج لمقارنة مخاطر SC بين طرق العلاج بالجسيمات. النموذج الذي وصفه أنطونيا هوفناجل والزملاء في الفيزياء الطبية، يمكن دمجها في نهاية المطاف في أنظمة تخطيط العلاج لتشمل مخاطر SC كمعيار تحسين إضافي.
الأحداث القاتلة مقابل الأحداث المسببة للسرطان
تعمل نماذج المخاطر SC عادة من خلال النظر في التوازن بين قتل الخلايا (مما يؤدي إلى قمع السرطان) وتحول الخلايا (تحريض الطفرات التي تؤدي في النهاية إلى السرطان). يتم تحديد احتمالية إصابة الحجم المشعع بالسرطان باستخدام النموذج الخطي التربيعي (LQ)، والذي يوفر علاقة بسيطة بين بقاء الخلية وجرعة الفوتون المسلمة.
في هذه الدراسة، استخدم الباحثون نموذج التأثير المحلي (LEM) للتنبؤ بالفعالية البيولوجية النسبية (RBE) لتحريض SC بعد العلاج بالجسيمات. ولمراعاة زيادة RBE لإشعاع الجسيمات، قاموا باستبدال معلمات الفوتون LQ في نموذج المخاطر بمعلمات LQ للشعاع الأيوني التي تنبأ بها LEM. السمة الرئيسية لنهجهم هي استخدام LEM في كل من مصطلحات قتل الخلايا وتحريض السرطان.

يوضح المؤلف الرئيسي أن "الاستخدام المزدوج لـ LEM يعكس المنافسة بين العمليتين الرئيسيتين اللتين تحددان تطور الخلايا الجذعية، وهما تحويل الخلايا وقتل الخلايا". مايكل شولتز. "مع زيادة الجرعة و/أو الفعالية، يمكن أن يؤدي قتل الخلايا إلى تثبيط قدرة الخلايا المتحولة على البقاء. وهذا يؤدي إلى تفاعل معقد، لا يمكن أن ينعكس ببساطة في إجراء من خطوة واحدة.
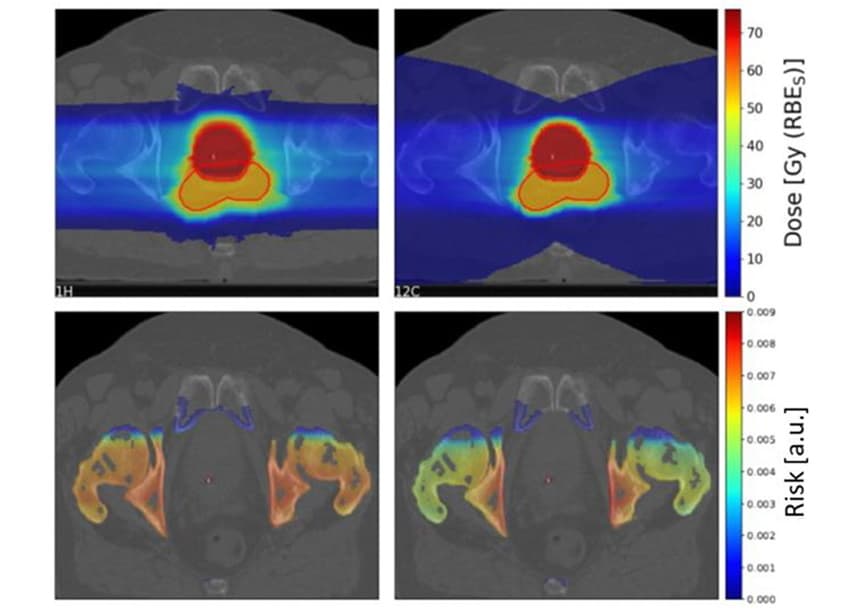
للتحقيق في العوامل التي تؤثر على مخاطر SC، استخدم الباحثون نظام التخطيط TPS TRiP98 لإنشاء خطط معالجة أيون الكربون والبروتونات المحسنة بيولوجيًا بناءً على هندسة مثالية. قامت الخطط بتشعيع هدف مقاس 4x4x4 سم باستخدام شعاع جسيمي واحد أو شعاعين متعارضين، مع وجود عضو معرض للخطر (OAR) مقاس 4x4x1 سم أمام الهدف. نظرًا لعدم اليقين في معلمات الفوتون LQ المستخدمة كمدخلات لـ LEM، فقد قاموا بتقدير نسب خطر البروتون إلى أيون الكربون، بدلاً من قيم المخاطر الفردية.
بالنسبة لهذه الإعدادات المثالية، لم يُظهر النموذج تفضيلًا واضحًا للبروتونات أو أيونات الكربون، ولكنه كشف عن اعتماد معقد على عوامل مختلفة. يؤدي انخفاض التشتت الجانبي لأيونات الكربون إلى انخفاض خطر SC مقارنة بالبروتونات الموجودة في قناة المدخل. ومع ذلك، تودع أيونات الكربون جرعة أعلى خلف الهدف بسبب ذيل التفتت، مما يزيد من خطر الإصابة بالمجالات المفتوحة خلف الورم بعد تشعيع أيونات الكربون.
بالنسبة لخطط الحزمة الواحدة، كان إجمالي خطر SC أعلى بحوالي 1.5 مرة بالنسبة لأيونات الكربون مقارنة بالبروتونات. مع وجود شعاعين متعارضين، كان إجمالي خطر SC أعلى بمقدار 1.16 مرة بالنسبة للبروتونات، على الرغم من أن هذا يختلف بشدة اعتمادًا على الموقع المكاني للحجم الحساس المفترض فيما يتعلق بالحجم المستهدف.
كان لحساسية الأنسجة الإشعاعية (للفوتونات) تأثير كبير على نسبة مخاطر SC، حيث استفادت المجاذيف المفتوحة المقاومة للإشعاع من معالجة أيونات الكربون والمجالات المفتوحة الحساسة من حزم البروتون. وفي المقابل، لم يكن لنظام التجزئة تأثير يذكر على قيم المخاطر المتوقعة.
هندسة المريض
للتحقيق في السيناريوهات السريرية، قدر شولز وزملاؤه مخاطر SC لدى 10 مرضى بسرطان البروستاتا تم علاجهم سابقًا بالعلاج الإشعاعي بالفوتون في مستشفى جامعة كارولينسكا. لقد قاموا بإنشاء خطط علاجية للمرضى باستخدام حقلين بروتون وأيون كربون متقابلين تم مسحهما جانبيًا.
كما رأينا سابقًا، أدى ذيل تجزئة أيونات الكربون إلى وجود مساحة كبيرة منخفضة الجرعة خلف الهدف. ومع ذلك، كانت المنطقة المستهدفة ذات الجرعة العالية أكثر توافقًا مع أيون الكربون من خطط البروتون.
قام الفريق بحساب نسب خطر البروتون إلى أيون الكربون SC لأربعة OARs (المثانة والمستقيم والعظام والجلد) للمرضى العشرة. بالنسبة للعظام والجلد، أسفرت خطط البروتون عن خطر أعلى قليلاً من خطط أيونات الكربون، مع متوسط نسب خطر تبلغ 10 و1.19 للعظام والجلد، على التوالي. ومع ذلك، بالنسبة للمثانة والمستقيم، أدت خطط البروتون إلى انخفاض مخاطر SC بشكل ملحوظ، مع نسب خطر تبلغ 1.06 و0.68 للمثانة والمستقيم، على التوالي.
وخلص الباحثون إلى أن الأفكار التي اكتسبها هذا النموذج يمكن أن تساعد في تحسين العلاجات المستقبلية. في الوقت الحالي، تعد نمذجة المخاطر النسبية مناسبة بشكل أساسي كأداة لمقارنة سيناريوهات العلاج المختلفة لمجموعات مختلفة من المرضى. لكن شولز يشير إلى أن دمج مثل هذه النماذج في التخطيط العلاجي للمرضى الأفراد سيكون أمرًا مباشرًا.

العلاج بشبكة أيونات الكربون يحافظ على الأنسجة السليمة
ويوضح قائلاً: "إن الأمر يتطلب فقط تشغيل التخطيط لتوزيع جرعة معينة باستخدام مجموعتين مختلفتين من العوامل البيولوجية التي تمثل عملية قتل الخلية وعملية تحويل الخلية، على التوالي". "بعد ذلك، لا يلزم سوى بعض المعالجة اللاحقة لتوزيعات التأثير ثلاثي الأبعاد الناتجة باستخدام الأدوات الرياضية القياسية لاشتقاق توزيعات نسبة المخاطر المقابلة."
ويقول إن الخطوة التالية هي التحقق من صحة النموذج من خلال مقارنته بالبيانات السريرية. يقول شولز: "نظرًا لندرة هذه البيانات في الوقت الحالي، فإن توسيع النهج ليشمل أيضًا معالجات الفوتون وتحديد نسب الخطر المقابلة للبروتونات مقابل الفوتونات وأيونات الكربون مقابل الفوتونات سيكون خطوة تالية مهمة". عالم الفيزياء.