في سن 70 عامًا تقريبًا ، بدت الفئران مسنة وغير ملحوظة. ومع ذلك ، كانت مخبأة تحتها ساعة خلوية شبابية ، عادت بالزمن إلى الوراء بناءً على إستراتيجية حائزة على جائزة نوبل. إنه أيضًا أحدث رهان للعثور على ينبوع الشباب ، مدعومًا بشركات ناشئة ضاربة في مكافحة الشيخوخة في وادي السيليكون.
في المركز إعادة البرمجة الخلوية الجزئية. هذه التقنية ، وهي نوع من العلاج الجيني ، تجبر الخلايا على صنع أربعة بروتينات ، يطلق عليها مجتمعة عوامل ياماناكا. مثل المحايات ، تمسح العوامل التاريخ الجيني للخلية ، وتعيد الخلايا البالغة - على سبيل المثال ، خلايا الجلد - إلى هوية شبيهة بالخلايا الجذعية ، مما يمنحها القوة العظمى لتتحول إلى أي نوع من الخلايا تقريبًا.
العملية ليست كل شيء أو لا شيء. في تطور ، وجد العلماء مؤخرًا أنه يمكنهم استخدام العوامل لإعادة لف شريط التاريخ الجيني للخلية بدلاً من تدميره تمامًا. وإذا توقفوا عند النقطة الصحيحة ، تفقد الخلية عمرها بشكل كبير ، وتصبح أكثر شبابًا لكنها تحتفظ بهويتها. النتائج أثار موجة من الاهتمام في نقل العلاج إلى البشر ، مع شركة Calico Life Sciences - وهي شركة شقيقة لـ Google - و Altos Labs ، بدعم من Jeff Bezos ، في السباق.
لكن عوامل ياماناكا لها جانب مظلم. كثيرًا ، ويصاب الجسم بأورام كابوسية تسمى الأورام المسخية ، وهي عبارة عن تكتل من الأنسجة غالبًا ما يشمل الأسنان والعظام والعضلات التي تم تطويرها جزئيًا. كما أن كيفية الحث على إعادة البرمجة الجزئية دون دفع الخلايا بالكامل إلى الخلايا الجذعية تظل غامضة.
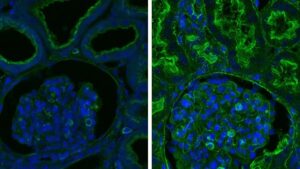
A دراسة جديدةبقيادة الدكتور خوان كارلوس إيزبيسوا في معهد سالك و مختبرات ألتوس، هو كسر الشفرة. باختبار ثلاثة جداول علاجية مختلفة على الفئران ، بدءًا من منتصف العمر أو متأخرًا ، وجد الفريق أن دفعات قصيرة من عوامل ياماناكا تجدد شباب الجلد والكلى في الفئران التي تتلقى علاجات طويلة الأمد. يشبه ملف تعريف التعبير الجيني الخاص بها تلك الموجودة في الفئران الأصغر سنًا ، مع وجود علامات على التمثيل الغذائي للشباب.
كان أكبر مكسب هو أن العلاج لم يترك أي علامات على وجود ورم مسخي أو مشاكل صحية أخرى. "ما أردنا حقًا تحديده هو أن استخدام هذا النهج لفترة زمنية أطول يعد آمنًا ،" محمد مؤلف الدراسة الدكتور براديب ريدي.
إن تجديد الخلايا لدى البشر المتقدمين في السن سيكون أصعب بكثير ، بالنظر إلى مخاطر الآثار الجانبية الخطيرة. يعمل العلماء على بدائل للعلاج الجيني لعوامل ياماناكا. إذا نجحت ، يمكن أن يطلق السعي وراء علاجات جديدة جذرية لإبطاء أو عكس الأمراض التي تظهر مع تقدم العمر ، مثل هشاشة العظام والسكري والخرف.
"يتمثل هدفنا النهائي في إيجاد أشكال جديدة لمساعدة الجميع على إبطاء أو حتى عكس العمليات التي تؤدي إلى المرض ،" محمد Izpisua إلى إل باييس. "أنا مقتنع أنه في غضون عقدين من الزمن سيكون لدينا أدوات لا تعالج الأعراض فحسب ، بل يمكنها أيضًا التنبؤ بالأمراض والشيخوخة والوقاية منها وعلاجها من خلال تجديد الخلايا".
Tick-Tock يذهب إلى الساعة اللاجينية
كيف تعرف عمر الخلية؟
تكمن إجابة واحدة في الساعة اللاجينية. إذا كانت جيناتنا عبارة عن جمل ، فإن علم التخلق هو "علامات" كيميائية تخبر الجين ، مثل تحرير الملاحظات ، متى يتم تشغيله أو إيقاف تشغيله. إنها الطريقة التي تمتلك بها خلايانا - لنقل الخلايا العصبية وخلايا الجلد - نفس الحمض النووي ولكنها تبدو وتعمل بشكل مختلف تمامًا.
هذه الملاحظات ليست عشوائية. مع تقدمنا في العمر ، تكون بعض أحرف الحمض النووي أكثر عرضة للتعديل. أحد "القلم" القوي بشكل خاص هو المثيلة ، التي تضيف مجموعة كيميائية إلى أجزاء مختارة من الحمض النووي وتغلق الجين بشكل فعال. ترتبط هذه الأنماط ارتباطًا وثيقًا بالعمر الزمني (عدد السنوات التي عشتها) ، لدرجة أنها تستخدم على نطاق واسع كمؤشر بيولوجي للشيخوخة. بطريقة ما ، تمثل هذه العلامات الكيميائية تاريخ حياة الخلية.
أدخل عوامل Yamanaka. حساء البروتينات التي تنظم التعبير عن الحمض النووي - Oct4 ، Sox2 ، Klf4 ، و c-Myc - سميت باسم الدكتورة شينيا ياماناكا. تم وصف العوامل لأول مرة في عام 2006 ، حيث تمحو المشهد اللاجيني للخلية - بما في ذلك أنماط المثيلة - وتحول الخلايا النامية مرة أخرى إلى حالة جنينية. بشرت الدراسة الحائزة على جائزة نوبل بعصر الخلايا الجذعية المستحثة (iPSCs) ، وهي مكونات أدمغة صغيرة, أجنة من صنع المختبر، والأعضاء المطبوعة بيولوجيا.
تمتلك أبحاث طول العمر تقاطعًا تاريخيًا طويلًا مع مجال الخلايا الجذعية ، وسرعان ما لفتت عوامل ياماناكا انتباه العلماء. لكنهم طرحوا سؤالاً منفصلاً: ماذا سيحدث إذا أعطينا الأنسجة الشيخوخة مجرد اندفاعة من جرعة التجديد؟
الجواب: الغطس في ينبوع الشباب. في عام 2016 ، فريق Izpisua Belmonte أظهرت أن دفعات قصيرة من العوامل تصدت لعلامات الشيخوخة وزيادة العمر الافتراضي في نموذج فأر وراثي للشيخوخة السريعة. ومما يثير الدهشة أن العلاج أدى أيضًا إلى تجديد العضلات والتمثيل الغذائي في الفئران البالغة من العمر 12 شهرًا ، وهو ما يعادل البشر في منتصف العمر. وجد العمل اللاحق أيضًا أن العوامل حسنت القلب والعصب البصري ووظيفة الدماغ ، واكتسبت اهتمامًا واسع النطاق.
"نحن نستثمر في هذا المجال [لأنه] أحد التدخلات القليلة التي نعرفها والتي يمكنها استعادة وظيفة الشباب في مجموعة متنوعة من أنواع الخلايا ،" محمد الدكتور جاكوب كيميل في كاليكو ل التكنولوجيا الحيوية الطبيعة.
وصفة للشباب
لبناء نظام إعادة البرمجة الجزئية ، طرح الفريق بعض الأسئلة. متى يجب أن نبدأ العلاج؟ إلى متى يجب أن تستمر؟
لقد عملوا مع ثلاث مجموعات مختلفة من الفئران. كانت إحدى الدراسات قصيرة ، حيث بدأت العلاج في عمر 25 شهرًا - أي ما يعادل 80 عامًا تقريبًا في عمر الإنسان - ولمدة شهر واحد فقط. أخذ الاثنان الآخران الطريق الأطول. بدأت إحدى المجموعات في منتصف العمر ، والأخيرة في حوالي 35 عامًا في سنوات البشر. تلقى كلاهما العلاج حتى 22 شهرًا ، أو حوالي 70 عامًا في البشر. تم تعديل جميع الفئران وراثيًا بحيث يمكن تشغيل عوامل Yamanaka عن طريق ضخ مياه الشرب باستخدام مادة كيميائية لمدة يومين في الأسبوع.
الاخبار الجيدة؟ لم تظهر على أي من الفئران علامات مسخي. كانت الفئران أيضًا طبيعية في ملف الدم وأظهرت سلوكيات توتر وقلق مماثلة لأقرانها الذين لم يخضعوا للعلاج.
الأخبار السيئة؟ العلاج قصير الأمد بالعوامل لم يكن له تأثير كبير. ظلت ساعاتهم اللاجينية عالقة في "وضع الشيخوخة" ، مع عدم وجود تحسينات ملحوظة في وظائف الجسم. سبب الفشل غير واضح. قد لا تكون الدفقات قصيرة المدى كافية لتجديد الخلايا ، أو يمكن حبس جينومات الفئران المسنة في حالة "تجميد" أثناء الشيخوخة ، مما يجعل إعادة البرمجة غير فعالة.
حظت الفئران ذات المسافات الطويلة بحظ أفضل. تم تقييم ساعاتهم اللاجينية لعدة أعضاء: الكبد والكلى والجلد والعضلات والطحال والرئتين. كان للجلد أفضل استجابة للعلاج ، مع عكس العمر اللاجيني. في اختبار التئام الجروح ، عزز العلاج قدرة الفئران على التئام جلدها دون تندب ، والتي عادة ما تصبح مشكلة في سن الشيخوخة. وجد الفريق ، من خلال التنميط الجيني للأنسجة ، جينات منظمة تشارك في مكافحة الإجهاد التأكسدي - وهي عملية خلوية تدمر الأنسجة وتزداد مع تقدم العمر - وزيادة أخرى في الجينات لتثبيط الالتهاب والشيخوخة.
من خلال تحديد خصائص التمثيل الغذائي للفئران ، منع العلاج القوارض الكبيرة من مستويات الدهون الدهنية الخطيرة في الدم - وهو مقياس شائع للصحة أثناء الشيخوخة - ومظهر استقلاب أفضل. يحتاج العمل المستقبلي إلى معرفة ما إذا كانت هذه "تعكس التمثيل الغذائي الصحي" ، كتب أريانا ماركل والدكتور جورج كيو دالي في مستشفى بوسطن للأطفال وجامعة هارفارد ، اللذان لم يشاركا في الدراسة. على سبيل المثال ، يمكن أن تكون التغييرات في التعبير الجيني قادرة على محاربة زوبعة من الاضطرابات الأيضية التي تحدث عادة مع تقدم العمر ، ومحاربة مرض السكري ، وارتفاع الكوليسترول ، أو أمراض التمثيل الغذائي الأخرى المرتبطة بالعمر.
إلو أين سيقودنا هذا الأمر؟
أظهرت الدراسة ، لأول مرة ، أنه من الممكن إرجاع الساعة اللاجينية في الفئران التي تتقدم في العمر بشكل طبيعي باستخدام نبضات عوامل ياماناكا دون التعرض لخطر الإصابة بالسرطان. لكنه يترك الكثير من الأسئلة.
على رأس القائمة لماذا لم يتم تجديد شباب جميع الأنسجة. احتفظت أنسجة الكبد والعضلات والطحال والرئة ببرمجتها اللاجينية القديمة. في حين أنه من المحتمل أن الأنسجة المختلفة قد تحتاج إلى أنظمة علاج مخصصة لمكافحة الشيخوخة ، فمن الممكن أيضًا أن يكون لكل منها "نقطة اللاعودة" الغامضة ، وبعد ذلك لا يستجيب النسيج لإعادة البرمجة الخلوية.
إلى Markel و Daley ، اللذين شاركا في الكتابة قطعة رأي، لم تبلغ الدراسة أيضًا عن أفضلية أبحاث الشيخوخة: هل عاشت الفئران لفترة أطول؟
مشكلة أخرى هي العلاج الجيني طويل الأمد وشديد التعقيد. إذا تم استخدامه في البشر ، فإنه يضيف طبقة من التعقيد نظرًا لأعمارنا الأطول بكثير. تقوم العديد من المعامل ، بما في ذلك Daley's ، بتجربة عوامل فردية ذات قوى إصلاحية ، مما يلغي الحاجة إلى حساء علاجي من أربعة جينات. يقوم آخرون بفك رموز الأساس البيولوجي لعوامل ياماناكا بهدف تطوير عقاقير يمكن أن تحاكي العملية.
قال ريدي: "في نهاية اليوم ، نريد إعادة المرونة والعمل مرة أخرى إلى الخلايا القديمة حتى تكون أكثر مقاومة للإجهاد ، والإصابة ، والمرض". "تُظهر هذه الدراسة أنه ، على الأقل في الفئران ، هناك طريق للمضي قدمًا لتحقيق ذلك."
الصورة الائتمان: نيك فوينجز on Unsplash
- "
- 2016
- 70
- من نحن
- الذين تتراوح أعمارهم بين
- الكل
- القلق.
- نهج
- المنطقة
- حول
- أساس
- البداية
- أفضل
- بيزوس
- أكبر
- التكنولوجيا الحيوية
- دم
- الجسدي
- بوسطن
- نساعدك في بناء
- اشتعلت
- مادة كيميائية
- ساعة حائط
- الكود
- مشترك
- حول الشركة
- مجمع
- استطاع
- ائتمان
- اندفاع
- يوم
- تطوير
- فعل
- مختلف
- مرض
- الأمراض
- الحمض النووي
- بشكل كبير
- المخدرات
- الآثار
- لاستخدامات كبار السن
- إنشاء
- كل شخص
- مثال
- العوامل
- فشل
- الشكل
- الاسم الأول
- لأول مرة
- أشكال
- إلى الأمام
- وجدت
- نافورة
- وظيفة
- إضافي
- مستقبل
- جورج
- إعطاء
- هدف
- خير
- تجمع
- يحدث
- هارفارد
- صحة الإنسان
- مرتفع
- جدا
- تاريخي
- تاريخ
- كيفية
- كيفية
- HTTPS
- الانسان
- البشر
- هوية
- بما فيه
- زيادة
- مصلحة
- الاستثمار
- المشاركة
- قضية
- IT
- جيف بيزوس
- مختبرات
- آخر
- إطلاق
- قيادة
- يترك
- ليد
- قائمة
- مقفل
- طويل
- طويل الأجل
- بدا
- القيام ب
- نموذج
- شهر
- المقبلة.
- الأكثر من ذلك
- يتحرك
- الطبيعة
- أخبار
- عادي
- ملاحظة
- عدد
- مراجعة
- أخرى
- وفرة
- البوينت
- ممكن
- تنبأ
- المشكلة
- مشاكل
- عملية المعالجة
- العمليات
- ملفي الشخصي
- جانبي
- برمجة وتطوير
- سؤال
- سباق
- بقي
- تقرير
- بحث
- استجابة
- النتائج
- عكس
- خزنة
- قال
- العلماء
- طقم
- قصير
- لوحات
- وادي السيليكون
- مماثل
- بيج
- So
- بداية
- بدأت
- البدء
- الولايه او المحافظه
- جذع
- الإستراتيجيات
- إجهاد
- قوي
- دراسة
- ناجح
- فريق
- تجربه بالعربي
- الاختبار
- عبر
- الوقت
- أدوات
- تيشرت
- تحول
- علاج
- علاج
- تحريف
- جامعة
- us
- تستخدم
- مرئي
- مطلوب
- مياه
- موجة
- أسبوع
- ابحث عن
- في حين
- من الذى
- واسع الانتشار
- كسب
- في غضون
- بدون
- للعمل
- عمل
- عامل
- سوف
- سنوات