الورم الميلانيني الجلدي هو أخطر أنواع سرطانات الجلد ، خاصة بسبب ميله إلى غزو وتطوير النقائل في المواقع البعيدة. إنه الورم الخبيث الأساسي الثالث بعد سرطان الرئة والثدي الذي يستعمر الدماغ بشكل تفضيلي ، مع حدوث تطور ورم خبيث في الدماغ.
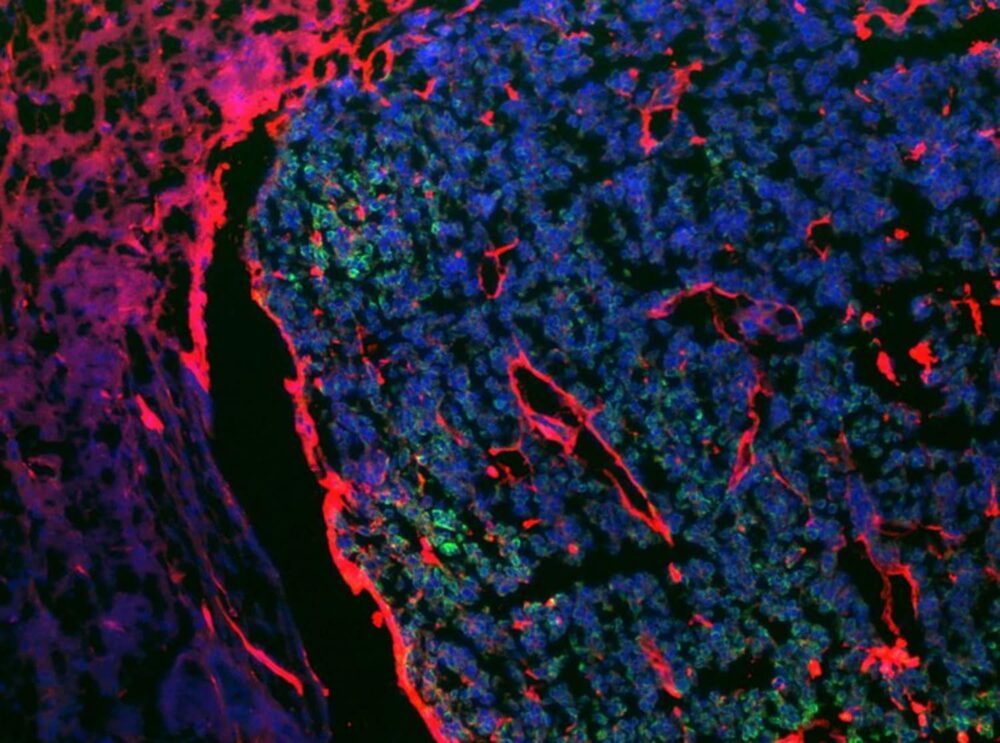
لأول مرة ، علماء من جامعة تل أبيب كشف آلية تمكن سرطان الجلد من الانتقال إلى الدماغ وتمكن من تأخير انتشار المرض بنسبة 60٪ إلى 80٪ باستخدام العلاجات الحالية. وجدوا أن الخلايا السرطانية "تجند" الخلايا النجمية ، وهي خلايا على شكل نجمة تقع في النخاع الشوكي والدماغ المسؤولة عن الحفاظ على التوازن ، أو الظروف المستقرة ، في الدماغ، في مرضى الورم الميلانيني مع نقائل الدماغ.
قال البروفيسور رونيت ساتشي فينارو ، "في مرحلة متقدمة ، يصاب 90٪ من مرضى سرطان الجلد (سرطان الجلد) بنقائل دماغية. هذه إحصائية محيرة. نتوقع رؤية نقائل في الرئتين والكبد ، لكن من المفترض أن يكون الدماغ عضوًا محميًا. يمنع الحاجز الدموي الدماغي المواد الضارة من دخول الدماغ ، ومن المفترض أنه لا يقوم بهذه المهمة هنا - فالخلايا السرطانية من الجلد تنتشر في الدم وتتمكن من الوصول إلى الدماغ. سألنا أنفسنا "مع من" تتحدث "الخلايا السرطانية" في الدماغ لاختراقها ".
قال البروفيسور ساتشي فاينارو ، "الخلايا النجمية هي أول من يأتي لتصحيح الموقف في حالة حدوث سكتة دماغية أو صدمة ، على سبيل المثال ، ومعها يكون سرطان الخلايا تتفاعل وتتبادل الجزيئات وتفسدها. علاوة على ذلك ، تقوم الخلايا السرطانية بتجنيد الخلايا النجمية بحيث لا تمنع انتشار النقائل. على هذا النحو ، فإنها تخلق التهابًا موضعيًا في مناطق تفاعل خلايا الورم الميلاني والخلايا النجمية التي تزيد من النفاذية من خلال الحاجز الدموي الدماغي وانقسام الخلايا السرطانية وانتقالها ".
"ينعكس الاتصال بينهما في حقيقة أن الخلايا النجمية تبدأ في إفراز بروتين يعزز الالتهاب يسمى MCP-1 (المعروف أيضًا باسم CCL2) ، واستجابة لذلك ، تبدأ الخلايا السرطانية في التعبير عن مستقبلاتها CCR2 و CCR4 ، التي اشتبهنا في أنها مسؤولة عن الاتصال المدمر مع الخلايا النجمية. "
اختبر العلماء فرضيتهم عن طريق تثبيط تعبير البروتين ومستقبلاته في نماذج معملية معدلة وراثيًا ونماذج ثلاثية الأبعاد لورم الميلانوما الأولية ونقائل الدماغ. استخدموا كلاً من الجسم المضاد (الجزيء البيولوجي) وجزيء صغير (اصطناعي) مصمم لمنع بروتين MCP-3.
كما استخدموا تقنية كريسبر لتعديل الخلايا السرطانية وراثيًا وقطع الجينين اللذين يعبران عن المستقبلين المرتبطين ، CCR2 و CCR4. مع كل طريقة ، يمكن للباحثين تأخير انتشار النقائل.
البروفيسور ساتشي فينارو محمد, نجحت هذه العلاجات في تأخير تغلغل الخلايا السرطانية في الدماغ وانتشارها لاحقًا في جميع أنحاء الدماغ. من المهم ملاحظة أن نقائل الورم الميلانيني في الدماغ شديدة العدوانية ، مع تشخيص سيئ لمدة 15 شهرًا بعد الجراحة والإشعاع و العلاج الكيميائي. اعتمادًا على مرحلة التدخل ، وصلنا إلى 60٪ إلى 80٪ تأخير ".
“لقد حققنا أفضل النتائج من خلال العلاج الذي أجري مباشرة بعد الجراحة لإزالة الورم الميلانيني الأولي ، وتمكنا من منع النقائل من اختراق الدماغ ؛ لذلك أعتقد أن العلاج مناسب للعيادة كإجراء وقائي ".
"تم اختبار كل من الجسم المضاد والجزيء الصغير الذي استخدمناه - والذي يهدف أساسًا إلى علاج التصلب والسكري وتليف الكبد وأمراض القلب والأوعية الدموية ، بالإضافة إلى استخدامه كمؤشر حيوي لأنواع أخرى من السرطان - على البشر كجزء من التجارب السريرية . لذلك ، هذه العلاجات آمنة ، ويمكننا محاولة إعادة استخدامها لعلاج سرطان الجلد ".
المرجع مجلة:
- سابينا بوتزي وآنا سكومبارين وآخرون. تثبيط محور MCP-1 / CCR2 يحسس البيئة الدقيقة للدماغ ضد تطور ورم خبيث في الدماغ. JCI Insight. دوى: 10.1172 / jci.insight.154804