Smertelindring opnås normalt ved at bruge håndkøbs smertestillende medicin såsom paracetamol eller anti-inflammatoriske lægemidler; mere alvorlige smerter kan kræve opioider, som kan have bivirkninger og føre til afhængighed. Forskere ved Virginia Tech undersøger en anden tilgang til smertebehandling, der slet ikke bruger medicin, men i stedet retter sig mod et bestemt punkt i hjernen med fokuseret ultralyd.
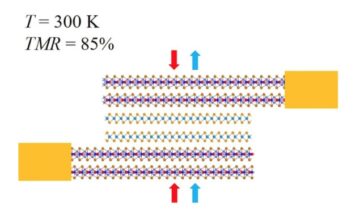
Insula er et område i hjernen, der er forbundet med opfattelsen af smerte. Dens placering dybt i hjernebarkens folder gør den dog svær at få adgang til. Lav-intensitet fokuseret ultralyd (LIFU), hvor ultralydsstråler konvergeres til et lille sted, kunne give en måde at målrette sådanne dybe strukturer ikke-invasivt med høj rumlig opløsning.
I et dobbeltblindt klinisk studie, ledet af Wynn Legon fra Fralin Biomedicinsk Forskningsinstitut ved VTC, undersøgte holdet, om brug af LIFU til ikke-kirurgisk at ændre neuronal aktivitet kan reducere både opfattelsen af smerte og kroppens reaktion på en smertefuld stimulus, såsom ændringer i hjertefrekvens.
"LIFU giver høj rumlig specificitet kombineret med evnen til at fokusere til forskellige dybder," forklarer Legon. "Dette giver således adgang til flere svære at målrette hjerneregioner uden operation. Det har også fordelen – som alle enhedsbaserede muligheder – ved at være ikke-afhængighedsskabende.”
Legon og kolleger undersøgte 23 raske frivillige ved at bruge metoden kontakt varmefremkaldt potentiale (CHEP) til at vurdere smertebehandling. CHEP virker ved at levere korte varmestimuli til hånden til et niveau, der vurderes til at være moderat smertefuldt (omkring fem på en smerteresponsskala fra nul til ni). Varmestimulus genererer en CHEP-bølgeform, som kan måles via en elektroencefalografi (EEG) elektrode på hovedbunden.
Hver deltager deltog i fire sessioner, den første omfattede anatomisk MR- og CT-scanning plus baseline-spørgeskemaer. I de andre tre sessioner blev frivillige udsat for 40 CHEP-stimuli (300 ms hver) under levering af LIFU (i 1 s) til enten den anteriore insula (AI) eller den posteriore insula (PI) eller en inert sham-eksponering.
Forskerne brugte en ultralydstransducer koblet til hovedet med konventionel gel til at levere fokuseret ultralyd med millimeteropløsning. De brugte også en brugerdefineret koblingspuck designet ved hjælp af hver enkelt persons MR-scanninger til at placere fokuspunktet nøjagtigt på de isolerede mål.
Hovedmålet med undersøgelsen, rapporteret i tidsskriftet SMERTE, var at bestemme, om LIFU til AI eller PI kunne hæmme smerte, som vurderet af deltagerne under hver CHEP-session. Forskerne brugte også elektrokardiografi (EKG) til at undersøge, hvordan LIFU påvirkede hjertefrekvens og hjertefrekvensvariabilitet, og vurderede dens indvirkning på CHEP-bølgeformen.
Holdet fandt ud af, at LIFU til både AI og PI reducerede smertevurderinger. Gennemsnitsreaktioner på de 40 CHEP-stimuli for hvert individ resulterede i gennemsnitlige smertevurderinger på 3.03±1.42, 2.77±1.28 og 3.39±1.09 for henholdsvis AI, PI og sham-eksponering. Forskellen mellem PI og sham-stimulering var statistisk signifikant, mens forskelle mellem AI og sham eller AI og PI ikke var det.
Legon bemærker, at selvom denne reduktion på omkring tre fjerdedele af et punkt på smerteskalaen kan virke ret lille, så er det på grænsen til at være klinisk meningsfuldt, når først dette når et fuldt point. "Det kan gøre en væsentlig forskel i livskvaliteten eller at kunne håndtere kroniske smerter med håndkøbsmedicin i stedet for receptpligtige opioider," forklarer han i en pressemeddelelse.
For at vurdere virkningen af LIFU af CHEP-bølgeformen målte forskerne peak-to-peak amplituden fra den første store negative (N1) til den første store positive (P1) afbøjning i EEG. Top-to-peak-amplituderne var 23.35±11.58, 22.90±12.35 og 27.79±10.78 mV for henholdsvis AI, PI og sham-eksponering. Analyse afslørede en signifikant forskel mellem sham og AI, og sham og PI, men ikke mellem AI og PI.
Holdet observerede, at levering af fokuseret ultralyd til AI eller PI påvirkede CHEP-sporet på forskellige måder. LIFU til PI påvirkede tidligere EEG-amplituder, mens LIFU til AI påvirkede senere EEG-amplituder, hvilket antyder, at modulering af PI og AI forårsager forskellige fysiske effekter.
Legon fortæller Fysik verden at det før dette studie ikke var muligt ikke-kirurgisk at undersøge, hvordan forskellige regioner af insula bidrager til smerteoplevelsen, eller hvordan nociceptiv (smerterelateret) information videregives fra det ene område til det andet. Millimeteropløsningen af LIFU muliggør dog specifik målretning af tæt beliggende regioner for at lede efter specifikke effekter.

Hjernestimulation giver smertelindring uden uønskede bivirkninger
"Tidligere invasive dybdeelektrodeoptagelser havde vist, at nociceptiv information blev videregivet i rum og tid fra PI til AI," siger han. "Vores resultater rekapitulerede dette ikke-invasivt, hvilket er et vigtigt fund."
LIFU påvirkede ikke deltagernes middelpuls under CHEP-stimuli. Forskerne så dog en signifikant forskel i hjertefrekvensvariabiliteten mellem sham og AI-eksponering. LIFU til AI øget hjertefrekvensvariabilitet, hvilket er forbundet med bedre overordnet helbred.
Holdet undersøger nu leveringen af LIFU til forskellige hjerneområder som et potentielt smertebehandlingsmiddel. "Vi ved endnu ikke, hvilken dosering der er passende, eller hvilke specifikke parametre der kan føre til klinisk meningsfulde resultater," forklarer Legon. "Således begynder vi at teste LIFU for smertelindring i kroniske smertepopulationer. Vi undersøger også anvendeligheden af LIFU til andre kliniske indikationer såsom angst og afhængighed."
Ledsager studie
I en separat undersøgelse offentliggjort i Journal of Neuroscience, undersøgte Virginia Tech-teamet brugen af LIFU til ikke-invasivt at modulere den dorsale anterior cingulate cortex (dACC), et kritisk hjerneområde for smertebehandling og autonom funktion. Forskerne undersøgte 16 raske frivillige ved at bruge den samme CHEP-procedure beskrevet ovenfor under påføring af LIFU eller en falsk eksponering.
Undersøgelsen afslørede, at LIFU til dACC reducerer smerte og ændrer autonome reaktioner på akutte varmesmertestimuli. Ultralydseksponering reducerede smertevurderinger med 1.09±0.20 point i forhold til sham-eksponering. LIFU øgede også hjertefrekvensvariabiliteten og resulterede i en 38.1 % reduktion i P2-amplituden i CHEP-bølgeformen.
- SEO Powered Content & PR Distribution. Bliv forstærket i dag.
- PlatoData.Network Vertical Generative Ai. Styrk dig selv. Adgang her.
- PlatoAiStream. Web3 intelligens. Viden forstærket. Adgang her.
- PlatoESG. Kulstof, CleanTech, Energi, Miljø, Solenergi, Affaldshåndtering. Adgang her.
- PlatoHealth. Bioteknologiske og kliniske forsøgs intelligens. Adgang her.
- Kilde: https://physicsworld.com/a/can-focused-ultrasound-provide-a-new-way-to-manage-pain/
- :har
- :er
- :ikke
- 09
- 1
- 16
- 160
- 20
- 2023
- 22
- 23
- 27
- 28
- 300
- 35 %
- 40
- 58
- a
- evne
- I stand
- over
- adgang
- opnået
- aktivitet
- afhængighed
- negativ
- påvirke
- påvirket
- AI
- Alle
- også
- Skønt
- an
- analyse
- ,
- Andrew
- En anden
- Angst
- Anvendelse
- tilgang
- passende
- ER
- OMRÅDE
- områder
- omkring
- AS
- vurdere
- vurderes
- forbundet
- At
- gennemsnit
- Baseline
- BE
- før
- Begyndelse
- være
- gavner det dig
- Bedre
- mellem
- biomedicinsk
- både
- Brain
- men
- by
- CAN
- Årsag
- Ændringer
- Klinisk
- nøje
- kolleger
- kombineret
- omfattende
- kontakt
- bidrage
- konventionelle
- kunne
- koblede
- kritisk
- skik
- dyb
- levere
- leverer
- leverer
- levering
- demonstrere
- demonstreret
- Dybder
- beskrevet
- konstrueret
- Bestem
- DID
- forskel
- forskelle
- forskellige
- distinkt
- do
- Er ikke
- dosering
- Narkotika
- i løbet af
- hver
- tidligere
- effekter
- enten
- selvstændige
- muliggør
- præcist nok
- undersøge
- Undersøgelse
- erfaring
- Forklarer
- Eksponering
- finde
- Fornavn
- fem
- brændvidde
- Fokus
- fokuserede
- folder
- Til
- fundet
- fire
- fra
- fuld
- funktion
- genererer
- mål
- havde
- hånd
- Hård Ost
- Have
- he
- hoved
- Helse
- sund
- Hjerte
- Høj
- Hvordan
- Men
- HTML
- HTTPS
- KIMOs Succeshistorier
- påvirket
- vigtigt
- in
- øget
- indikationer
- oplysninger
- i stedet
- Institut
- ind
- invasiv
- undersøge
- undersøge
- undersøgelse
- spørgsmål
- IT
- ITS
- tidsskrift
- jpg
- bedømt
- Kend
- stor
- senere
- føre
- Led
- til venstre
- Niveau
- placeret
- placering
- Se
- Main
- lave
- maerker
- administrere
- ledelse
- max-bredde
- Kan..
- betyde
- meningsfuld
- metode
- moderat
- mere
- MRI
- MS
- negativ
- Ny
- ni
- Noter
- nu
- of
- on
- engang
- ONE
- opioider
- Indstillinger
- or
- Andet
- over disken
- samlet
- Smerte
- smertebehandling
- smertefulde
- parametre
- deltager
- deltagere
- opfattelsen
- fysisk
- Fysik
- Fysik verden
- Place
- plato
- Platon Data Intelligence
- PlatoData
- plus
- Punkt
- punkter
- populationer
- positiv
- mulig
- potentiale
- recept
- trykke
- procedure
- forarbejdning
- give
- giver
- offentliggjort
- helt
- Sats
- nominel
- ratings
- når
- reaktion
- reducere
- Reduceret
- reducerer
- reduktion
- region
- regioner
- relative
- relief
- rapporteret
- kræver
- forskning
- forskere
- Løsning
- henholdsvis
- svar
- reaktioner
- resulterer
- Resultater
- Revealed
- groft
- s
- samme
- siger
- Scale
- scanning
- scanninger
- se
- synes
- adskille
- Session
- sessioner
- flere
- svær
- side
- signifikant
- lille
- Space
- Rum og tid
- rumlige
- specifikke
- specificitet
- Spot
- Statement
- stimulus
- stress
- strukturer
- studeret
- Studere
- emne
- sådan
- Kirurgi
- mål
- rettet mod
- mål
- hold
- tech
- fortæller
- prøve
- at
- de
- denne
- tre
- thumbnail
- tid
- til
- Trace
- sand
- brug
- anvendte
- ved brug af
- sædvanligvis
- nytte
- Varierende
- via
- Virginia
- frivillige
- var
- Vej..
- måder
- we
- var
- Hvad
- hvorvidt
- som
- mens
- med
- uden
- virker
- world
- endnu
- zephyrnet
- nul