Protonterapi kan levere meget konforme dosisfordelinger til et tumormål, mens dosis til væv uden for målvolumenet minimeres. At skabe behandlingsplaner, der realiserer denne styrke, er en topprioritet for dosimetrister og medicinske fysikere.
Protoner afsætter dosis på en fundamentalt anderledes måde end røntgenstråler, en anden type ekstern strålebehandling. Når en proton når slutningen af sin bane, øges den hastighed, hvormed dens energi overføres til væv - dens lineære energioverførsel (LET), udtrykt i keV/µm.
Den relative biologiske effektivitet (RBE) fanger de biologiske implikationer af at øge LET, og en fast RBE-værdi på 1.1 anvendes ofte til kliniske protonbehandlinger. Men proton RBE er afhængig af mange andre faktorer, herunder kliniske endepunkter, vævstype, fraktioneringsskema, patientspecifik radiosensitivitet, fysisk dosis og usikkerheder i eksperimentelle målinger. Som følge heraf undervurderer brugen af en fast RBE-værdi i protonterapi sandsynligvis RBE på steder med høj LET, hvilket kan resultere i en øget risiko for strålingsinducerede toksiciteter.
Alligevel er LET stærkt korreleret med RBE og er en nøglefaktor for bestemmelse af variabel RBE i protonterapi. Som sådan undersøger forskere metoder til at beregne og evaluere LET under behandlingsplanlægning. Disse biologiske behandlingsplanlægningsværktøjer er dog begrænsede, og indtil de er udviklet og studeret yderligere, skal klinikker identificere deres egen behandlingsplanlægningspraksis for at minimere LET uden for målvolumener, siger Austin Faught, en medicinsk fysiker ved St Jude Children's Research Hospital i Tennessee.
"Hvordan man kan påvirke [LET-distributionen] er et aktivt forskningsområde, og der er nogle fantastiske metoder under udvikling," forklarer Faught. "Problemet, vi står over for, er, at disse ikke er let tilgængelige uden tilpasset software udviklet internt eller gennem specielle forskningsversioner af leverandørleverede applikationer ... [og der er] få undersøgelser, der giver kvantitativ vejledning om, hvad vi bør sigte efter."
Behandlingsplanlægningsstrategier
Som et skridt mod LET-baseret planevaluering og optimering for fotonterapi udførte Faught og hans team en undersøgelse af planlægningsstrategier, der er kommercielt tilgængelige for kliniske teams til intensitetsmoduleret protonterapi (IMPT). Deres undersøgelse, rapporteret i Journal of Applied Clinical Medical Physics, introducerer nogle vejledninger til planlæggere af protonterapibehandling. "Vi ønskede at se på nogle let tilgængelige behandlingsplanlægningsteknikker, og hvordan de kan påvirke LET," forklarer Faught.
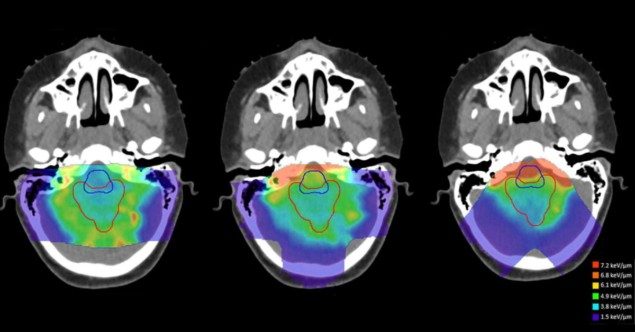
Forskerne evaluerede forskellene i dosisvægtet LET (LETd) mellem otte fremadbaserede behandlingsplanlægningstilgange anvendt på et cylindrisk vandfantom og fire pædiatriske hjernetumortilfælde (Faught bemærker, at strålingsinduceret toksicitet er et fokusområde for holdet). De sammenlignede disse planlægningsstrategier med en plan med modsatte laterale stråler (for fantomet) eller med den oprindelige kliniske plan (for patienter), ved at bruge Monte Carlo sekundære beregninger til at evaluere både dosis og LETd.
Forskerne fandt ud af, at behandlingsfeltgeometri var den største bidragyder til placeringen af høj-LET områder. For at afbøde den potentielle påvirkning af biologiske usikkerheder forbundet med høj LETd, foreslår de, at behandlingsplanlæggere bruger store skæringsvinkler mellem behandlingsbjælker og undgår bjælker, der stopper umiddelbart proksimalt for kritiske strukturer.
"Dette er gode nyheder, da det betyder, at omhyggelig udvælgelse af antallet af behandlingsfelter og deres orientering med hensyn til nærliggende sundhedsvæv kan være effektive," siger Faught. "Med nogle bevidste, forudgående tanker, er det noget, alle behandlingsplanlæggere kan tage i betragtning under planlægningsprocessen."
Forskerne fandt også ud af, at brugen af en range shifter reducerede den gennemsnitlige LET betydeligtd i det kliniske målvolumen. Som følge heraf anbefaler de at bruge afstandsskiftere og alternative strategier med begrænsning af spotplacering sparsomt, og kun når klinikker kan beregne den resulterende LETd at evaluere i forhold til alternative planlægningsstrategier.
På grund af undersøgelsens lille stikprøvestørrelse kunne forskerne ikke fastslå en klar tendens i LETd variationer i de kliniske tilfælde. De evaluerede ikke forholdet mellem ændringer i LET og en ændring i sandsynligheden for tumorkontrol eller normale vævskomplikationer.
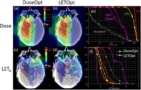
LET-baserede planer optimerer protonterapi
Mens virkningerne af hver planlægningstilgang på høj-LET-regioner var beskedne, siger Faught, at det er vigtigt at erkende, at teamets behandlingsplanlægningsstrategier og anbefalinger er evidensbaserede og let kan omsættes til klinisk praksis.
”Jeg håber, at en af fordelene er, at vi som felt vil drage fordel af kommercielle værktøjer, der giver mulighed for at beregne LET i behandlingsplanlægningssystemet. Endnu bedre, vi ville elske at have måder at optimere med LET i tankerne. Denne undersøgelse var en god bro, indtil disse værktøjer er mere udbredte," siger Faught.