Partikelterapi – kræftbehandling ved hjælp af stråler af protoner eller tungere ioner – giver meget konform dosistilførsel og større skånsomhed for normalt væv end konventionel fotonbaseret strålebehandling. Men for langsigtede kræftoverlevere er risikoen for strålingsinduceret sekundær cancer (SC) vigtig og bør overvejes, når de vælger deres behandlingsmodalitet.
Med knappe epidemiologiske data for nyere behandlinger såsom proton- og carbon-ion-terapi, ledte et hold op på GSI Helmholtz Center for Heavy Ion Research udvikler en model til at sammenligne SC-risici mellem partikelterapi-modaliteter. Modellen, beskrevet af Antonia Hufnagl og kolleger i Medicinsk fysik, kunne i sidste ende inkorporeres i behandlingsplanlægningssystemer for at inkludere SC-risiko som et yderligere optimeringskriterium.
Dødelige versus kræftfremkaldende hændelser
SC-risikomodeller fungerer typisk ved at overveje balancen mellem celledrab (der fører til kræftundertrykkelse) og celletransformation (induktion af mutationer, der i sidste ende fører til kræft). Sandsynligheden for, at et bestrålet volumen vil udvikle kræft, er defineret ved hjælp af den lineær-kvadratiske (LQ) model, som giver et simpelt forhold mellem celleoverlevelse og leveret fotondosis.
I denne undersøgelse brugte forskerne den lokale effektmodel (LEM) til at forudsige den relative biologiske effektivitet (RBE) af SC-induktion efter partikelterapi. For at tage højde for den øgede RBE af partikelstråling erstattede de foton-LQ-parametrene i risikomodellen med ionstråle-LQ-parametrene forudsagt af LEM. Et nøgletræk ved deres tilgang er brugen af LEM i både celledrab og cancerinduktion.

"Den dobbelte brug af LEM afspejler konkurrencen mellem de to store processer, der bestemmer SC-udvikling, nemlig celletransformation og celledrab," forklarer seniorforfatter Michael Scholz. "Med stigende dosis og/eller effektivitet kan celledrab undertrykke levedygtigheden af transformerede celler. Dette fører til et komplekst samspil, som ellers ikke blot kan afspejles i en et-trins procedure.”
For at undersøge, hvilke faktorer der påvirker SC-risikoen, brugte forskerne TPS TRiP98-planlægningssystemet til at generere biologisk optimerede carbon-ion- og protonbehandlingsplaner baseret på en idealiseret geometri. Planerne bestrålede et 4x4x4 cm mål med en enkelt partikelstråle eller to modstående stråler, med et 4x4x1 cm organ-at-risk (OAR) foran målet. På grund af usikkerheder i foton-LQ-parametrene, der blev brugt som input til LEM, estimerede de proton-til-carbon-ion-risikoforhold snarere end individuelle risikoværdier.
For disse idealiserede opstillinger viste modellen ikke en klar præference for hverken protoner eller carbonioner, men afslørede en kompleks afhængighed af forskellige parametre. Den reducerede laterale spredning af carbonioner fører til en lavere SC-risiko end protoner i indgangskanalen. Imidlertid afsætter carbonioner en højere dosis bag målet på grund af fragmenteringshalen, hvilket øger SC-risikoen for OAR'er bag tumoren efter carbon-ion-bestråling.
For enkeltstråleplaner var den samlede SC-risiko omtrent 1.5 gange højere for carbonioner end for protoner. Med to modstående stråler var den samlede SC-risiko 1.16 gange højere for protoner, selvom denne varierede stærkt afhængigt af den rumlige placering af det antagne følsomme volumen i forhold til målvolumenet.
Vævsstrålefølsomhed (over for fotoner) havde en stor indflydelse på SC-risikoforholdet, hvor radioresistente OAR'er drager fordel af carbon-ion-behandling og følsomme OAR'er fra protonstråler. Derimod havde fraktioneringsordningen ringe indflydelse på forventede risikoværdier.
Patientgeometri
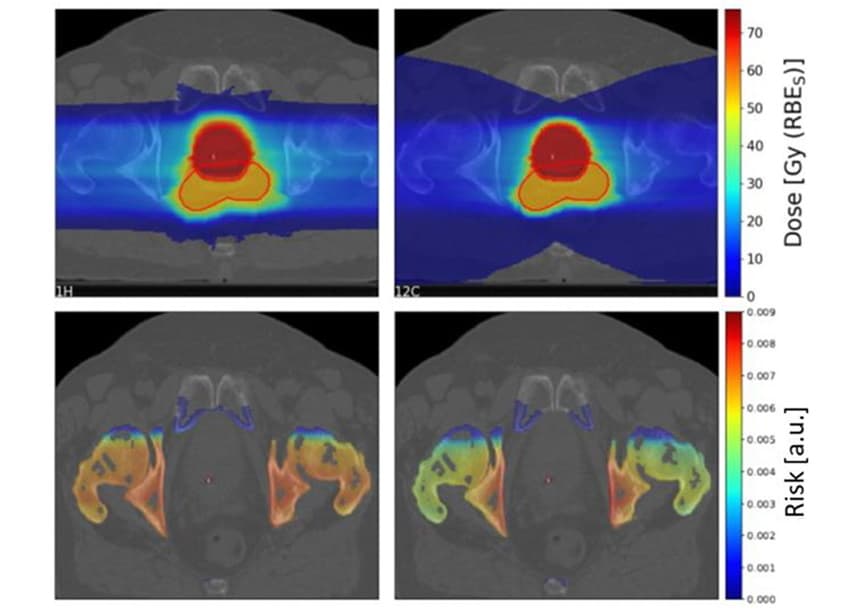
For at undersøge kliniske scenarier estimerede Scholz og kolleger SC-risikoen for 10 prostatacancerpatienter, der tidligere var behandlet med fotonstrålebehandling på Karolinska Universitetshospitalet. De genererede behandlingsplaner for patienterne ved hjælp af to lateralt modsatte scannede proton- og kulstof-ion-felter.
Som tidligere set resulterede fragmenteringshalen af kulstofioner i et stort lavdosisområde bag målet. Imidlertid var højdosis-målregionen mere konform for carbon-ionen end protonplanerne.
Holdet beregnede proton-til-carbonion SC-risikoforhold for fire OAR'er (blære, rektum, knogler og hud) for de 10 patienter. For knogler og hud gav protonplaner en lidt højere SC-risiko end carbon-ion-planer med medianrisikoforhold på henholdsvis 1.19 og 1.06 for knogler og hud. For blære og endetarm resulterede protonplaner imidlertid i signifikant lavere SC-risici med risikoforhold på henholdsvis 0.68 og 0.49 for blære og rektum.
Forskerne konkluderer, at den indsigt, denne model opnår, kan hjælpe med at optimere fremtidige behandlinger. I øjeblikket er relativ risikomodellering hovedsageligt velegnet som et værktøj til at sammenligne forskellige behandlingsscenarier for forskellige patientkohorter. Men Scholz bemærker, at det ville være ligetil at inkorporere sådanne modeller i behandlingsplanlægning for individuelle patienter.

Carbon ion gitterterapi skåner sundt væv
"Det kræver blot at køre planlægningen for en given dosisfordeling med to forskellige biologiske parametersæt, der repræsenterer henholdsvis celledrab og celletransformationsprocessen," forklarer han. "Så er det kun nødvendigt med en vis efterbehandling af de resulterende 3D-effektfordelinger med matematiske standardværktøjer for at udlede de tilsvarende risikoforholdsfordelinger."
Det næste skridt, siger han, er at validere modellen via sammenligning med kliniske data. "Da disse data på nuværende tidspunkt er knappe, ville en udvidelse af tilgangen til også at omfatte fotonbehandlinger og bestemmelse af de tilsvarende risikoforhold mellem protoner versus fotoner og carbonioner versus fotoner være et vigtigt næste skridt," fortæller Scholz Fysik verden.