Strålebehandling er en af de mest almindelige kræftbehandlinger, der effektivt forlænger overlevelsestiden og øger helbredelsesraten for kræftpatienter. Radioterapi-induceret knogleskader – herunder reduceret knoglemasse, øget knogleskørhed og højere risiko for frakturer og osteonekrose – er dog fortsat et almindeligt problem, som i øjeblikket mangler effektive modforanstaltninger.
Stråling forårsager denne skade ved at undertrykke væksten, overlevelsen og modningen af knogledannende celler kaldet osteoblaster og dermed hæmme knogledannelsen. Et potentielt middel kunne være udsættelse for ikke-invasive elektromagnetiske felter (EMF'er), som er kendt for at stimulere osteoblastvækst og differentiering og kunne afbøde virkningerne af bestråling. Nu har et forskerhold i Kina identificeret den optimale EMF-bølgeform for at maksimere effektiviteten af en sådan behandling, og rapporterer resultaterne i Science Forskud.
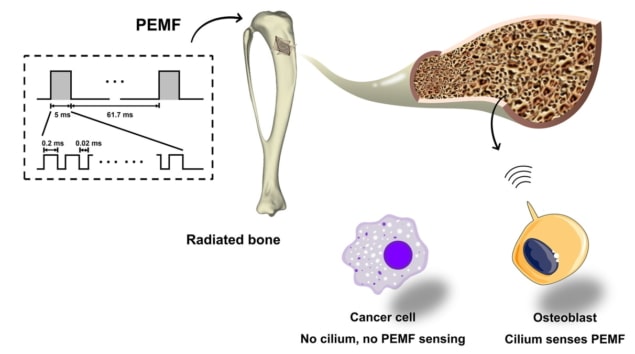
Da Jing, fra Fjerde Militærmedicinske Universitet, og kolleger udsatte først knogleceller for EMF-stimulering ved hjælp af forskellige bølgeformer, herunder sinusformet EMF, single-pulsed EMF og pulsed-burst EMF (PEMF). For at vurdere cellernes respons overvågede de intracellulær calciumion i realtid (Ca2+) signalering, en af de tidligste cellulære reaktioner på eksterne stimuli.
Holdet fandt, at PEMF inducerede mere robust intracellulær Ca2+ signalering i bestrålede osteoblaster end de andre bølgeformer, karakteriseret ved unikke Ca2+ svingninger med flere Ca2+ pigge. Yderligere analyser viste, at en tidligere uidentificeret PEMF-bølgeform med en magnetfeltintensitet på 2 mT og en frekvens på 15 Hz fremkaldte den stærkeste respons i osteoblaster. I modsætning hertil havde denne PEMF-bølgeform ingen effekt på andre typer af bestrålede knogleceller (osteoklaster og osteocytter).
Dernæst undersøgte forskerne, om PEMF leveret ved hjælp af disse optimale parametre kunne afbøde strålingsinduceret knogletab in vivo. I undersøgelser på rotter udsatte de en bagben for to 8 Gy-doser af fokal stråling (med en dags mellemrum) og brugte mikro-CT til at vurdere knoglestrukturen 45 dage senere. De bestrålede lemmer udviste signifikant trabekulært knogletab, herunder et cirka 50 % fald i knoglevolumenfraktion og knoglemineraltæthed sammenlignet med den ubestrålede side.
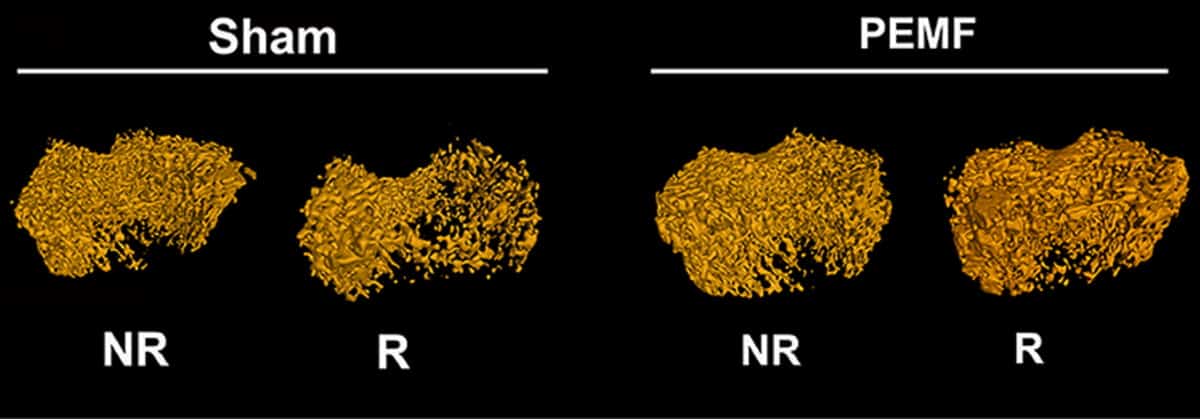
En anden gruppe rotter modtog dagligt helkrops-PEMF (2 timer/dag) i de 45 dage efter bestråling. Denne behandling genoprettede knoglemasse og mekaniske egenskaber i bestrålede baglemmer til niveauet for ikke-bestrålede lemmer ved at redde osteoblaster. Holdet bemærker, at PEMF ikke havde nogen effekt på dyrenes kropsvægt eller fødeindtagelse.
Efter at have vist, at PEMF-eksponering kan mindske strålingsinduceret knogletab, er det også vigtigt, at PEMF ikke har en negativ indvirkning på tumorbehandlingen. Med dette i tankerne sammenlignede forskerne følsomheden af osteoblaster og forskellige tumorceller (brystkræft, tyktarmskræft, malignt melanom og osteosarkomceller) med PEMF.
Bestråling reducerede cellelevedygtighed og fremmede apoptose i alle celletyperne. Det er afgørende, selvom PEMF forbedrede osteoblast-levedygtighed og hæmmede osteoblast-apoptose, havde det ingen effekt på levedygtighed eller apoptose i nogen af tumorcellerne på noget tidspunkt.
Levende bioblæk kan forbedre knoglereparation og regenerering
Forskerne tilskriver denne selektivitet tilstedeværelsen af primære cilia - sensoriske organeller, der detekterer og oversætter ekstracellulære mekaniske signaler - der fungerer som PEMF-sensorer. Disse primære cilia er meget rigelige i osteoblaster, men fraværende i de fleste tumorceller. I et eksperiment, hvor dannelsen af primære cilia i bestrålede osteoblaster blev blokeret, forsvandt den PEMF-medierede stigning i osteoblastoverlevelse og differentiering næsten fuldstændigt.
"I betragtning af, at blandt alle knoglecelletyper er osteoblaster særligt følsomme over for stråling, synes denne PEMF-kur, som inducerer den specifikke aktivering af osteoblaster, at være en lovende og yderst effektiv tilgang mod strålingsinduceret knogleskader," konkluderer forskerne.