HONGKONG, 17. Februar 2022 – (ACN Newswire) – SinoMab BioScience Limited („SinoMab“ oder das „Unternehmen“, zusammen mit seinen Tochtergesellschaften die „Gruppe“, Aktiencode: 3681.HK), ein in Hongkong ansässiges Biopharmazeutikum Das Unternehmen, das sich der Erforschung, Entwicklung, Herstellung und Vermarktung von Therapeutika zur Behandlung immunologischer Erkrankungen verschrieben hat, freut sich bekannt zu geben, dass am 11. Februar 2022 (EST-Ortszeit) ein Prüfantrag für ein neues Medikament ("IND") für das Unternehmen eingereicht wurde Das First-in-Class (FIC) Asthma-Therapeutikum SM17 (humanisierter monoklonaler Anti-IL17RB-Antikörper zur Injektion) wurde von der US-amerikanischen Food and Drug Administration ("FDA") eingereicht und akzeptiert. Das Unternehmen plant, die First-In-Human-Studie in den USA im ersten Quartal 2022 zu starten, sobald IND von der FDA zugelassen ist.
 |
SM17 ist der weltweit erste monoklonale Antikörper gegen IL17BR, der gemeinsam von SinoMab und LifeArc (einer medizinischen Forschungsorganisation mit Sitz im Vereinigten Königreich) entwickelt wurde. SM17 hat ein breites Indikationsspektrum, darunter Indikationen mit großem Marktvolumen wie Asthma und Krankheiten mit hohen Sterblichkeitsraten wie idiopathische Lungenfibrose. Im Vergleich zu anderen Produkten auf dem Markt genießt SM17 Differenzierungsvorteile. Aufgrund der präklinischen Daten und des einzigartigen Wirkmechanismus von SM17 ist das Unternehmen der Ansicht, dass SM17 möglicherweise eine breitere und vorteilhaftere Wirkung auf die Asthmabehandlung hat als andere zugelassene Biologika.
Auf dem Weltmarkt steigt die Zahl der Asthmapatienten allmählich und wird voraussichtlich bis 247.5 2023 Millionen erreichen und bis 267.7 weiter auf 2030 Millionen steigen. Die Zahl der Asthmapatienten in der VR China steigt schneller als die globale Rate und wird bis 25.6 voraussichtlich 2023 Millionen erreichen und bis 27.8 weiter auf 2030 Millionen steigen. Was die Marktgröße betrifft, so wird der weltweite Asthmamarkt bis 25.1 auf 2023 Milliarden US-Dollar und bis 34.6 auf 2030 Milliarden US-Dollar geschätzt Es wird erwartet, dass die PRC bis 36.4 2023 Milliarden RMB und bis 65.0 2030 Milliarden RMB erreichen wird. Was die Behandlungsoptionen betrifft, basiert die traditionelle Asthmabehandlung auf inhalativen Kortikosteroiden, aber sie sind anfällig für schwerwiegende Nebenwirkungen, insbesondere bei Jugendlichen. Bei längerer Anwendung können sich auch Resistenzen entwickeln. Es wird erwartet, dass die Einführung von SM17 eine bessere Behandlungsoption im Hinblick auf ein ausgewogenes Verhältnis von Wirksamkeit und Sicherheit bietet.
Dr. Shui On LEUNG, Chairman, Executive Director und Chief Executive Officer von SinoMab, sagte: „Nach der Annahme des IND-Antrags für SN1011 zur Behandlung von Multipler Sklerose durch die NMPA, der vollständigen Annahme des IND-Antrags für SM17 durch die FDA zeigt die effiziente Durchführung des neuen Forschungs- und Entwicklungsprogramms für Arzneimittel des Unternehmens. Es besteht noch immer ein ungedeckter medizinischer Bedarf an zusätzlichen wirksamen Therapien, insbesondere für Patienten, die auf die derzeitigen Behandlungen nicht ansprechen. Wir sind daher von den enormen Aussichten der klinischen Entwicklung von SM17 überzeugt. Unser Kern Produkte, darunter SM03, SN1011 und SM17, macht in der klinischen F&E reibungslose Fortschritte und treibt das Unternehmen stetig in Richtung Kommerzialisierung. In Zukunft werden wir die Umsetzung unserer Projekte beschleunigen, um Patienten Vorteile zu bringen und durch Innovation Wert für Aktionäre zu schaffen."
Über SM17
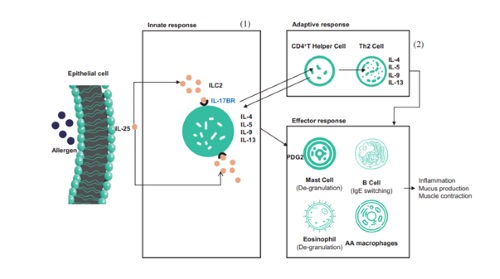
SM17 ist bekanntermaßen der weltweit erste humanisierte, monoklonale IgG4-k-Antikörper für die Entwicklung neuer Medikamente, der auf IL-17RB abzielt. Und IL-17RB ist ein Typ-I-Single-Transmembran-Glykoprotein, das zur IL-17-Rezeptorfamilie gehört. Die Bindung von SM17 an IL-17RB könnte Th2-Immunantworten unterdrücken, die durch eine Kategorie von Zytokinen namens „Alarmin“ induziert werden, von denen gezeigt wurde, dass sie an der Pathogenese von allergischen Erkrankungen und viralen Reaktionen der Atemwege beteiligt sind. Es wird erwartet, dass ein alternativer Ansatz, der auf vorgeschaltete Mediatoren der Th2-Entzündungskaskade wie „Alarmine“ abzielt, eine breitere Wirkung auf Atemwegsentzündungen hat und eine wirksamere Asthmakontrolle bietet als derzeit verfügbare Therapien und Produkte mit ähnlichem Wirkmechanismus wie SM17 von der FDA zugelassen.
Über SinoMab BioScience Limited
SinoMab BioScience Limited (Aktiencode: 3681.HK) widmet sich der Erforschung, Entwicklung, Herstellung und Vermarktung von Therapeutika zur Behandlung immunologischer Erkrankungen. Das Flaggschiffprodukt des Unternehmens, SM03, ist ein potenzieller globaler First-in-Target-mAb gegen CD22 zur Behandlung von rheumatoider Arthritis (RA) und befindet sich derzeit in einer klinischen Phase-III-Studie für rheumatoide Arthritis in China, die als eines der bedeutendsten Spezialprodukte anerkannt wurde Projekte zur Entwicklung bedeutender neuer Arzneimittel in der zwölften Fünfjahresplanperiode und der dreizehnten Fünfjahresplanperiode. Darüber hinaus verfügt das Unternehmen über weitere potenzielle First-in-Target- und First-in-Class-Medikamentenkandidaten, von denen sich einige bereits in der klinischen Phase befinden und deren Indikationen rheumatoide Arthritis (RA), systemischer Lupus erythematodes (SLE) und Pemphigus vulgaris abdecken (PV), Non-Hodgkin-Lymphom (NHL), Asthma und andere Krankheiten mit großem ungedecktem klinischen Bedarf.
Copyright 2022 ACN Newswire. Alle Rechte vorbehalten. www.acnnewswire.comSinoMab BioScience Limited („SinoMab“ oder das „Unternehmen“, zusammen mit seinen Tochtergesellschaften die „Gruppe“, Aktiencode: 3681.HK), ein biopharmazeutisches Unternehmen mit Sitz in Hongkong, das sich der Forschung, Entwicklung und Herstellung widmet und Kommerzialisierung von Therapeutika zur Behandlung immunologischer Erkrankungen
- 11
- 2022
- 7
- beschleunigen
- ACN-Newswire
- Action
- Zusätzliche
- Vorteilen
- Alle
- bereits
- Bekannt geben
- Anwendung
- Ansatz
- verfügbar
- glaubt,
- Vorteile
- Milliarde
- Vorsitzende
- Charity
- Chef
- Chief Executive Officer
- China
- Code
- Vermarktung
- Unternehmen
- zuversichtlich
- Smartgeräte App
- Urheberrecht
- könnte
- Strom
- technische Daten
- gewidmet
- entwickeln
- Entwicklung
- Direktor
- Krankheit
- Krankheiten
- Fahren
- Medikament
- Drogen
- bewirken
- Effektiv
- enorm
- insbesondere
- Exekutive
- Geschäftsführer
- erwartet
- Familie
- FDA
- Vorname
- Folgende
- Nahrung,
- Zukunft
- Global
- High
- HTTPS
- Einschließlich
- Erhöhung
- Innovation
- bekannt
- grosse
- Limitiert
- aus einer regionalen
- Lang
- Dur
- Making
- Herstellung
- Markt
- sowie medizinische
- Million
- Offizier
- Option
- Optionen
- Andere
- Phase
- Produkt
- Produkte
- Programm
- Projekte
- die
- Quartal
- F&E
- Angebot
- Honorar
- Forschungsprojekte
- Sicherheit
- Said
- signifikant
- ähnlich
- Größe
- Stufe
- -bestands-
- Studie
- eingereicht
- Durch
- Zeit
- gemeinsam
- traditionell
- Behandlungen
- Versuch
- uns
- einzigartiges
- Vereinigt
- Großbritannien
- Wert
- WHO