By Kenna Hughes-Castleberry gepostet am 07. Oktober 2022
Viele Gleichungen innerhalb der Quantenphysik können hilfreich sein, um Forscher bei der Untersuchung chemischer Wechselwirkungen anzuleiten. Da sowohl Quantenphysik als auch Chemie Obwohl sie auf den gleichen atomaren Ebenen arbeiten, werden sie häufig gemeinsam eingesetzt, um neue Ergebnisse zu erzielen. Kürzlich haben Forscher am Los Alamos Nationales Laboratorium (LANL) hat diese Paarung durch Hinzufügen noch einen Schritt weitergeführt Maschinelles Lernen Prozesse zur Vorhersage biochemischer Wechselwirkungen in molekularen Simulationen. Dies wiederum könnte dazu beitragen, Schritte bei der Arzneimittelentwicklung und anderen Branchenszenarien zu beschleunigen und Arzneimittel langfristig sicherer und schneller zu machen.
Verwendung von maschinellem Lernen für Datensätze
Es gibt bereits maschinelle Lernverfahren angewandt zum Quantencomputing und zur Quantenphysik. Da maschinelles Lernen Muster aus großen Datenmengen vorhersagt und erstellt, ist es für Bereiche wie die Quantenphysik oder die Chemie von Vorteil, in denen es viele bewegliche Teile gibt. Laut LANL-Forscher Benjamin Nebgen: „Vor dem Aufkommen von Methoden des maschinellen Lernens (ML) in den Bereichen Chemie und Materialwissenschaften war die größte praktische Simulation von Chemie und Materialsystemen auf ein paar tausend Atome begrenzt.“ Dies ist viel zu klein, um viele Effekte genau zu erfassen, die chemische oder materielle Eigenschaften wie Kornpfade oder seltene Reaktionspfade bestimmen.“ Dank der Vorteile des maschinellen Lernens können Forscher kompliziertere Szenarien in Simulationen untersuchen, darunter auch solche mit Schwerpunkt auf Quantenphysik und Chemie.
Für Wissenschaftler, die Neues entwerfen Drogen Bei der Untersuchung chemischer Reaktionen ist es wichtig, vollständig zu verstehen, was mit den Elektronen auf Quantenebene geschieht. „Die Bewegung von Elektronen und Atomkernen steuert nahezu alle chemischen und materiellen Eigenschaften, die unsere moderne Existenz bestimmen“, sagte Nebgen. „Dazu gehört die Chemie von allem, von den Medikamenten, die wir einnehmen, den Haushaltsreinigern, die wir täglich verwenden, bis hin zu den Kraftstoffen in unseren eigenen Autos und Lastwagen. Darüber hinaus werden die Eigenschaften der Materialien, aus denen unsere Autos, Häuser, Werkzeuge, Flugzeuge und fast alles, mit dem wir täglich interagieren, bestehen, von derselben zugrunde liegenden Physik gesteuert.“ Dies ermöglicht es Forschern, die Wechselwirkungen eines Moleküls auf grundlegender Ebene tiefer zu untersuchen. Sobald dieses Niveau jedoch erreicht ist, kommt es zu komplizierteren Berechnungen. „Die auf einzelne Atome wirkenden Kräfte, die in Newtons Gleichungen eingehen, stammen aus der Bewegung von Elektronen, die von Natur aus Quantennatur sind“, erklärte Nebgen. „Daher müssen die Elektronen mit der Schrödinger-Gleichung behandelt werden, was ein viel schwieriger zu lösendes mathematisches Problem darstellt.“
LANL nutzt maschinelles Lernen, um Modelle zu erstellen
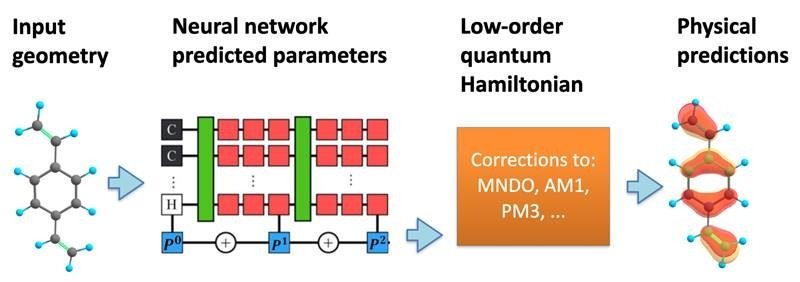
Um diese schwierigen Gleichungen zu lösen, nutzen Forscher wie Nebgen Werkzeuge des maschinellen Lernens. Diese Werkzeuge können eine chemische Simulation beschleunigen, indem sie sich nur auf einige der wichtigsten Elektronen im System konzentrieren, fügte Nebgen hinzu. Mithilfe eines maschinellen Lerntools namens neuronales Netzwerk konnten Nebgen und sein Team eine erstellen Vorhersagemodell der möglichen Elektronenzustände und der damit verbundenen Energien innerhalb eines Moleküls. Von dort aus konnte das Team einige der möglichen Ergebnisse der Simulation anhand unterschiedlicher Eingaben genau vorhersagen. Für Biotech-Unternehmen, die Millionen von Dollar für die Entwicklung und Erprobung neuer Medikamente ausgeben, könnten Vorhersagemodelle wie dieses viele kosteneffektive Vorteile bringen. Der Einsatz von maschinellem Lernen in der Arzneimittelindustrie ist zwar nichts Neues, doch die Kombination mit der Leistungsfähigkeit des Quantencomputings könnte die nächste Technologiegeneration hervorbringen, die für die Einführung zukünftiger Arzneimittel erforderlich ist.
Kenna Hughes-Castleberry ist Mitarbeiterin bei Inside Quantum Technology und Science Communicator bei JILA (eine Partnerschaft zwischen der University of Colorado Boulder und NIST). Ihre Beats beim Schreiben umfassen Deep Tech, Metaverse und Quantentechnologie.