Die Protonentherapie kann hochgradig konforme Dosisverteilungen an ein Tumorziel liefern, während die Dosis für Gewebe außerhalb des Zielvolumens minimiert wird. Die Erstellung von Behandlungsplänen, die diese Stärke realisieren, hat für Dosimetristen und Medizinphysiker höchste Priorität.
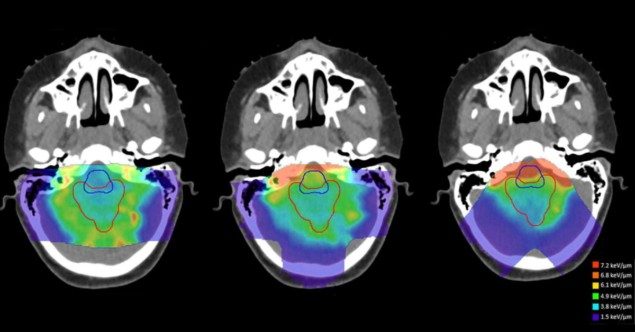
Protonen deponieren eine Dosis auf eine grundlegend andere Weise als Röntgenstrahlen, eine andere Art der Strahlentherapie mit externem Strahl. Wenn ein Proton das Ende seiner Bahn erreicht, steigt die Geschwindigkeit, mit der seine Energie auf das Gewebe übertragen wird – sein linearer Energietransfer (LET), ausgedrückt in keV/µm – an.
Die relative biologische Wirksamkeit (RBE) erfasst die biologischen Auswirkungen einer Erhöhung des LET, und für klinische Protonenbehandlungen wird häufig ein fester RBE-Wert von 1.1 verwendet. Die Protonen-RBE ist jedoch von vielen anderen Faktoren abhängig, darunter klinische Endpunkte, Gewebetyp, Fraktionierungsschema, patientenspezifische Strahlenempfindlichkeit, physikalische Dosis und Unsicherheiten bei experimentellen Messungen. Infolgedessen wird bei der Verwendung eines festen RBE-Werts in der Protonentherapie die RBE an Orten mit hohem LET wahrscheinlich unterschätzt, was zu einem erhöhten Risiko strahleninduzierter Toxizitäten führen könnte.
Dennoch korreliert LET stark mit RBE und ist ein Schlüsselfaktor für die Bestimmung der variablen RBE in der Protonentherapie. Daher untersuchen Forscher Ansätze zur Berechnung und Bewertung von LET während der Behandlungsplanung. Diese biologischen Behandlungsplanungsinstrumente sind jedoch begrenzt, und bis sie entwickelt und weiter untersucht werden, müssen Kliniken ihre eigenen Behandlungsplanungspraktiken identifizieren, um LET außerhalb des Zielvolumens zu minimieren, sagt er Austin kämpfte, Medizinphysiker bei St. Jude Children's Research Hospital in Tennessee.
„Die Beeinflussung der [LET-Verteilung] ist ein aktives Forschungsgebiet, und es werden einige großartige Methoden entwickelt“, erklärt Faught. „Das Problem, mit dem wir konfrontiert sind, ist, dass diese ohne kundenspezifische Software, die intern entwickelt wurde, oder durch spezielle Forschungsversionen von von Anbietern bereitgestellten Anwendungen nicht ohne weiteres verfügbar sind … [und es gibt] wenige Studien, die quantitative Leitlinien dazu liefern, was wir anstreben sollten.“
Behandlungsplanungsstrategien
Als Schritt in Richtung einer LET-basierten Planbewertung und -optimierung für die Photonentherapie führten Faught und sein Team eine Untersuchung von Planungsstrategien durch, die klinischen Teams für die intensitätsmodulierte Protonentherapie (IMPT) kommerziell erhältlich sind. Ihre Studie, berichtet in der Zeitschrift für angewandte klinische medizinische Physik, führt einige Leitlinien für Behandlungsplaner der Protonentherapie ein. „Wir wollten uns einige leicht verfügbare Techniken zur Behandlungsplanung ansehen und wie sie den LET beeinflussen können“, erklärt Faught.
Die Forscher bewerteten die Unterschiede im dosisgewichteten LET (LETd) zwischen acht zukunftsorientierten Behandlungsplanungsansätzen, die auf ein zylindrisches Wasserphantom angewendet werden, und vier pädiatrischen Hirntumorfällen (Faught stellt fest, dass strahleninduzierte Toxizitäten ein Schwerpunktbereich für das Team sind). Sie verglichen diese Planungsstrategien mit einem Plan, der entgegengesetzte seitliche Strahlen (für das Phantom) verwendete, oder mit dem ursprünglichen klinischen Plan (für Patienten), wobei sie sekundäre Monte-Carlo-Berechnungen verwendeten, um sowohl die Dosis als auch den LET zu bewertend.
Die Forscher fanden heraus, dass die Geometrie des Behandlungsfeldes den größten Beitrag zur Lokalisierung von Bereichen mit hohem LET leistete. Um die potenziellen Auswirkungen biologischer Unsicherheiten im Zusammenhang mit einem hohen LET zu minderndschlagen sie vor, dass Behandlungsplaner große Schnittwinkel zwischen Behandlungsstrahlen verwenden und Strahlen vermeiden, die unmittelbar proximal von kritischen Strukturen stoppen.
„Das sind großartige Neuigkeiten, da es bedeutet, dass eine sorgfältige Auswahl der Anzahl der Behandlungsfelder und ihre Ausrichtung in Bezug auf nahe gelegene Gesundheitsgewebe effektiv sein können“, sagt Faught. „Mit einigen bewussten, vorausschauenden Überlegungen können dies alle Behandlungsplaner während des Planungsprozesses berücksichtigen.“
Die Forscher fanden auch heraus, dass die Verwendung eines Range Shifters den mittleren LET signifikant reduzierted im klinischen Zielvolumen. Aus diesem Grund empfehlen sie, Range Shifter und alternative Strategien der Spotplatzierungsbeschränkungen sparsam einzusetzen und nur dann, wenn Kliniken den resultierenden LET berechnen könnend gegen alternative Planungsstrategien zu evaluieren.
Aufgrund der geringen Stichprobengröße der Studie konnten die Forscher keinen klaren Trend bei LET feststellend Variationen in den klinischen Fällen. Sie bewerteten nicht die Beziehung zwischen Änderungen des LET und einer Änderung der Wahrscheinlichkeit einer Tumorkontrolle oder von normalen Gewebekomplikationen.
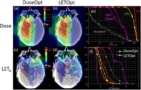
LET-basierte Pläne optimieren die Protonentherapie
Während die Auswirkungen jedes Planungsansatzes auf Regionen mit hohem LET bescheiden waren, ist es laut Faught wichtig zu erkennen, dass die Behandlungsplanungsstrategien und -empfehlungen des Teams evidenzbasiert sind und leicht in die klinische Praxis umgesetzt werden können.
„Ich hoffe, dass einer der Erkenntnisse darin besteht, dass wir als Fachgebiet von kommerziellen Tools profitieren würden, die die Berechnung von LET innerhalb des Behandlungsplanungssystems ermöglichen. Noch besser, wir würden gerne Möglichkeiten zur Optimierung mit LET im Hinterkopf haben. Diese Studie war eine gute Brücke, bis diese Tools breiter verfügbar sind“, sagt Faught.