Η εν τω βάθει εγκεφαλική διέγερση (DBS), στην οποία τα ηλεκτρόδια που εμφυτεύονται στον εγκέφαλο παρέχουν ηλεκτρικά ερεθίσματα σε συγκεκριμένους στόχους, είναι μια αποτελεσματική κλινική θεραπεία για πολλές νευρολογικές παθήσεις. Το DBS χρησιμοποιείται επί του παρόντος για τη θεραπεία κινητικών διαταραχών όπως η νόσος του Πάρκινσον, ο ιδιοπαθής τρόμος και η δυστονία, καθώς και καταστάσεις όπως η επιληψία και η ιδεοψυχαναγκαστική διαταραχή. Η θεραπεία, ωστόσο, απαιτεί χειρουργική επέμβαση στον εγκέφαλο για την εισαγωγή των ηλεκτροδίων διέγερσης, με τη δυνατότητα να προκαλέσει πολλές παρενέργειες.
Για να άρουν την ανάγκη για επεμβατική χειρουργική, ερευνητές από το Πανεπιστήμιο Επιστήμης και Τεχνολογίας Pohang (POSTECH) στην Κορέα αναπτύσσουν μια μη επεμβατική στρατηγική νευρωνικής διέγερσης που βασίζεται σε πιεζοηλεκτρικά νανοσωματίδια. Τα νανοσωματίδια εξυπηρετούν δύο λειτουργίες – παροδικό άνοιγμα του αιματοεγκεφαλικού φραγμού (BBB) και διέγερση της απελευθέρωσης ντοπαμίνης – και οι δύο ελέγχονται από εξωτερικά εστιασμένο υπερήχο.
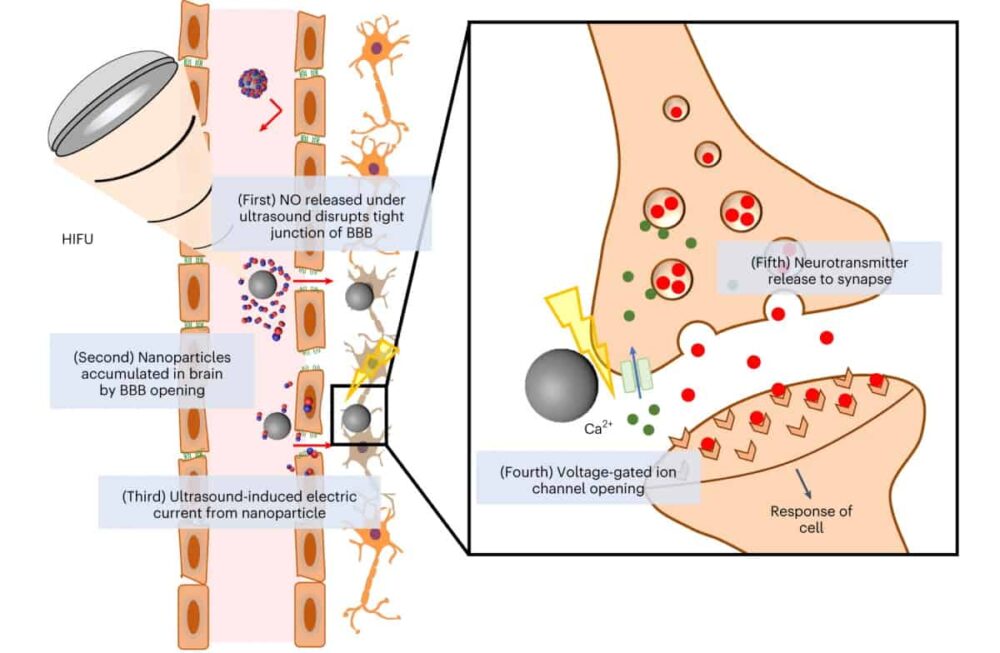
Τα πιεζοηλεκτρικά νανοσωματίδια παρουσιάζουν ενδιαφέρον ως νευρωνικοί διεγέρτες επειδή ως απόκριση σε εξωτερικά ερεθίσματα – όπως ο υπέρηχος, για παράδειγμα – παραμορφώνονται και παράγουν συνεχές ρεύμα. Οι ερευνητές προτείνουν ότι αυτό το ρεύμα θα μπορούσε στη συνέχεια να χρησιμοποιηθεί για την τόνωση των ντοπαμινεργικών νευρώνων για την απελευθέρωση νευροδιαβιβαστών.
Μια βασική πρόκληση είναι η παράδοση των νανοσωματιδίων στον εγκέφαλο, συγκεκριμένα, ο τρόπος με τον οποίο θα μεταφερθούν στο BBB. Για να το επιτύχουν αυτό, οι ερευνητές στράφηκαν στο μονοξείδιο του αζώτου (NO), ένα εξαιρετικά αντιδραστικό μόριο που δείχνει πιθανότητες διακοπής του BBB. Σχεδίασαν ένα πολυλειτουργικό σύστημα, που περιγράφεται στο Φύση Βιοϊατρική μηχανική, που περιλαμβάνει ένα νανοσωματίδιο τιτανικού βαρίου επικαλυμμένο με BNN6 που απελευθερώνει ΝΟ και πολυντοπαμίνη (pDA). Σε απόκριση στον υπέρηχο, αυτά τα νανοσωματίδια θα πρέπει να παράγουν τόσο ΝΟ όσο και συνεχές ρεύμα.
Για να δοκιμάσετε την προσέγγισή τους, κύριος συγγραφέας Γουόν Γιονγκ Κιμ και οι συνάδελφοι ερεύνησαν αρχικά την ικανότητα των νανοσωματιδίων να απελευθερώνουν NO. Σε απόκριση σε 5 δευτερόλεπτα εστιασμένου υπερήχου υψηλής έντασης (HIFU), τα νανοσωματίδια απελευθέρωσαν στιγμιαία ΝΟ. Αξιολόγησαν επίσης την πιεζοηλεκτρική συμπεριφορά χρησιμοποιώντας μια διάταξη μπαλώματος-σφιγκτήρα. Ενώ ο διαλύτης χωρίς νανοσωματίδια επικαλυμμένα με pDA δεν εμφάνισε αιχμές ρεύματος, παρουσία των νανοσωματιδίων, παρατηρήθηκαν διακριτές αιχμές ρεύματος με εντάσεις ανάλογες με την ένταση του υπερήχου.
Το DBS υποτίθεται ότι διεγείρει ηλεκτρικά το νευρικό σύστημα ανοίγοντας το Ca2+ κανάλια των κοντινών νευρώνων και στη συνέχεια επιταχυνόμενη απελευθέρωση νευροδιαβιβαστών στη σύναψη. Για να διερευνήσει εάν το ρεύμα που δημιουργείται από νανοσωματίδια θα μπορούσε να προσφέρει παρόμοια νευρική διέγερση, η ομάδα παρακολούθησε το Ca2+ δυναμική κυττάρων που μοιάζουν με νευρώνες. Ενδοκυτταρικό Ca2+ Η συγκέντρωση αυξήθηκε σημαντικά στα κύτταρα που έλαβαν τόσο νανοσωματίδια όσο και υπερήχους, ενώ είτε ο υπέρηχος είτε τα νανοσωματίδια από μόνα τους δεν είχαν κανένα αποτέλεσμα.
Τα κύτταρα που υποβλήθηκαν σε επεξεργασία με νανοσωματίδια διεγερμένα από υπερήχους δημιούργησαν επίσης αυξημένη εξωκυτταρική συγκέντρωση ντοπαμίνης, υποδεικνύοντας Ca2+ μεσολαβούμενη από εισροή απελευθέρωση νευροδιαβιβαστών. Και πάλι, καμία σημαντική αλλαγή δεν παρατηρήθηκε μόνο με υπερήχους ή νανοσωματίδια. Δοκιμές με χρήση μη πιεζοηλεκτρικών νανοσωματιδίων έδειξαν ασήμαντες αλλαγές στο Ca2+ εισροή και απελευθέρωση νευροδιαβιβαστών, υποδεικνύοντας ότι αυτές οι επιδράσεις προκύπτουν κυρίως ως απόκριση στην πιεζοηλεκτρική διέγερση.
Στη συνέχεια οι ερευνητές πραγματοποίησαν μια σειρά από ίη νίνο σπουδές. Για να διερευνήσουν το άνοιγμα BBB με τη μεσολάβηση ΝΟ, έκαναν ενδοφλέβια ένεση σε ποντίκια με πιεζοηλεκτρικά νανοσωματίδια που απελευθερώνουν ΝΟ και στη συνέχεια εφάρμοσαν HIFU σε στοχευμένες θέσεις του εγκεφάλου υπό την καθοδήγηση υπερήχων.
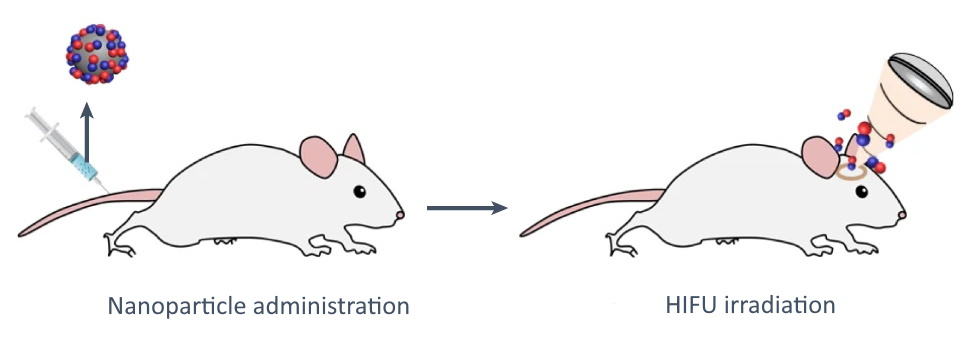
Δύο ώρες μετά την έγχυση, η ηλεκτρονική μικροσκοπία μετάδοσης αποκάλυψε σημαντικά υψηλότερες ποσότητες νανοσωματιδίων που συσσωρεύτηκαν μέσα στον εγκέφαλο των ζώων σε σύγκριση με τις ομάδες ελέγχου, αποδεικνύοντας ότι η απελευθέρωση ΝΟ διέκοψε προσωρινά τις στενές συνδέσεις στο BBB. Οι ερευνητές έδειξαν επίσης ότι 2 ώρες μετά την εφαρμογή HIFU, το BBB δεν ήταν πλέον διαπερατό, επιβεβαιώνοντας ότι η διαταραχή BBB που προκαλείται από ΝΟ είναι μόνο προσωρινή.
Τέλος, η ομάδα αξιολόγησε τα θεραπευτικά αποτελέσματα των νανοσωματιδίων χρησιμοποιώντας ένα μοντέλο ποντικού της νόσου του Πάρκινσον. Τα ποντίκια εγχύθηκαν με νανοσωματίδια ακολουθούμενα από πολλαπλές εφαρμογές HIFU στον υποθαλαμικό πυρήνα (την εγκεκριμένη από την Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ θέση στόχευσης DBS) για την αποκατάσταση των επιπέδων ντοπαμίνης στον εγκέφαλο.
Το DBS χρησιμοποιώντας τα νανοσωματίδια που οδηγούνται από υπερήχους ενίσχυσε τις συμπεριφορικές λειτουργίες των ζώων, συμπεριλαμβανομένου του κινητικού συντονισμού και της κινητικής δραστηριότητας. Τα ποντίκια εμφάνισαν σταδιακή βελτίωση στην κινητική λειτουργία με καθημερινή διέγερση HIFU για 10 ημέρες, με την κινητική δραστηριότητα σχεδόν αποκατασταθεί την ημέρα 16. Η ομάδα εικάζει ότι τα πιεζοηλεκτρικά νανοσωματίδια προκάλεσαν απελευθέρωση νευροδιαβιβαστών, η οποία ανακούφισε σημαντικά τα συμπτώματα της νόσου του Πάρκινσον χωρίς να προκαλέσει σημαντική τοξικότητα .

Η εξατομικευμένη διέγερση του εγκεφάλου θα μπορούσε να θεραπεύσει την μη θεραπεύσιμη κατάθλιψη
«Ελπίζουμε ότι τα πιεζοηλεκτρικά νανοσωματίδια που ανταποκρίνονται στον υπέρηχο που απελευθερώνουν ΝΟ μπορούν να αναπτυχθούν περαιτέρω σε ελάχιστα επεμβατικές θεραπευτικές προσεγγίσεις για τη θεραπεία νευροεκφυλιστικών ασθενειών», καταλήγουν.
Ο όμιλος χρησιμοποιεί τώρα θεμελιώδεις μελέτες για να προσδιορίσει τους υποκείμενους μηχανισμούς για το άνοιγμα BBB με τη μεσολάβηση NO. «Αναπτύσσουμε επίσης υλικά νέας γενιάς που ρυθμίζουν το ΝΟ για να μεγιστοποιήσουμε την κλινική τους χρήση, ελαχιστοποιώντας ταυτόχρονα τις ανεπιθύμητες παρενέργειές τους», εξηγεί ο πρώτος συγγραφέας. Taejeong Kim.