La mielina es una capa protectora que se forma alrededor de los nervios para aislarlos y acelerar la transmisión de los impulsos eléctricos. La desmielinización, la pérdida de esta capa aislante, contribuye a muchas enfermedades neurológicas, como la esclerosis múltiple, la enfermedad de Alzheimer, los accidentes cerebrovasculares y la demencia. Una técnica eficaz para detectar esta condición potencialmente reversible podría mejorar los diagnósticos de enfermedades cerebrales y permitir el seguimiento de posibles tratamientos. Actualmente, sin embargo, ninguna prueba de imagen puede identificar con precisión la desmielinización.
Para abordar este déficit, los investigadores de la Centro Gordon de Imágenes Médicas en el Hospital General de Massachusetts y la Facultad de Medicina de Harvard están investigando el uso de un nuevo radiotrazador PET: 18F-3-fluoro-4-aminopiridina (18F-3F4AP) – para obtener imágenes de lesiones desmielinizadas en el cerebro. Ahora han probado el marcador en humanos por primera vez, informando sus hallazgos en el Revista Europea de Medicina Nuclear e Imagen Molecular.
"Tener una herramienta de imagen que sea específica para la desmielinización puede ayudar a comprender mejor la contribución de la desmielinización a diferentes enfermedades y monitorear mejor una enfermedad o la respuesta a la terapia, por ejemplo, una terapia remielinizante", dice el primer autor. Pedro Brugarolas En un comunicado de prensa.
18F-3F4AP es una versión radiofluorada del fármaco 4-aminopiridina para la esclerosis múltiple. El marcador, que ingresa al cerebro a través de la difusión pasiva, se une a los axones desmielinizados de manera similar a la droga misma. Estudios previos demostraron que la PET con 18F-3F4AP puede detectar lesiones en un modelo de desmielinización en ratas, y que el marcador tiene propiedades adecuadas para obtener imágenes de los cerebros de los macacos rhesus, lo que llevó al equipo a investigar su uso en humanos.
Brugarolas y sus colegas realizaron exploraciones PET en cuatro voluntarios sanos después de administrar 368±17.9 MBq de 18F-3F4AP. Después de una tomografía computarizada de baja dosis, comenzaron la PET inmediatamente después de la inyección del marcador, registrando una serie de imágenes en siete posiciones de la cama del escáner para cubrir todo el cuerpo. Para capturar la cinética del trazador y maximizar la calidad de la imagen, el tiempo de escaneo inicial por posición fue de 1 min, aumentando a 2, 4 y 8 min por posición. Toda la adquisición de PET tomó 4 h.
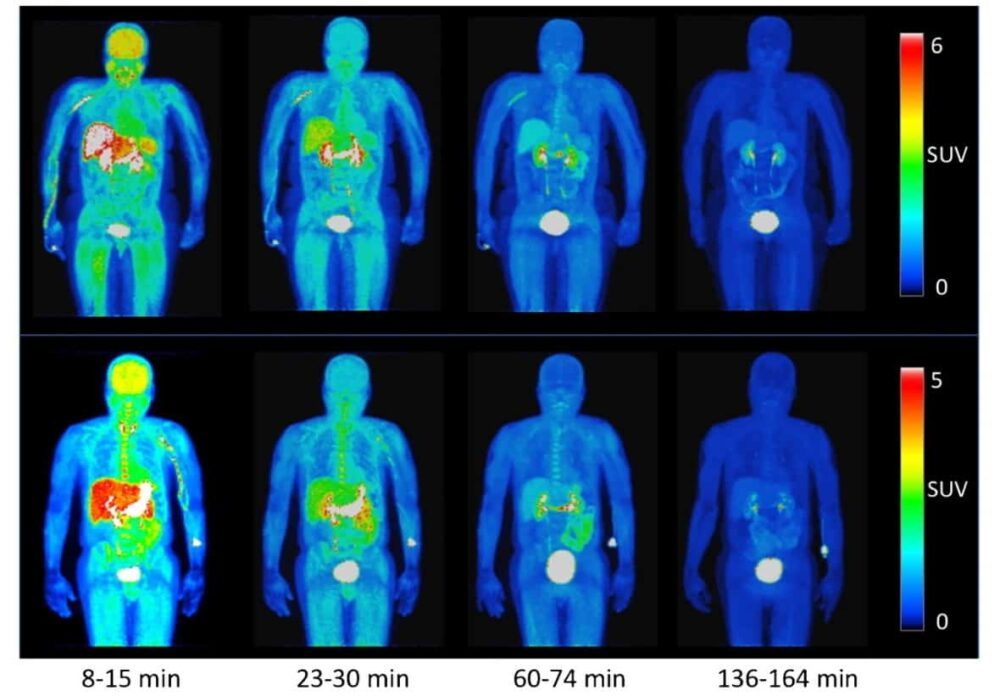
Las imágenes PET resultantes y las curvas de tiempo-actividad (TAC) revelaron que el marcador se distribuyó rápidamente por todo el cuerpo, incluido el cerebro, y se eliminó rápidamente a través de la excreción renal. A los 8-14 minutos después de la inyección, se observó la máxima actividad en el hígado, los riñones, la vejiga urinaria, el bazo, el estómago y el cerebro. A los 22-28 min, la mayor actividad se registró en los riñones, las vías biliares y la vejiga urinaria. Después de 60 minutos, la mayor parte de la actividad se había eliminado de los órganos y se había acumulado en la vejiga urinaria.
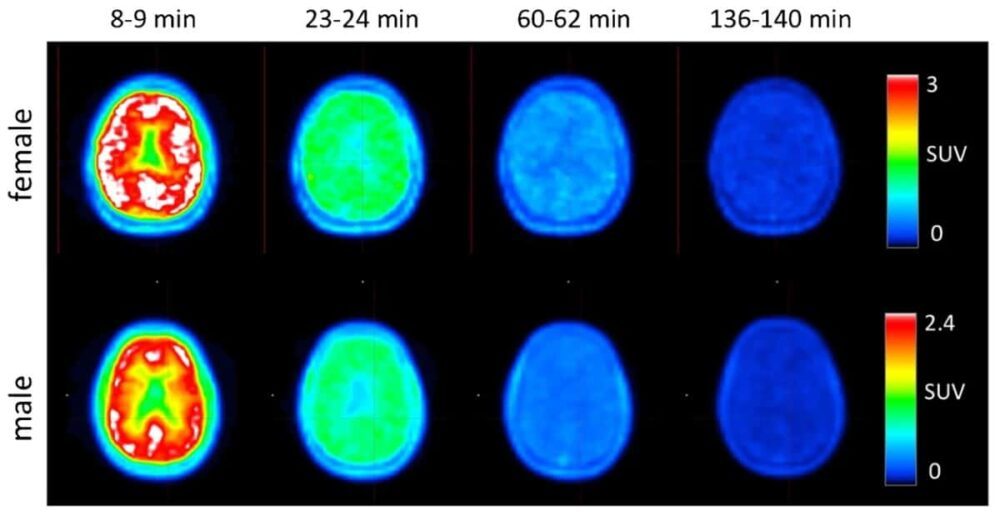
El equipo también utilizó los TAC integrados para realizar la dosimetría. La dosis efectiva promedio fue de 12.2 ± 2.2 µSv/MBq para los cuatro participantes, sin que se observaran diferencias entre los voluntarios masculinos y femeninos. Los investigadores señalan que esta dosis efectiva es significativamente más baja que la estimada a partir de estudios con primates no humanos (21.6 ± 0.6 µSv/MBq), probablemente debido a la eliminación más rápida observada en humanos que en macacos rhesus. Esta dosis también fue más baja que la de otros trazadores PET, como 18F-FDG.
Es importante destacar que todos los participantes toleraron bien el trazador y el procedimiento de obtención de imágenes, sin que se produjeran efectos adversos durante la exploración. No hubo diferencias significativas en los signos vitales de los voluntarios (temperatura, presión arterial y saturación de oxígeno) antes y después de la exploración, y no hubo cambios significativos en los metabolitos sanguíneos y los resultados del electrocardiograma obtenidos dentro de los 30 días anteriores y posteriores a la exploración.

El marcador PET mide la desmielinización en ratones
Los investigadores concluyen que 18F-3F4AP ingresa fácilmente al cerebro y es seguro para su uso en humanos, con un nivel aceptable de dosis de radiación. Sugieren que sus hallazgos abren la puerta a más estudios que investiguen la capacidad del marcador para detectar lesiones desmielinizadas en diferentes poblaciones de pacientes.
Brugarolas cuenta Mundo de la física que el equipo está realizando actualmente dos pequeños estudios clínicos utilizando el nuevo marcador: para investigar su valor para imagen de la esclerosis multiple; y evaluar su uso en pacientes con lesión cerebral traumática, deterioro cognitivo leve y enfermedad de Alzheimer.