La radioterapia es uno de los tratamientos contra el cáncer más comunes, que prolonga eficazmente los tiempos de supervivencia y aumenta las tasas de curación de los pacientes con cáncer. Sin embargo, el daño óseo inducido por la radioterapia (incluida la reducción de la masa ósea, el aumento de la fragilidad ósea y un mayor riesgo de fracturas y osteonecrosis) sigue siendo un problema común que actualmente carece de contramedidas efectivas.
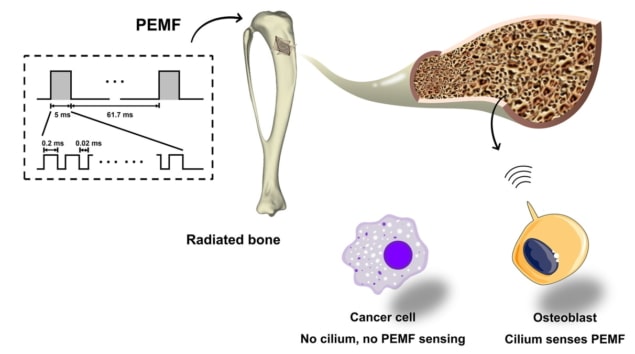
La radiación causa este daño al suprimir el crecimiento, la supervivencia y la maduración de las células formadoras de hueso llamadas osteoblastos, inhibiendo así la formación de hueso. Un posible remedio podría ser la exposición a campos electromagnéticos (EMF) no invasivos, que se sabe que estimulan el crecimiento y la diferenciación de los osteoblastos y podrían mitigar los efectos de la irradiación. Ahora, un equipo de investigación en China ha identificado la forma de onda óptima de los CEM para maximizar la eficacia de dicho tratamiento, informando los hallazgos en Science Advances.
Da Jing, de Cuarta Universidad Médica Military sus colegas sometieron por primera vez células óseas a estimulación EMF usando varias formas de onda, incluyendo EMF sinusoidal, EMF de pulsación única y EMF de ráfaga pulsada (PEMF). Para evaluar la respuesta de las células, monitorearon el ion de calcio intracelular en tiempo real (Ca2+) señalización, una de las primeras respuestas celulares a estímulos externos.
El equipo descubrió que PEMF inducía Ca intracelular más robusto2+ señalización en osteoblastos irradiados que las otras formas de onda, caracterizadas por Ca único2+ oscilaciones con múltiples Ca2+ Picos. Análisis adicionales mostraron que una forma de onda PEMF no identificada previamente con una intensidad de campo magnético de 2 mT y una frecuencia de 15 Hz provocó la respuesta más fuerte en los osteoblastos. Por el contrario, esta forma de onda PEMF no tuvo efecto sobre otros tipos de células óseas irradiadas (osteoclastos y osteocitos).
A continuación, los investigadores investigaron si el PEMF administrado utilizando estos parámetros óptimos podría mitigar la pérdida ósea inducida por la radiación. in vivo. En estudios con ratas, expusieron una extremidad trasera a dos dosis de 8 Gy de radiación focal (con un día de diferencia) y utilizaron micro-CT para evaluar la estructura ósea 45 días después. Las extremidades irradiadas exhibieron una pérdida ósea trabecular significativa, incluida una disminución de aproximadamente el 50 % en la fracción de volumen óseo y la densidad mineral ósea en comparación con el lado no irradiado.
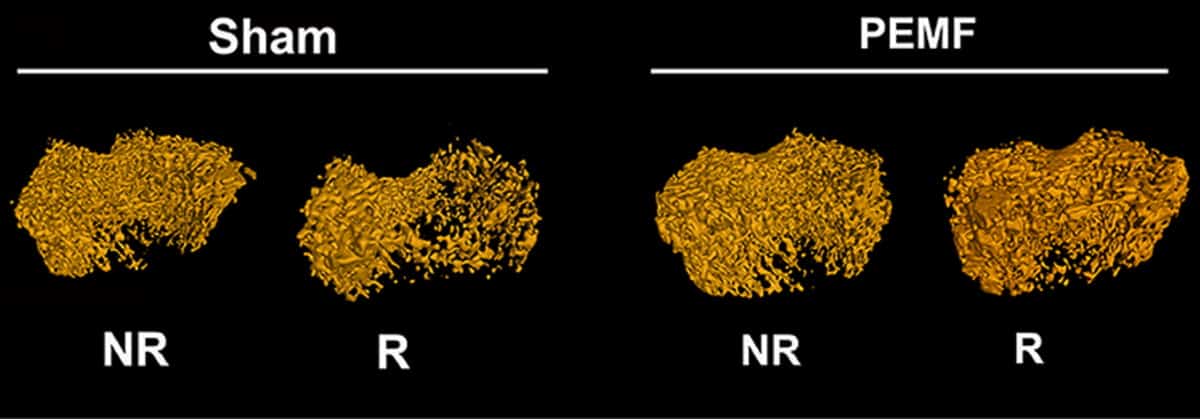
Un segundo grupo de ratas recibió PEMF de cuerpo entero diariamente (2 horas/día) durante los 45 días posteriores a la irradiación. Este tratamiento restauró la masa ósea y las propiedades mecánicas de las extremidades posteriores irradiadas al nivel de las extremidades no irradiadas, mediante el rescate de los osteoblastos. El equipo señala que PEMF no tuvo ningún efecto sobre el peso corporal de los animales ni sobre la ingesta de alimentos.
Habiendo demostrado que la exposición al PEMF podría mitigar la pérdida ósea inducida por la radiación, también es esencial que el PEMF no afecte negativamente al tratamiento del tumor. Teniendo esto en cuenta, los investigadores compararon la sensibilidad de los osteoblastos y de diversas células tumorales (cáncer de mama, cáncer de colon, melanoma maligno y células de osteosarcoma) al PEMF.
La irradiación redujo la viabilidad celular y promovió la apoptosis en todos los tipos de células. Fundamentalmente, aunque PEMF mejoró la viabilidad de los osteoblastos e inhibió la apoptosis de los osteoblastos, no tuvo ningún efecto sobre la viabilidad o la apoptosis en ninguna de las células tumorales en ningún momento.
La biotinta viva podría mejorar la reparación y regeneración ósea
Los investigadores atribuyen esta selectividad a la presencia de cilios primarios (orgánulos sensoriales que detectan y traducen señales mecánicas extracelulares) que actúan como sensores PEMF. Estos cilios primarios son muy abundantes en los osteoblastos, pero están ausentes en la mayoría de las células tumorales. En un experimento en el que se bloqueó la generación de cilios primarios en osteoblastos irradiados, el aumento mediado por PEMF en la supervivencia y diferenciación de los osteoblastos desapareció casi por completo.
"Teniendo en cuenta que, entre todos los tipos de células óseas, los osteoblastos son especialmente sensibles a la radiación, este régimen PEMF, que induce la activación específica de los osteoblastos, parece ser un enfoque prometedor y muy eficaz contra el daño óseo inducido por la radiación", concluyen los investigadores.