Küberrünnakud haiglatele võivad avaldada laastavat mõju, eriti radioloogia- ja kiiritusravi osakondadele, mille toimimine sõltub eriti tehnoloogiast. Hea näide on üleriigiline küberrünnak Iirimaa avalike tervishoiuteenuste vastu 2021. aasta mais, mis katkestas mõne vähihaige plaanilise kiiritusravi kuni 12 päevaks.
Pärast seda juhtumit meditsiinifüüsikud kl Galway ülikooli haigla ja Iirimaa riiklik ülikool Galway hakkas välja töötama ettevõttesisest tööriista, mis aitab luua kiiritusravi raviplaane pärast katkestuste tekkimist. Tööriist – nimega EQD2VH – arvutab välja ravikompensatsiooni plaanid ja võimaldab visuaalselt võrrelda kõiki plaanivõimalusi, samuti iga patsiendi plaani struktuuri individuaalset analüüsi. Teadlased kirjeldavad uut tarkvaratööriista dokumendis Journal of Applied Clinical Medical Physics.
Kiiritusravi antakse kõige sagedamini mitme nädala jooksul väikeste kiirgusdooside seeriana (tavaliselt 2 Gy), mida nimetatakse fraktsioonideks. Planeerimata ravilüngad – kas küberrünnakute, masinarikke või patsiendi haigestumise tõttu – võivad põhjustada olulisi tagasilööke. Selliste tühimike ajal asustuvad vähirakud kiiresti kasvajakoesse, mille tulemuseks on radiobioloogilise doosi vähenemine planeeritava sihtmahuni (PTV).

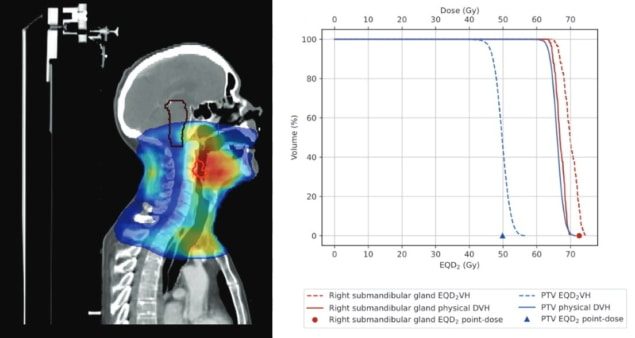
Selle probleemi lahendamiseks EQD2VH kasutab ravilünga arvutuste tegemiseks doosi-mahu histogrammi (DVH) teavet, mis on saadud esialgsetest patsientide plaanidest. Juhtautor Katie O'Shea Iirimaa Galway riiklikust ülikoolist ja tema kolleegid selgitavad, et tarkvara teisendab igas doosikastis oleva füüsilise annuse (DVH andmepunktide vaheline doosivahemik) bioloogiliselt efektiivseks annuseks (BED). See põhjustab nii PTV taasasustamise mõju kui ka parandamata normaalsete kudede subletaalse kahjustuse mõju riskiorganites (OAR-id).
Pärast BED-i teisenduse muutmist, et võtta arvesse annuse variatsioone igas struktuuris, kasutades muutuva doosiga meetodit, teisendab tööriist iga struktuuri BED-i ekvivalentdoosiks 2 Gy fraktsioonides (EQD).2). See normaliseerib iga ravi tavapärase fraktsioneerimisega ja võimaldab erinevate fraktsioneerimisskeemidega plaane kokku võtta. Saadud EQD2 -põhine DVH annab 2D esituse ravilõhe kompenseerimise strateegiate mõjust nii PTV kui ka OAR doosi jaotusele, võrreldes ettenähtud raviplaaniga.
EQD hindamiseks2VH kliinilise otsustusvahendina valisid teadlased välja viis kiirelt kasvavate kasvajatega kõrge prioriteediga patsienti, kelle ravilüngad ei tohiks ületada kahte päeva. See hõlmas nelja pea- ja kaelapiirkonna vähiga patsienti, kes said intensiivsusega moduleeritud kiiritusravi, ja ühte kopsuvähiga patsienti, kes said 3D-konformset kiiritusravi ja kelle ravivahe oli 12 või 13 päeva. Need juhtumid võimaldasid meeskonnal hinnata EQD kasutamist2VH patsientidele, kellel on nii tavapärane (2 Gy) kui ka mittekonventsionaalne (2.2 Gy) fraktsioneerimine ja erinevad ravivaheajad (46-XNUMX päeva ravi alguses).
Iga patsiendi muudetud raviplaanid põhinesid nende algsetel plaanidel, muutes kas fraktsiooni annust või fraktsioonide arvu. O'Shea selgitab, et iga patsiendi muudetud plaanis ja ajakavas kasutati rakkude taasasustamise mõju vähendamiseks kaks korda päevas toimuvat fraktsioneerimist, nädalavahetuse ravi ja sihtmahu suurendatud annust.
Kavad piirasid ravi kuue fraktsiooniga nädalas ja välistasid kaks korda päevas fraktsioneerimise järjestikustel päevadel. Kui ettenähtud ravi ei suudetud vajaliku aja jooksul lõpule viia, uurisid teadlased hüpofraktsiooni (suurendatud annuse manustamine fraktsiooni kohta) plaane. Nad suutsid visuaalselt ja kvantitatiivselt võrrelda erinevaid muudetud plaane patsiendi algse plaaniga, et teha kindlaks, milline annaks PTV-le parima annuse ja OAR-idele väikseima annuse.
Teadlased märgivad, et iga üksiku struktuuri 2D-esitus EQD-s2VH pakub põhjalikumat analüüsi kui Royal College of Radiologists (RCR) soovitatud 1D punktdoosi arvutamise meetod, mida praegu kasutatakse kiiritusravi lünkade lahendamiseks. Annuse jaotuse ruumala piires 1D-esitus ei võta arvesse OAR-e, millel on tavaliselt ebaühtlane annusejaotus, ja see võib OAR-i annust üle hinnata. Lisaks EQD2VH-tööriist võib koostada plaane mis tahes pikkusega ravivahe jaoks, samas kui RCR-i juhised põhinevad standardsel nelja- kuni viiepäevasel vaheajal.
Uue tööriista täiendavad eelised hõlmavad võimalust jälgida iga patsiendi plaanis olevat OAR-i, et minimeerida edasist annuse suurendamist, mis võib põhjustada ägedamat toksilisust. Kasutajad saavad ka arvutada erinevate ravivahede kestuste mõju patsiendi ravile. See võimalus aitab kindlaks teha, kas patsient tuleb üle viia teise kliinikusse, kui plaanilises kliinikus on liiga pikk vahe või kas patsient võib ohutult oodata ravi jätkumist.

Kuidas on COVID-19 mõjutanud kiiritusravi osutamist?
EQD2VH võib arvesse võtta ka muutusi üldises raviajas ja subletaalseid kahjustusi normaalsetes kudedes, mida kaubanduslik süsteem ei pruugi teha. Mis aga kõige tähtsam, tööriist ei pea toimimiseks olema haiglavõrguga ühendatud – seda saab kasutada ka siis, kui haigla serverid on endiselt küberründe tõttu halvatud.
"Me alles hindame EQD-d2VH kui otsustusvahend, ”ütleb juhtivteadur Margaret Moore Galway ülikooli haiglast. "See on osa praegusest projektist, mille käigus vaadatakse üle patsiendid, kes saavad mitu korda kordusravi palliatiivseks režiimiks, mille puhul annus fraktsiooni kohta on ebastandardne ja mille puhul võib kaaluda fraktsioneerimisskeemide valikut. Raviannuse teisendamine mitmest erineva fraktsiooniga ravist EQD-ks2 võimaldab koguda sihtkudede ja OAR-ide radiobioloogilise doosi üldise doosiülevaate saamiseks, mis võib aidata edasise ravi valikul otsustada.