Traumaatiline ajukahjustus (TBI), mis on põhjustatud äkilisest põrutusest või löögist peaga, vajab diagnoosimist nii kiiresti kui võimalik. Pöördumatute kahjustuste vältimiseks tuleb elukriitilised raviotsused teha traumajärgse “kuldse tunni” jooksul. TBI diagnoosimine hooldepunktis on keeruline, tuginedes kiirabibrigaadi tähelepanekutele, millele järgneb haiglasse saabumisel radioloogilised uuringud, nagu MRI või CT-skaneerimine.
Õigeaegsema sekkumise võimaldamiseks tegid teadlased Birminghami ülikool arendavad käeshoitavat diagnostikaseadet, mis tuvastab TBI, suunates silma ohutu laseriga. Seade, mida on kirjeldatud punktis Teadus ettemaksed, on mõeldud kasutamiseks kohe pärast vigastuse tekkimist – olgu siis tee ääres, lahinguväljal või spordiväljakul –, et hinnata patsientidel TBI suhtes, määrata trauma raskusaste ja suunata sellele vastavalt ravi.
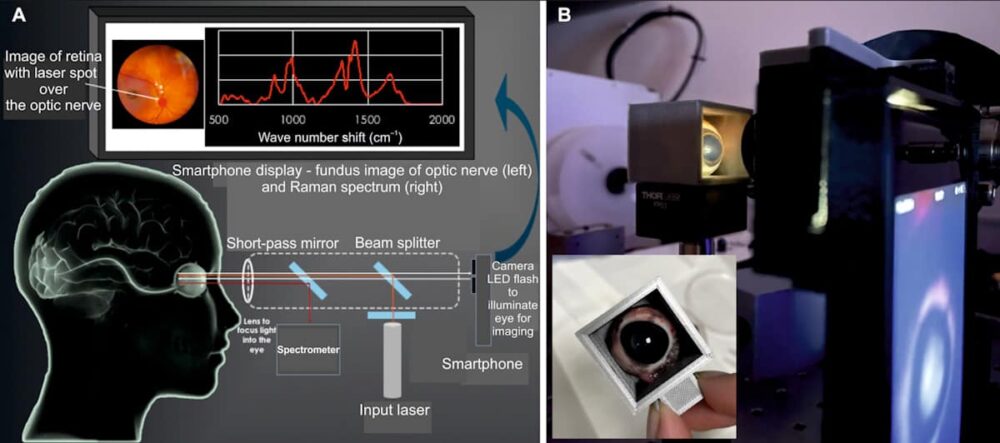
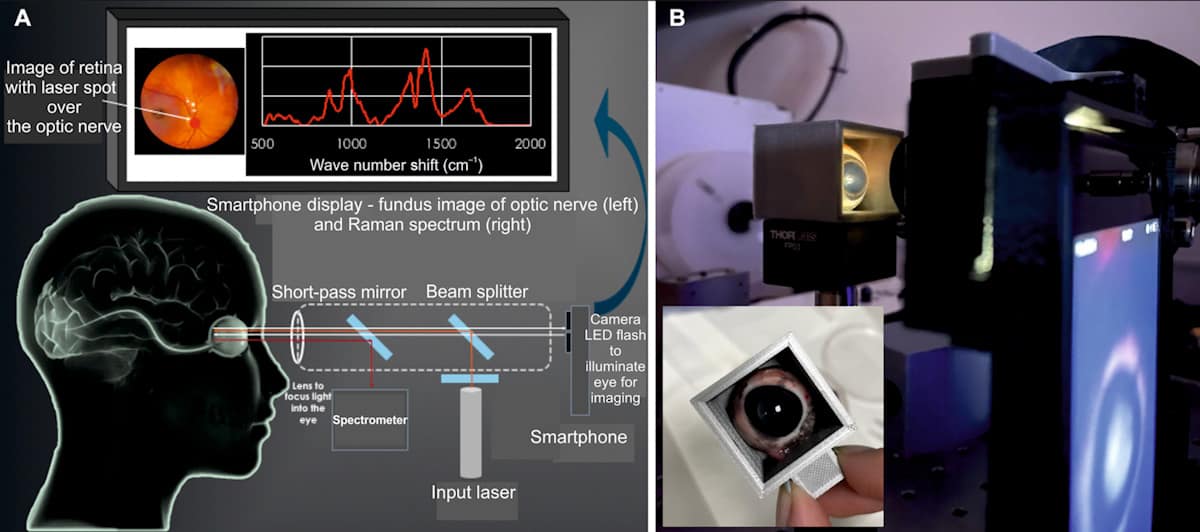
Silmadele ohutu seade (EyeD) põhineb Ramani spektroskoopial – optilisel tehnikal, mis kasutab molekulaarse koostise uurimiseks laservalguse mitteelastset hajumist. See töötab sarvkestale 635 nm 1. klassi laseriga. Seejärel fokusseeritakse kollimeeritud kiir silma enda optika abil võrkkestale. Laseri huvipakkuvasse piirkonda suunamiseks teostab EyeD-süsteem samaaegselt silmapõhja kujutise ja spektroskoopilise analüüsi, kasutades nutitelefoni kaamerat, et visualiseerida silma tagaosa.
Võrkkestast ja nägemisnärvist kogutud Ramani spektreid analüüsitakse TBI-spetsiifiliste biokeemiliste muutuste esinemise suhtes, kasutades otsustusabivahendina tehisnärvivõrgu algoritmi SKiNET. Kuna võrkkest ja nägemisnärv on ajuga nii tihedalt seotud, peegeldavad biomarkerite muutused pärast vigastust aju mikrokeskkonnas toimuvaid biokeemilisi muutusi.
"Meie seade võimaldab TBI varakult diagnoosida, hinnates otseselt reaalajas ägedaid stressimuutusi elavas neuroretinaalses / nägemisnärvi koes. See võimaldab meil uurida kesknärvisüsteemi kudesid otse ja mitteinvasiivselt, ”selgitab meeskonna juht Pola Goldberg Oppenheimer. "Neuroretina analüüs kesknärvisüsteemi projektsioonina annab akna aju biokeemiasse."
Spektroskoopilised uuringud
Oma pildiseadme toimivuse testimiseks konstrueerisid Oppenheimer ja kolleegid koefantoomi, mis jäljendab silma füüsilisi mõõtmeid ja optilisi omadusi, pakkudes samal ajal võrkkesta realistlikku Ramani allkirja. Fantoom sisaldab läätse, 4 mm läbimõõduga ava, mis esindab laienemata pupilli, ja võrkkesta koe proovihoidjat.
Meeskond näitas, et EyeD-seade suudab tõhusalt fokuseerida laserkiire võrkkesta soovitud asendisse. Kudefantoomist mõõdetud spektrid eraldasid suure lainearvuga piirkonnas peamised Ramani ribad, mida saab kasutada mitmete koetüüpide eristamiseks.
Järgmisena kasutasid teadlased prototüüpseadet, et analüüsida sigade silmade võrkkesta proove, mis on suuruse, struktuuri, arengu ja koostise poolest sarnased inimese silmadega. Nad kogusid 510 mõõtmist 39 TBI võrkkesta proovist ja 12 kontrollproovist, registreerides spektrid optilise ketta lähedalt. Üldiselt näitasid Ramani spektrid mitmeid iseloomulikke ribasid vahemikus 1200–1700 cm-1 sõrmejäljepiirkond, pluss suure lainearvuga ribade täiustamine vahemikus 2800–3200 cm-1 Piirkond.
SKiNETi kasutamine võrkkesta Ramani spektrite rühmitamist näitavate iseoptimeerivate kaartide (SOM) loomiseks näitas selget eraldumist TBI-ga võrkkesta ja kontrollproovide vahel. See tuleneb sellest, et Ramani spektrid peegeldavad biokeemilisi variatsioone silmas pärast TBI-d. Näiteks suurendab TBI lipiidide ja valgusisaldust silmas, põhjustades nendest pärinevate piikide Ramani spektrites rohkem väljendumist.
Kõige olulisemad spektraalsed muutused vastuseks TBI-le olid tingitud aju lipiidide kardiolipiini ja tsütokroom C panusest, mis väljendus 2930 ja 2850 cm suhte suurenemisena.-1 Ramani spektrite tipp. Teadlased kasutasid SKiNETi klassifikatsiooni moodustamiseks TBI spektri 2850/2930 piikide suhte valitud tunnuseid ja kuue iseloomuliku piigi intensiivsust, saades TBI tuvastamiseks spektroskoopilise vöötkoodi.
Et hinnata EyeD-süsteemi võimet eristada TBI-d võrkkesta muutuste kaudu, arvutasid nad iga piigi kõveraaluse pindala (AUC) ja piikide suhte 2930/2850 ning joonistasid tõelised positiivsed ja valenegatiivsed määrad. SKiNETi optimeerimise kasutamine koos treeningandmete 10-kordse ristvalideerimisega andis klassifitseerimise täpsuseks 90.7 ± 0.9%. See tulemus näitab, et muutused 2930/2850 tippsuhtes pärast TBI-d võivad olla väärtuslik näitaja TBI eristamiseks tervetest kontrollidest.
"Samaaegse Ramani spektroskoopia ja silmapõhja kujutise kasutamine, mis on pakitud odavaks käeshoitavaks seadmeks, annab esimese käegakatsutava tee TBI mitteinvasiivse hoolduspunkti diagnostika poole," räägib Oppenheimer. Füüsika maailm.

Põrutuste puhul on silmad aknad ajusse
Järgmine samm on prototüübi optimeerimine kliiniliseks valideerimiseks. Kliinilise tõlke hõlbustamiseks kavatsevad teadlased asendada eraldiseisva spektromeetri kompaktse seadmes oleva spektromeetri ja nutitelefoni näiduga, mis võimaldab ühe nutitelefoni ekraani kaudu silmapõhja pildistada ja Ramani spektroskoopiat.
"Praegu töötame välja kasutajasõbralikku juurutatavat seadet, mis on integreeritud meie tehisnärvivõrgu algoritmiga väljundite automatiseeritud tõlgendamiseks ilma spetsialistide tuge nõudmata, klassifitseerides kiiresti spektraalandmed," ütleb Oppenheimer. "[Samuti] hindame kliiniliselt seadme kasutatavust tervetel vabatahtlikel ja patsientidel, et näidata selle potentsiaali reaalajas diagnoosimiseks. Pärast seadme taluvuse ja kasutatavuse kindlakstegemist alustame esmakordset hindamist ja väikesemahulist kliinilist uuringut.
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- PlatoData.Network Vertikaalne generatiivne Ai. Jõustage ennast. Juurdepääs siia.
- PlatoAiStream. Web3 luure. Täiustatud teadmised. Juurdepääs siia.
- PlatoESG. Süsinik, CleanTech, Energia, Keskkond päikeseenergia, Jäätmekäitluse. Juurdepääs siia.
- PlatoTervis. Biotehnoloogia ja kliiniliste uuringute luureandmed. Juurdepääs siia.
- Allikas: https://physicsworld.com/a/handheld-device-uses-eye-safe-retinal-spectroscopy-to-diagnose-brain-injury/
- :on
- 1
- 10
- 12
- 39
- a
- võime
- AC
- vastavalt
- täpsus
- omandamine
- lisamine
- pärast
- vastu
- algoritm
- võimaldama
- Lubades
- Ka
- ameerika
- an
- analüüsima
- analüüs
- ja
- taotlus
- OLEME
- PIIRKOND
- ümber
- saabumine
- kunstlik
- AS
- hinnata
- Hindamine
- At
- vau
- Automatiseeritud
- tagasi
- põhineb
- lahinguväli
- BE
- Laius
- sest
- muutuma
- vahel
- Aju
- by
- arvutatud
- kaamera
- CAN
- põhjustatud
- põhjustades
- kesk-
- Vaidluste lahendamine
- iseloomulik
- omadused
- klass
- klassifikatsioon
- selge
- klõps
- kliiniline
- lähedal
- lähedalt
- Klastrite loomine
- kolleegidega
- kompaktne
- koostis
- mõiste
- Tingimused
- sisu
- sissemaksed
- kontrollida
- kontrolli
- võiks
- looma
- Praegu
- kõver
- kahju
- andmed
- otsus
- otsused
- näitama
- Näidatud
- kirjeldatud
- Disain
- soovitud
- Detection
- Määrama
- arenev
- & Tarkvaraarendus
- seade
- diagnoosimine
- diagnoos
- diagnostika
- diagnostika
- eristada
- raske
- mõõdud
- otsene
- otse
- eristama
- distress
- kaks
- iga
- leevendada
- tõhusalt
- võimaldama
- võimaldab
- võimaldades
- Inseneriteadus
- asutades
- hindamine
- hindamine
- näide
- Selgitab
- silm
- silmad
- FUNKTSIOONID
- sõrmejälg
- esimene
- Keskenduma
- keskendunud
- Järgneb
- Järel
- jalgpall
- eest
- vorm
- Alates
- juhataja
- tervislik
- omanik
- haigla
- aga
- HTTPS
- inim-
- pilt
- Imaging
- mõju
- in
- hõlmab
- Suurendama
- Tõstab
- näitab
- Indikaator
- info
- vigastus
- integreeritud
- tõlgendus
- sekkumine
- sisse
- Uuringud
- probleem
- IT
- ITS
- jpg
- laser
- juht
- valgus
- seotud
- elu-
- odava
- tehtud
- peamine
- kaardid
- max laiuse
- mõõdud
- molekulaarne
- rohkem
- kõige
- MRI
- rohkus
- peab
- võrk
- närvi-
- Närvivõrgus
- järgmine
- number
- of
- Pakkumised
- on
- peale
- avatud
- optika
- optimeerimine
- optimeerima
- or
- päritolu
- meie
- väljundid
- üldine
- enda
- pakendatud
- tee
- patsientidel
- tipp
- jõudlus
- täidab
- fantoom
- fotograafia
- füüsiline
- Füüsika
- Füüsika maailm
- Pigi
- kava
- Platon
- Platoni andmete intelligentsus
- PlatoData
- pluss
- kaasaskantav
- positsioon
- võimalik
- potentsiaal
- olemasolu
- vältida
- sond
- Projektsioon
- hääldatud
- omadused
- Valk
- prototüüp
- anda
- annab
- pakkudes
- kiiresti
- kiiresti
- Rates
- suhe
- reaalne
- reaalajas
- realistlik
- salvestamine
- kajastama
- piirkond
- tuginedes
- asendama
- esindavad
- Vajab
- Teadlased
- lahendatud
- vastus
- kaasa
- Võrkkest
- Revealed
- ohutu
- ütleb
- teadus
- Ekraan
- väljavalitud
- mitu
- näitas
- allkiri
- märkimisväärne
- sarnane
- üheaegselt
- ühekordne
- SIX
- SUURUS
- nutikas telefon
- So
- varsti
- spetsialist
- Spektraalne
- Spektroskoopia
- sport
- standalone
- Samm
- struktuur
- selline
- äkiline
- toetama
- süsteem
- materiaalne
- sihtmärk
- suunatud
- meeskond
- tehnika
- Tehnoloogia
- test
- et
- .
- Piirkond
- oma
- SIIS
- Need
- nad
- see
- Läbi
- thumbnail
- aeg
- õigeaegne
- et
- tööriist
- suunas
- koolitus
- Tõlge
- ravi
- kohtuprotsess
- tõsi
- liigid
- all
- peale
- us
- kasutatavus
- kasutama
- Kasutatud
- kasutajasõbralik
- kasutusalad
- kasutamine
- kinnitamine
- väärtuslik
- kaudu
- visualiseeri
- vabatahtlikud
- we
- olid
- kas
- mis
- kuigi
- will
- aken
- aknad
- koos
- jooksul
- ilma
- töötab
- maailm
- saagikus
- sephyrnet