HONGKONG, 17. veebruar 2022 – (ACN Newswire) – SinoMab BioScience Limited ("SinoMab" või "Ettevõte" koos oma tütarettevõtetega "Group", aktsiakood: 3681.HK), Hongkongis asuv biofarmatseutiline ravim ettevõttel, mis tegeleb immunoloogiliste haiguste raviks kasutatavate ravimite uurimise, arendamise, tootmise ja turustamisega, on hea meel teatada, et 11. veebruaril 2022 (EST kohaliku aja järgi) ilmus ettevõtte jaoks uute ravimite rakendus (IND) USA Toidu- ja Ravimiamet (FDA) on esitanud ja heaks kiitnud esimese klassi (FIC) astmaravitoote SM17 (humaniseeritud anti-IL17RB monoklonaalne süstimiseks mõeldud antikeha). Ettevõte kavatseb algatada USA-s uuringu First-In-Human 2022. aasta esimeses kvartalis, kui FDA on IND-i heaks kiitnud.
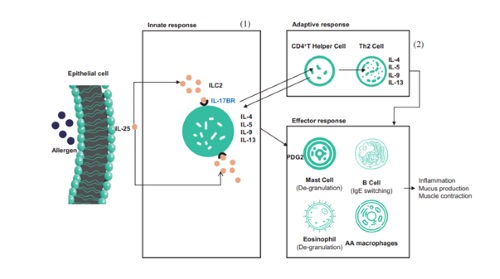 |
SM17 on maailma esimesed IL17BR-i sihtmärgiks olevad monoklonaalsed antikehad, mille on välja töötanud SinoMab ja LifeArc (Ühendkuningriigis asuv meditsiiniuuringute heategevusorganisatsioon). SM17-l on lai valik näidustusi, sealhulgas suure turumahuga näidustused, nagu astma ja kõrge suremusega haigused, nagu idiopaatiline kopsufibroos. Võrreldes teiste turul olevate toodetega on SM17-l eristavad eelised. SM17 prekliiniliste andmete ja ainulaadse toimemehhanismi põhjal usub ettevõte, et SM17-l on potentsiaalselt laiem ja kasulikum mõju astma ravile kui teistel heakskiidetud bioloogilistel ravimitel.
Ülemaailmsel turul suureneb astmahaigete arv järk-järgult ja peaks 247.5. aastaks jõudma 2023 miljonini ja 267.7. aastaks kasvama veelgi 2030 miljonini. Astmahaigete arv Hiinas kasvab kiiremini kui ülemaailmne tempo. prognoositakse, et 25.6. aastaks ulatub see 2023 miljonini ja suureneb veelgi 27.8 miljonini 2030. aastaks. Turu suuruse järgi ulatub ülemaailmne astmaturg 25.1. aastaks 2023 miljardi USA dollarini ja 34.6. aastaks 2030 miljardini. Eeldatakse, et Hiina Rahvavabariik jõuab 36.4. aastaks 2023 miljardi RMB ja 65.0. aastaks 2030 miljardi RMBni. Ravivõimaluste osas põhineb traditsiooniline astmaravi inhaleeritavatel kortikosteroididel, kuid neil on tõsine kõrvaltoime, eriti noorukitel. Pikaajalisel kasutamisel võib tekkida ka ravimiresistentsus. Eeldatakse, et SM17 kasutuselevõtt annab parema ravivõimaluse tõhususe ja ohutuse tasakaalu seisukohalt.
Dr Shui On LEUNG, SinoMabi esimees, tegevdirektor ja tegevjuht ütles, et: "pärast seda, kui NMPA võttis vastu SN1011 IND taotluse sclerosis multiplex'i raviks, võttis FDA täielikult vastu SM17 IND taotluse näitab ettevõtte uue ravimite uurimis- ja arendusprogrammi tõhusat elluviimist. Endiselt on rahuldamata meditsiiniline vajadus täiendavate tõhusate ravimeetodite järele, eriti patsientidel, kes ei allu praegusele ravile. Seetõttu oleme kindlad SM17 kliinilise arengu tohututes väljavaadetes. Meie tuum tooted, sealhulgas SM03, SN1011 ja SM17, edenevad kliinilises uurimis- ja arendustegevuses sujuvalt, ajendades ettevõtet liikuma stabiilselt kommertsialiseerimise suunas. Tulevikus kiirendame oma projektide elluviimist, et tuua kasu patsientidele ja luua aktsionäridele innovatsiooni kaudu väärtust.
SM17 kohta
SM17 on teadaolevalt maailma esimene humaniseeritud IgG4-k monoklonaalne antikeha uute ravimite väljatöötamiseks, mis on suunatud IL-17RB-le. Ja IL-17RB on I tüüpi üksik transmembraanne glükoproteiin, mis kuulub IL-17 retseptorite perekonda. SM17 seondumine IL-17RB-ga võib pärssida Th2 immuunvastuseid, mis on indutseeritud tsütokiinide kategooria nimega "alarmin", mis on osutunud seotud allergiliste haiguste ja hingamisteede viirusreaktsioonide patogeneesiga. Alternatiivne lähenemine, mis on suunatud Th2 põletikukaskaadi ülesvoolu vahendajatele, nagu "alarmiinid", avaldab eeldatavasti laiemat mõju hingamisteede põletikele ja tagab tõhusama astma kontrolli kui praegu saadaolevad ravimeetodid, ning SM17-ga sarnase toimemehhanismiga tooteid on kasutatud. FDA poolt heaks kiidetud.
Teave SinoMab BioScience Limited kohta
SinoMab BioScience Limited (börsikood: 3681.HK) on pühendunud immunoloogiliste haiguste raviks kasutatavate ravimite uurimisele, arendamisele, tootmisele ja turustamisele. Ettevõtte lipulaev SM03 on potentsiaalne ülemaailmne esimene sihtmärk-mAb CD22 vastu reumatoidartriidi (RA) raviks ja on praegu Hiinas reumatoidartriidi III faasi kliinilises uuringus, mis on tunnistatud üheks oluliseks eriotstarbeks. Kaheteistkümnenda viie aasta plaani perioodi ja kolmeteistkümnenda viie aasta plaani perioodi olulise uute ravimite väljatöötamise projektid. Lisaks on ettevõttel teisi potentsiaalseid sihtrühma ja esimese klassi ravimikandidaate, millest mõned on juba kliinilises staadiumis ja mille näidustused hõlmavad reumatoidartriiti (RA), süsteemset erütematoosluupust (SLE), pemphigus vulgaris't. (PV), mitte-Hodgkini lümfoomi (NHL), astma ja muude suurte kliiniliste vajadustega haigused.
Autoriõigus 2022 ACN Newswire. Kõik õigused kaitstud. http://www.acnnewswire.com ja immunoloogiliste haiguste raviks kasutatavate ravimite turustamine
- 11
- 2022
- 7
- kiirendama
- ACN Newswire
- tegevus
- Täiendavad lisad
- eelised
- Materjal: BPA ja flataatide vaba plastik
- juba
- Teatama
- taotlus
- lähenemine
- saadaval
- usub,
- Kasu
- Miljard
- eesistuja
- Heategevus
- juht
- tegevjuht
- Hiina
- kood
- kommertsialiseerumine
- ettevõte
- kindel
- kontrollida
- autoriõigus
- võiks
- Praegune
- andmed
- pühendunud
- arendama
- & Tarkvaraarendus
- Juhataja
- haigus
- haigused
- sõidu
- uimasti
- Narkootikumide
- mõju
- Tõhus
- tohutu
- eriti
- täidesaatev
- Tegevdirektor
- oodatav
- pere
- FDA
- esimene
- Järel
- toit
- tulevik
- Globaalne
- Suur
- HTTPS
- Kaasa arvatud
- Suurendama
- Innovatsioon
- teatud
- suur
- piiratud
- kohalik
- Pikk
- peamine
- Tegemine
- tootmine
- Turg
- meditsiini-
- miljon
- Ohvitser
- valik
- Valikud
- Muu
- faas
- Toode
- Toodet
- Programm
- projektid
- anda
- Kvartal
- R & D
- valik
- Rates
- teadustöö
- ohutus
- Ütlesin
- märkimisväärne
- sarnane
- SUURUS
- Stage
- varu
- Uuring
- esitatud
- Läbi
- aeg
- kokku
- traditsiooniline
- ravi
- kohtuprotsess
- meie
- ainulaadne
- Ühendatud
- Ühendkuningriik
- väärtus
- WHO