Võimalus ühendada elektroonikat ja optilisi andureid inimkehaga ühe raku tasandil võiks kunagi võimaldada üksikute rakkude kaugseiret ja juhtimist reaalajas. Elektroonika valmistamise edusammud on võimaldanud luua nanomõõtmelise eraldusvõimega transistore ja andureid, samas kui uuenduslikud nanomustri tehnikad võimaldavad neid seadmeid painduvatele aluspindadele kokku panna. Sellised protsessid nõuavad aga üldiselt tugevaid kemikaale, kõrgeid temperatuure või vaakumtehnikaid, mis ei sobi elusrakkudele ja kudedele.
Nende takistuste ületamiseks on Johns Hopkinsi ülikooli uurimisrühm välja töötanud mittetoksilise, kõrge eraldusvõimega ja kulutõhusa protsessi kulla nanomustrite trükkimiseks eluskudedele ja rakkudele. Oma leidudest teatamine Nano tähed, näitavad nad, et uus tehnika võib "tätoveerida" elavaid rakke ja kudesid kuldsete nanopunktide ja nanojuhtmete paindlike massiividega. Lõppkokkuvõttes saab seda meetodit kasutada nutiseadmete integreerimiseks eluskoega selliste rakenduste jaoks nagu bioonika ja biosensing.
"Kui meil oleks tehnoloogiaid isoleeritud rakkude tervise jälgimiseks, saaksime haigusi diagnoosida ja ravida palju varem ning mitte oodata, kuni kogu organ on kahjustatud," selgitab meeskonnajuht. David Gracias pressiteates. «Me räägime sellise asja nagu elektrooniline tätoveering panemisest nööpnõelapeast kümneid kordi väiksemale elavale objektile. See on esimene samm andurite ja elektroonika ühendamise suunas elavatele rakkudele.
Thanks, Luo Gu ja kolleegid on välja töötanud kolmeetapilise nanotransfer printimise protsessi kulla nanomustrite sidumiseks elusrakkudega. Esimeses etapis kasutasid nad tavalist nanoimprint litograafiat (NIL), et trükkida kuldsete nanopunktide või nanojuhtmete massiive polümeeriga kaetud räniplaatidele. Seejärel lahustasid nad polümeeri, vabastades nanokiibid klaasist katteklaasidele ülekandmiseks.
Järgmisena funktsionaliseerisid teadlased kullapinna tsüsteamiiniga ja katsid kuldsed NIL-massiivid alginaathüdrogeeli ülekandekihiga. Nad näitasid, et see lähenemisviis võib usaldusväärselt üle kanda 8 × 8 mm nanopunktide ja nanojuhtmete massiivi klaasist pehmetele ja painduvatele hüdrogeelidele. Viimases etapis konjugeeritakse kuldsed NIL-massiivid želatiiniga, et võimaldada nende ülekandmist elusrakkudele või koele. Hüdrogeeli ülekandekihi eraldamine paljastab kulla mustri.
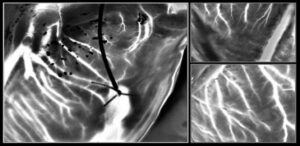
Teadlased uurisid elusate fibroblastirakkude käitumist, mis olid külvatud alginaathüdrogeelidel 250 nm läbimõõduga kuldtäppide massiividele (550 nm tsentritevaheline vahekaugus) või 300 nm laiustele kuldtraatidele (vahe 450 nm). Umbes 24 tundi pärast külvamist migreerusid nanojuhtmega trükitud hüdrogeeli rakud eelistatavalt paralleelselt nanojuhtmetega, samas kui nanopunktidel olevad rakud migreerusid juhuslikult, kuid veidi kiiremini. Nanojuhtmete rakkude pikenemine oli samuti ligikaudu kaks korda suurem kui nanopunktidel. Need leiud näitavad kuldsete NIL-massiivide võimet juhtida rakkude orientatsiooni ja migratsiooni.
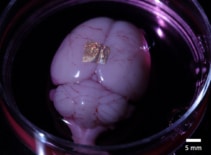
Lisaks sellele, et alginaathüdrogeel on rakkude ja kudedega bioühilduv, võib see kanda ka kullast NIL-massiivid elusorganitele ja rakkudele. Selle demonstreerimiseks paigutasid teadlased nanojuhtmega prinditud hüdrogeelid terve aju ajukoorele ja pärgarteri ajulõigule.
Pärast 2 tundi söötmes ja hüdrogeeli dissotsiatsiooni jäid nanojuhtmed kogu aju pinnaga seotuks. Seevastu ajulõigul olevad nanojuhtmed ei kleepunud, mis viitab sellele, et adhesioonitugevus varieerub erinevates rakutüüpides ja kultiveerimismeetodites. Teadlased märgivad, et tugeva pikaajalise sidumise jaoks on vaja täiendavaid uuringuid adhesioonimehhanismide iseloomustamiseks ja optimeerimiseks.
Lõpuks, et hinnata biotransfer printimist üheraku tasemel, kultiveerisid teadlased ühekihilisi rakulehti kullast NIL-massiiviga trükitud alginaathüdrogeelidel. 24 tunni pärast keerasid nad fibroblastidega külvatud hüdrogeelid želatiiniga kaetud katteklaasidele ja lasid rakkudel üleöö katteklaasidele kinnituda.
Pärast alginaathüdrogeeli dissotsiatsiooni näitas fluorestsentsmikroskoopia, et kulla nanodotsidega mustriga fibroblastide elujõulisus oli ligikaudu 97%, samas kui nanojuhtmetega mustriga fibroblastide elujõulisus oli ligikaudu 98%, mis näitab, et printimisprotsess on elusrakkudega bioloogiliselt ühilduv. Mustrilise fibroblasti rakkude lehel nähtavad peegeldavad värvid viitavad sellele, et kuldse NIL-massiivi kuju säilis.
Valmistamisprotsess ühildub ka mikroskaala fotolitograafiaga, mis võimaldas teadlastel luua 200 µm laiuseid kuusnurkseid ja kolmnurkseid kulla NIL-massiivide laike. Seejärel trükiti biotransfer need rakulehtedele, mis viis fibroblastirakkude selektiivse kasvuni mikroplaastritel. Üle 16 tunni salvestatud filmid näitasid, et rakud, mille peal olid prinditud nanojuhtmete laigud, tundusid terved ja võimelised migreeruma, kusjuures massiivid jäid pehmetele rakkudele isegi liikumise ajal.

Pisike andur mõõdab samaaegselt südamerakkude elektrilist ja mehaanilist aktiivsust
"Oleme näidanud, et suudame elusrakkudele kinnitada keerulisi nanomustreid, tagades samas, et rakk ei sure," ütleb Gracias. "See on väga oluline tulemus, et rakud saavad elada ja liikuda koos tätoveeringutega, kuna elusrakkude ja elektroonika valmistamise meetodite vahel on sageli märkimisväärne kokkusobimatus."
Gracias ja tema kolleegid järeldavad, et nende nanomustriprotsess koos standardsete mikrotootmismeetoditega "avab võimalused uute rakukultuuri substraatide, biohübriidmaterjalide, biooniliste seadmete ja biosensorite väljatöötamiseks". Järgmisena kavatsevad nad proovida kinnitada keerukamaid nanoskeeme, mis suudavad paigal püsida pikema aja jooksul, samuti katsetada erinevat tüüpi rakkudega.
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- PlatoData.Network Vertikaalne generatiivne Ai. Jõustage ennast. Juurdepääs siia.
- PlatoAiStream. Web3 luure. Täiustatud teadmised. Juurdepääs siia.
- PlatoESG. Autod/elektrisõidukid, Süsinik, CleanTech, Energia, Keskkond päikeseenergia, Jäätmekäitluse. Juurdepääs siia.
- PlatoTervis. Biotehnoloogia ja kliiniliste uuringute luureandmed. Juurdepääs siia.
- ChartPrime. Tõsta oma kauplemismängu ChartPrime'iga kõrgemale. Juurdepääs siia.
- BlockOffsets. Keskkonnakompensatsiooni omandi ajakohastamine. Juurdepääs siia.
- Allikas: https://physicsworld.com/a/researchers-tattoo-gold-nanopatterns-onto-live-cells/
- :on
- :on
- :mitte
- $ UP
- 16
- 200
- 24
- 8
- a
- võime
- Võimalik
- MEIST
- tegevus
- kinni pidama
- ettemaksed
- pärast
- Ka
- vahel
- an
- ja
- ilmunud
- rakendused
- lähenemine
- umbes
- OLEME
- ümber
- Array
- AS
- Kokkupanek
- hinnata
- At
- kinnitage
- BE
- sest
- on
- vahel
- keha
- võlakiri
- Aju
- kuid
- CAN
- Rakke
- iseloomustama
- klõps
- kolleegidega
- kombineeritud
- kokkusobiv
- keeruline
- lõpetama
- kontrast
- kontrollida
- tavaline
- kuluefektiivne
- võiks
- looma
- kultuur
- päev
- näitama
- kavandatud
- arenenud
- & Tarkvaraarendus
- seadmed
- DID
- Surema
- erinev
- haigused
- Ei tee
- Ajalugu
- Elektrooniline
- Elektroonika
- võimaldama
- lubatud
- Inseneride
- tagades
- Kogu
- Isegi
- Selgitab
- kiiremini
- lõplik
- järeldused
- esimene
- paindlik
- eest
- Alates
- edasi
- GAO
- üldiselt
- klaas
- Kuldne
- Kasv
- suunata
- olnud
- Olema
- juhataja
- Tervis
- tervislik
- süda
- Suur
- kõrgresolutsiooniga
- hopkins
- aga
- HTTPS
- inim-
- pilt
- oluline
- in
- eraldi
- info
- uuenduslik
- integreerima
- isoleeritud
- probleem
- IT
- johns
- Johns Hopkinsi ülikooli
- jpg
- kiht
- juht
- juhtivate
- laskma
- Tase
- nagu
- elama
- elu-
- pikaajaline
- enam
- tehtud
- materjalid
- max laiuse
- võib olla
- meetmed
- mehaaniline
- mehhanismid
- Meedia
- Merge
- meetod
- meetodid
- Mikroskoopia
- rännanud
- rännanud
- ränne
- järelevalve
- rohkem
- liikuma
- kolis
- Filmid
- palju
- vaja
- Uus
- järgmine
- objekt
- takistusi
- of
- sageli
- on
- ONE
- peale
- avatud
- Võimalused
- optimeerima
- or
- üle
- Ületada
- üleöö
- Parallel
- Paikade
- Muster
- perioodid
- Füüsika
- Füüsika maailm
- Koht
- kava
- Platon
- Platoni andmete intelligentsus
- PlatoData
- paigutatud
- võimalik
- vajutage
- trükk
- trükkimine
- protsess
- Protsessid
- Putting
- juhuslik
- ROT
- reaalne
- reaalajas
- dokumenteeritud
- jäi
- ülejäänud
- kauge
- Aruandlus
- nõudma
- teadustöö
- Teadlased
- resolutsioon
- kaasa
- Revealed
- jõuline
- ligikaudu
- ütleb
- nähtud
- selektiivne
- andur
- kuju
- leht
- näitas
- näidatud
- märkimisväärne
- Räni
- üheaegselt
- Viil
- väiksem
- nutikas
- Pehme
- midagi
- standard
- väljavõte
- jääma
- Samm
- tugevus
- uuringud
- selline
- soovitama
- Pind
- rääkimine
- meeskond
- tehnikat
- Tehnoloogiad
- kümneid
- kui
- et
- .
- oma
- SIIS
- Need
- nad
- see
- need
- thumbnail
- aeg
- korda
- et
- ülemine
- suunas
- jälgida
- üle
- käsitlema
- tõsi
- püüdma
- Kaks korda
- liigid
- lõpuks
- Ülikool
- kuni
- kasutama
- Kasutatud
- vaakum
- väga
- elujõulisus
- ootama
- oli
- we
- Hästi
- samas kui
- mis
- kuigi
- kogu
- lai
- koos
- maailm
- sephyrnet