Farmaatsiaettevõtted, kes taotlevad luba sellistelt reguleerivatelt asutustelt nagu USA Toidu- ja Ravimiamet (FDA) või Jaapani Farmaatsia- ja Meditsiiniseadmete Agentuur (PMDA), et müüa oma ravimeid turul, peavad esitama tõendid, mis tõendavad, et nende ravim on ettenähtud jaoks ohutu ja tõhus. kasutada. Arstide, statistikute, keemikute, farmakoloogide ja teiste kliiniliste teadlaste meeskond vaatab läbi kliinilise uuringu esitamise andmed ja kavandatud märgistuse. Kui läbivaatamise käigus leitakse, et on piisavalt statistilisi tõendeid selle kohta, et ravimist saadav kasu tervisele kaalub üles riskid, kiidetakse ravim müügiks heaks.
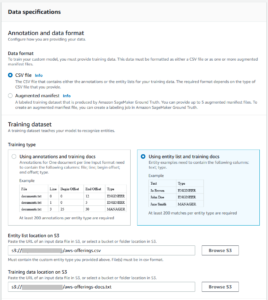
Kliiniliste uuringute esitamise pakett koosneb tabeliandmetest, analüüsiandmetest, uuringu metaandmetest ja statistilistest aruannetest, mis koosnevad statistilistest tabelitest, loenditest ja joonistest. USA FDA puhul on elektrooniline ühine tehniline dokument (eCTD) standardvorm taotluste, muudatuste, täienduste ja aruannete esitamiseks FDA bioloogiliste ainete hindamise ja uuringute keskusele (CBER) ning ravimite hindamise ja uuringute keskusele. CDER). FDA ja Jaapani PMDA jaoks on regulatiivne nõue esitada tabeliandmed CDISC standardandmete tabelimudelis (SDTM), analüüsiandmed CDISC analüüsiandmestiku mudelis (ADaM) ja proovi metaandmed CDISC Define-XML-is (operatsiooniandmete mudeli alusel). (ODM)).
Selles postituses näitame, kuidas saame RStudio't kasutada Amazon SageMaker selliste regulatiivsete esitamistulemuste loomiseks. Selles postituses kirjeldatakse kliiniliste uuringute esitamise protsessi, seda, kuidas saame kliiniliste uuringute andmeid sisse võtta, andmeid tabelistada ja analüüsida ning seejärel luua statistilisi aruandeid – kokkuvõtlikke tabeleid, andmeloendeid ja jooniseid (TLF). See meetod võimaldab farmaatsiaklientidel luua sujuva ühenduse oma AWS-i keskkonda salvestatud kliiniliste andmetega, töödelda neid R-i abil ja kiirendada kliiniliste uuringute uurimisprotsessi.
Ravimi väljatöötamise protsess
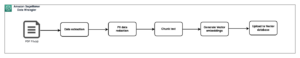
Ravimi väljatöötamise protsessi võib laias laastus jagada viieks peamiseks etapiks, nagu on näidatud järgmisel joonisel.
Umbes 10 15 potentsiaalse molekuli hulgast ühe ravimi edukaks heakskiitmiseks kulub keskmiselt 1–3 aastat ja ligikaudu 10,000–XNUMX miljardit USA dollarit. Uurimise varases faasis (ravimite avastamise faas) tuvastatakse paljutõotavad ravimikandidaadid, mis liiguvad edasi prekliiniliste uuringute juurde. Prekliinilises faasis püüavad teadlased esinemise teel välja selgitada ravimi toksilisust vitro katsed laboris ja in vivo katsed loomadega. Pärast prekliinilist testimist liiguvad ravimid kliinilise uuringu uurimisfaasi, kus neid tuleb inimeste peal testida, et teha kindlaks nende ohutus ja tõhusus. Teadlased kavandavad kliinilisi uuringuid ja kirjeldavad üksikasjalikult uuringuplaani kliinilise uuringu protokollis. Need määravad kindlaks erinevad kliiniliste uuringute faasid – alates väikestest 1. faasi uuringutest ravimite ohutuse ja annuste määramiseks kuni suuremate 2. faasi uuringuteni, et määrata ravimite efektiivsust ja kõrvaltoimeid, kuni veelgi suuremate 3. ja 4. faasi uuringuteni, et määrata ravimite efektiivsust, ohutust ja kõrvaltoimete jälgimine. Pärast edukaid kliinilisi inimkatseid esitab ravimisponsor ravimi turustamiseks uue ravimitaotluse (NDA). Reguleerivad asutused vaatavad läbi kõik andmed, teevad sponsoriga koostööd retsepti märgistamise teabe osas ja kiidavad ravimi heaks. Pärast ravimi heakskiitmist vaatavad reguleerivad asutused läbi turustamisjärgsed ohutusaruanded, et tagada toote täielik ohutus.
1997. aastal asutati vabatahtlike rühmana Clinical Data Interchange Standards Consortium (CDISC), ülemaailmne mittetulunduslik organisatsioon, mis koosneb farmaatsiaettevõtetest, CRO-dest, biotehnoloogiast, akadeemilistest institutsioonidest, tervishoiuteenuste osutajatest ja valitsusasutustest. CDISC on avaldanud andmestandardid, et lihtsustada andmete kogumist esitamise kaudu ning hõlbustanud andmevahetust partnerite ja pakkujate vahel. CDISC on avaldanud järgmised standardid:
- CDASH (kliiniliste andmete hankimise standardite ühtlustamine) – kogutud andmete standardid
- SDTM (Study Data Tabulation Model) – Tabeliandmete esitamise standardid
- ADaM (analüüsi andmemudel) – Analüüsiandmete standardid
- SAADA (mittekliiniliste andmete vahetamise standard) – Mittekliiniliste andmete standardid
- PRM (protokolli esitusmudel) – Protokolli standardid
Need standardid võivad aidata koolitatud ülevaatajatel standardsete tööriistade abil andmeid tõhusamalt ja kiiremini analüüsida, vähendades seeläbi ravimite heakskiitmise aega. USA FDA ja Jaapani PMDA regulatiivne nõue on esitada kõik tabeliandmed SDTM-vormingus.
R kliiniliste uuringute uuringute esitamiseks
SAS ja R on kaks enimkasutatavat statistilise analüüsi tarkvara, mida farmaatsiatööstuses kasutatakse. Kui CDISC alustas SDTM-i standardite väljatöötamist, oli SAS farmaatsiatööstuses ja FDA-s peaaegu universaalsel kasutusel. Kuid R kogub tänapäeval tohutut populaarsust, kuna see on avatud lähtekoodiga ning uusi pakette ja teeke lisatakse pidevalt. Õpilased kasutavad R-i peamiselt õppetöös ja uurimistöös ning võtavad selle R-i tundmise oma töösse kaasa. R pakub tuge ka uutele tehnoloogiatele, nagu täiustatud süvaõppe integratsioonid.
Pilvepakkujatest, nagu AWS, on nüüdseks saanud farmaatsiaklientide jaoks valitud platvorm oma infrastruktuuri majutamiseks. AWS pakub ka hallatavaid teenuseid, nagu SageMaker, mis muudab masinõppe (ML) mudelite loomise, treenimise ja juurutamise pilves vaevata. SageMaker võimaldab juurdepääsu RStudio IDE-le kõikjalt veebibrauseri kaudu. See postitus kirjeldab üksikasjalikult, kuidas statistilised programmeerijad ja biostatistikud saavad oma kliinilisi andmeid R-keskkonda neelata, kuidas R-koodi käitada ja kuidas tulemusi salvestatakse. Pakume koodilõike, mis võimaldavad kliiniliste uuringute andmete teadlastel XPT-faile R-keskkonda neelata, luua R-andmeraamid SDTM-i ja ADaM-i jaoks ning lõpuks luua TLF-i, mida saab salvestada Amazoni lihtne salvestusteenus (Amazon S3) objektide hoidmise ämber.
RStudio SageMakeris
2. novembril 2021 tegi AWS koostöös RStudio PBC teatas - üldine kättesaadavus RStudio SageMakeris, tööstuse esimene täielikult hallatav RStudio Workbench IDE pilves. Nüüd saate oma praeguse RStudio litsentsi tuua, et oma isehallatavad RStudio keskkonnad vaid mõne lihtsa sammuga SageMakerisse üle viia. Selle põneva koostöö kohta lisateabe saamiseks vaadake lehte RStudio väljakuulutamine Amazon SageMakeris.
Koos RStudio Workbenchiga pakub R-arendajatele mõeldud RStudio komplekt ka RStudio Connecti ja RStudio Package Manageri. RStudio Connect on loodud selleks, et andmeteadlased saaksid avaldada teadmisi, armatuurlaudu ja veebirakendusi. Selle abil on lihtne jagada andmeteadlaste keerulisest tööst saadud ML-i ja andmeteaduslikke teadmisi ja anda see otsustajate kätesse. RStudio Connect muudab ka sisu hostimise ja haldamise lihtsaks ja laialdaseks tarbimiseks skaleeritavaks.
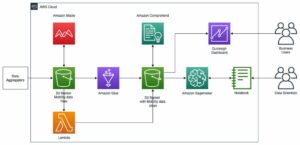
Lahenduse ülevaade
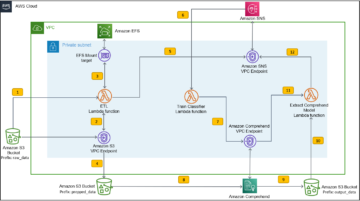
Järgmistes jaotistes arutame, kuidas saame importida töötlemata andmeid kaughoidlast või S3 ämbrist SageMakeri RStudios. Võimalik on ka otse ühendada Amazoni relatsioonide andmebaasiteenus (Amazon RDS) ja andmelaod nagu Amazoni punane nihe (Vt R ühendamine Amazon Redshiftiga) otse RStudiost; see aga jääb sellest postitusest välja. Pärast seda, kui andmed on paarist erinevast allikast sisse võetud, töötleme neid ja loome tabeli jaoks R andmeraamid. Seejärel teisendame tabeli andmeraami RTF-failiks ja salvestame tulemused tagasi S3 ämbrisse. Neid väljundeid saab seejärel potentsiaalselt kasutada regulatiivsetel eesmärkidel, eeldusel, et postituses kasutatud R-paketid on kliendi poolt regulatiivsete esildiste jaoks kasutamiseks valideeritud.
Seadistage SageMakeris RStudio
Juhiseid oma keskkonnas SageMakeris RStudio seadistamise kohta leiate aadressilt Alustage RStudioga SageMakeris. Veenduge, et RStudio täitmisrollil SageMakeris oleks juurdepääs andmete allalaadimiseks ja üleslaadimiseks S3 ämbrisse, kuhu andmed salvestatakse. Lisateavet R-pakettide haldamise ja analüüsi avaldamise kohta SageMakeris RStudio abil vaadake jaotisest Teatame täielikult hallatavast RStudiost saidil SageMaker andmeteadlastele.
Sisestage andmed RStudiosse
Selles etapis neelame andmeid erinevatest allikatest, et muuta need meie R-seansi jaoks kättesaadavaks. Toome andmeid SAS XPT formaadis; protsess on aga sarnane, kui soovite andmeid alla laadida muudes vormingutes. Üks RStudio kasutamise eelistest SageMakeris on see, et kui lähteandmed on salvestatud teie AWS-i kontodele, pääseb SageMaker andmetele natiivselt juurde, kasutades AWS-i identiteedi- ja juurdepääsuhaldus (IAM) rollid.
Juurdepääs kaughoidlasse salvestatud andmetele
Selles etapis impordime ADAM-i andmed saidilt FDA GitHubi hoidla. Loome kohaliku kataloogi nimega data RStudio keskkonnas andmete salvestamiseks ja demograafiliste andmete allalaadimiseks (dm.xpt) kaughoidlast. Selles kontekstis viitab kohalik kataloog kataloogile, mis on loodud teie privaatses Amazon EFS-i salvestusruumis, mis on vaikimisi lisatud teie R-seansi keskkonda. Vaadake järgmist koodi:
Kui see samm on lõpetatud, näete dm.xpt alla laaditakse, navigeerides aadressile Faile, andmed, dm.xpt.
Juurdepääs Amazon S3-sse salvestatud andmetele
Selles etapis laadime alla meie kontole S3 ämbrisse salvestatud andmed. Kopeerisime sisu FDA GitHubi hoidlast S3 ämbrisse nimega aws-sagemaker-rstudio selle näite jaoks. Vaadake järgmist koodi:
Kui samm on lõpetatud, näete pp.xpt alla laaditakse, navigeerides aadressile Faile, andmed, pp.xpt.
Töötle XPT andmeid
Nüüd, kui meil on R-keskkonnas saadaval SAS XPT-failid, peame need teisendama R-andmeraamideks ja töötlema. Me kasutame haven raamatukogu XPT-failide lugemiseks. Ühendame CDISC SDTM-i andmestikud dm ja pp ADPP andmestiku loomiseks. Seejärel loome ADPP andmeraami abil kokkuvõtliku statistikatabeli. Seejärel eksporditakse kokkuvõtlik tabel RTF-vormingus.
Esiteks loetakse XPT-faile kasutades read_xpt varjupaiga raamatukogu funktsioon. Seejärel luuakse analüüsi andmestik, kasutades sqldf funktsioon sqldf raamatukogu. Vaadake järgmist koodi:
Seejärel luuakse väljundandmete raam, kasutades üksuse funktsioone Tplyr ja dplyr raamatukogud:
Väljundandmete kaader salvestatakse seejärel RTF-failina RStudio keskkonna väljundkausta:
Laadige väljundid Amazon S3-sse
Pärast väljundi genereerimist paneme andmed tagasi S3 ämbrisse. Selle saavutamiseks loome uuesti SageMakeri seansi, kui seanss pole veel aktiivne, ja laadime väljundkausta sisu üles S3 ämbrisse, kasutades session$upload_data funktsioon:
Nende toimingutega oleme andmeid sisse võtnud, neid töödelnud ja tulemused üles laadinud, et need saaksid reguleerivatele asutustele esitada.
Koristage
Soovimatute kulude vältimiseks peate praegusest seansist väljuma. Valige lehe paremas ülanurgas toiteikoon. See peatab automaatselt aluseks oleva eksemplari ja peatab seetõttu soovimatud arvutuskulud.
Väljakutsed
Postituses on kirjeldatud samme S3 ämbrisse või kaughoidlast salvestatud töötlemata andmete allaneelamiseks. Siiski on kliinilise uuringu jaoks palju muid algandmete allikaid, peamiselt eCRF-i (elektroonilised juhtumiaruande vormid) andmed, mis on salvestatud EDC (elektrooniliste andmete kogumise) süsteemidesse, nagu Oracle Clinical, Medidata Rave, OpenClinica või Snowflake; laboriandmed; eCOA (kliinilise tulemuse hindamine) ja ePRO (elektroonilised patsiendi teatatud tulemused) andmed; reaalmaailma andmed rakendustest ja meditsiiniseadmetest; ja elektroonilised tervisekaardid (EHR) haiglates. Enne nende andmete regulatiivseks esitamiseks kasutatavaks muutmist on vaja märkimisväärset eeltöötlust. Konnektorite loomine erinevate andmeallikatega ja nende kogumine tsentraliseeritud andmehoidlasse (CDR) või kliiniliste andmete järve, säilitades samal ajal õiged juurdepääsukontrollid, kujutab endast olulisi väljakutseid.
Teine oluline väljakutse, mis tuleb ületada, on eeskirjade järgimine. Regulatiivsete esitamisväljundite loomiseks kasutatav arvutisüsteem peab vastama asjakohastele eeskirjadele, nagu 21 CFR Part 11, HIPAA, GDPR või mis tahes muud GxP nõuded või ICH juhised. See tähendab töötamist valideeritud ja kvalifitseeritud keskkonnas, kus on olemas juurdepääsu, turvalisuse, varundamise ja auditeeritavuse juhtelemendid. See tähendab ka seda, et kõik R-paketid, mida kasutatakse regulatiivsete esitamisväljundite loomiseks, tuleb enne kasutamist valideerida.
Järeldus
Selles postituses nägime, et mõned eCTD esitamise peamised tulemused olid CDISC SDTM, ADaM-i andmestikud ja TLF. Selles postituses kirjeldati nende regulatiivsete esitamistulemuste loomiseks vajalikke samme, sisestades esmalt paarist allikast pärinevad andmed SageMakeri RStudiosse. Seejärel nägime, kuidas saame sissevõetud andmeid XPT-vormingus töödelda; teisendada see R-andmekaadriteks, et luua SDTM, ADaM ja TLF; ja seejärel lõpuks laadida tulemused S3 ämbrisse.
Loodame, et postituses esitatud laiaulatuslike ideede abil saavad statistilised programmeerijad ja biostatistikud hõlpsasti visualiseerida kliiniliste uuringute andmete laadimise, töötlemise ja analüüsimise protsessi SageMakeris RStudiosse ning kasutada saadud teadmisi kohandatud meetodi määratlemiseks. töövoog, mis sobib teie regulatiivsete esildiste jaoks.
Kas oskate mõelda mõnele muule rakendusele RStudio kasutamiseks, et aidata teadlastel, statistikutel ja R-programmeerijatel oma elu lihtsamaks muuta? Meil oleks hea meel kuulda teie ideedest! Ja kui teil on küsimusi, jagage neid kommentaaride jaotises.
Vahendid
Lisateabe saamiseks külastage järgmisi linke:
Autoritest
 Rohit Banga on ülemaailmse kliinilise arendustöö spetsialist, kes asub Ühendkuningriigis Londonis. Ta on koolituselt biostatistik ja aitab Healthcare'i ja LifeScience'i klientidel juurutada AWS-is uuenduslikke kliinilisi arenduslahendusi. Ta on kirglik selle vastu, kuidas andmeteadust, AI/ML-i ja arenevaid tehnoloogiaid saab kasutada tõeliste äriprobleemide lahendamiseks tervishoiu- ja loodusteaduste valdkonnas. Vabal ajal meeldib Rohitile suusatada, grillida ning pere ja sõpradega aega veeta.
Rohit Banga on ülemaailmse kliinilise arendustöö spetsialist, kes asub Ühendkuningriigis Londonis. Ta on koolituselt biostatistik ja aitab Healthcare'i ja LifeScience'i klientidel juurutada AWS-is uuenduslikke kliinilisi arenduslahendusi. Ta on kirglik selle vastu, kuidas andmeteadust, AI/ML-i ja arenevaid tehnoloogiaid saab kasutada tõeliste äriprobleemide lahendamiseks tervishoiu- ja loodusteaduste valdkonnas. Vabal ajal meeldib Rohitile suusatada, grillida ning pere ja sõpradega aega veeta.
 Georgios Schinas on tehisintellekti/ML-i spetsialiseerunud lahenduste arhitekt EMEA piirkonnas. Ta asub Londonis ja teeb tihedat koostööd klientidega Ühendkuningriigis ja Iirimaal. Georgios aitab klientidel kavandada ja juurutada masinõpperakendusi tootmises AWS-is, tundes erilist huvi MLOps-i tavade vastu ja võimaldades klientidel teostada masinõpet ulatuslikult. Vabal ajal meeldib talle reisida, süüa teha ning sõprade ja perega aega veeta.
Georgios Schinas on tehisintellekti/ML-i spetsialiseerunud lahenduste arhitekt EMEA piirkonnas. Ta asub Londonis ja teeb tihedat koostööd klientidega Ühendkuningriigis ja Iirimaal. Georgios aitab klientidel kavandada ja juurutada masinõpperakendusi tootmises AWS-is, tundes erilist huvi MLOps-i tavade vastu ja võimaldades klientidel teostada masinõpet ulatuslikult. Vabal ajal meeldib talle reisida, süüa teha ning sõprade ja perega aega veeta.
- AI
- ai kunst
- ai kunsti generaator
- on robot
- Amazon SageMaker
- Amazon Simple Storage Service (S3)
- tehisintellekti
- tehisintellekti sertifikaat
- tehisintellekt panganduses
- tehisintellekti robot
- tehisintellekti robotid
- tehisintellekti tarkvara
- AWS-i masinõpe
- blockchain
- plokiahela konverents ai
- coingenius
- vestluslik tehisintellekt
- krüptokonverents ai
- dall's
- sügav õpe
- google ai
- Keskmine (200)
- Maaülikooli
- masinõpe
- Platon
- plato ai
- Platoni andmete intelligentsus
- Platoni mäng
- PlatoData
- platogaming
- skaala ai
- süntaks
- sephyrnet