باتریهای روی آبی جایگزینهای امیدوارکنندهای برای پسرعموهای لیتیوم یونی خود هستند، اما آنها از یکی از مشکلات مشابه رنج میبرند: تشکیل دندریت. این ساختارهای سوزنی مانند روی سطح آند روی شکل میگیرند و به الکترولیت تبدیل میشوند و باعث کوتاه شدن باتری یا در برخی موارد حتی مشتعل میشوند. اکنون تیمی از محققان در چین نشان داده اند که افزودن شکر معمولی (ساکارز) اصلاح شده شیمیایی با گروه های هیدروکسیل به الکترولیت می تواند رشد دندریت روی را با تغییر محیط حلال کند کند. علاوه بر این، ساکارز همچنین یک پوشش محافظ روی آند ایجاد می کند و خوردگی آن را کاهش می دهد.
باتریهای لیتیوم یون پرکاربردترین باتریهای امروزی در وسایل نقلیه الکترونیکی و الکتریکی قابل حمل هستند، اما الکترولیتهای آلی قابل اشتعال و سمی موجود در آنها باعث نگرانی است. لیتیوم همچنین در مقایسه با سایر فلزات رایج تر گران است و عرضه جهانی قربانی عدم قطعیت های مختلف است. باتریهای روی، که معمولاً با الکترولیتهای آبی تشکیل میشوند، یک جایگزین جذاب هستند، زیرا روی ارزانتر، سمیتر، راحتتر بازیافت میشود و در دسترستر از لیتیوم است. آنها همچنین دارای چگالی انرژی بالا، با ظرفیت ویژه بالا (820 میلی آمپر ساعت بر گرم و 5 میلی آمپر ساعت بر سانتی متر) هستند.3و پتانسیل ردوکس مطلوب (-0.76V در مقابل الکترود هیدروژن استاندارد) آند روی.
مشکل این است که وقتی یون روی (Zn2+) غلظت روی سطح آند به صفر می رسد، دندریت ها روی آن شروع به رشد می کنند. وجود این ساختارها باعث بدتر شدن عملکرد الکتروشیمیایی باتری می شود و در صورت عدم کنترل می تواند خطرناک باشد.
اصلاح محیط حلال
مطالعات اخیر نشان داده است که اصلاح محیط حلال (یا «ساختار حلالسازی») بهعنوان مثال، با معرفی نمکها یا گنجاندن مولکولهای کمتر آب، میتواند سرعت روی را افزایش دهد.2+ یون ها در پاسخ به میدان الکتریکی حرکت می کنند و بنابراین رشد دندریت را سرکوب می کنند. با این حال، چنین تنظیماتی متأسفانه هدایت یونی سیستم باتری را کاهش می دهد و منجر به عملکرد کلی ضعیف تر می شود.
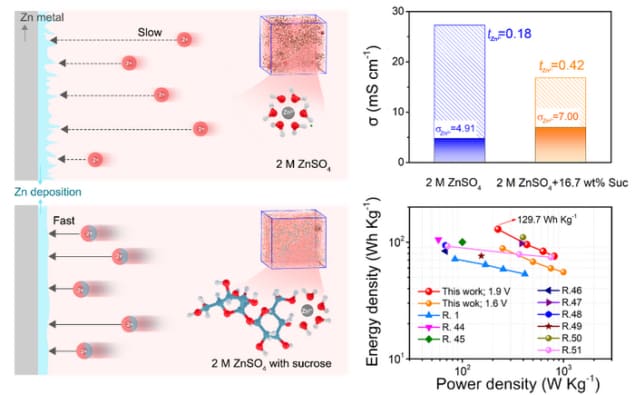
در مطالعه جدید، محققان به رهبری متخصص فناوری نانو مینان لیو از دانشگاه علم و فناوری چین دریافتند که معرفی ساکارز حاوی گروه های هیدروکسیل یک راه موثر برای تنظیم ساختار حلالیت روی است.2+ یون ها، که سرعت انتشار یون ها را بدون کاهش رسانایی یونی افزایش می دهد. ساکارز همچنین می تواند الکترولیت آبی را تثبیت کند و در عین حال روی آند روی جذب شود تا یک لایه محافظ روی آن تشکیل دهد. آنها می گویند که این مانع از خوردگی الکترولیت روی آند روی می شود.
ساکارز با گروه های هیدروکسیل به شدت با روی تعامل می کند2+ لیو توضیح می دهد که در مقایسه با مولکول های آب در الکترولیت. بنابراین میتواند جایگزین برخی از مولکولهای آب شود و با روی هماهنگ شود2+، بنابراین ساختار حلالیت یون ها را تنظیم می کند.
تشکیل دندریت کاهش یافت
روی اصلاح شده2+ ساختار حلالیت تأثیر مهمی بر سینتیک یون ها دارد، از جمله سرعت انتشار آنها در الکترولیت. دنیای فیزیک. نتایج تجربی ما به وضوح نشان میدهد که عدد انتقال روی2+ یون ها با معرفی ساکارز افزایش می یابد. این تحرک افزایش یافته یون ها به کاهش تشکیل دندریت ها کمک می کند.

نمک صنعتی یک باتری روی ایمن تر و پایدارتر می سازد
به گفته محققان، تکنیک آنها می تواند به دانشمندان کمک کند تا باتری های Zn با کارایی بالا تولید کنند و باتری Zn ایمن، سازگار با محیط زیست را به واقعیت نزدیک تر کند.
با نگاهی به آینده، لیو و همکارانش میگویند که قصد دارند روی تولید الکترولیتهایی با رسانایی یونی خوب که در دماهای پایینتر کار میکنند، تمرکز کنند. آنها به تفصیل مطالعه حاضر خود را در تحقیقات نانو.