درمانهای باکتریایی، که در آن از باکتریهای زنده برای تحویل دارو یا سایر محمولهها برای کشتن سلولهای سرطانی استفاده میشود، میتواند یک درمان جایگزین برای طیف وسیعی از سرطانها ارائه کند. هنگامی که باکتری ها به بدن انسان نفوذ می کنند، سیستم ایمنی یک مکانیسم مبارزه با ماده خارجی را آغاز می کند، که عواقب چنین رویدادهایی به قدرت باکتری بستگی دارد. با این حال، برخی از باکتری های پروبیوتیک، مانند اشریشیا کولی Nissle 1917 (EcN)، به راحتی در برابر خطوط دفاعی سیستم ایمنی مقاومت می کند. اگر چنین باکتری هایی برای کاربردهای درمانی در نظر گرفته شوند، می تواند مشکل ساز باشد.
باکتریهای زنده را میتوان طوری مهندسی کرد که به سیستم ایمنی حمله کنند، که منجر به دو نتیجه بالقوه میشود: سازش در سیستم ایمنی پس از تحویل باکتری. و باکتری های زنده ای که باعث سمیت سلول های میزبان آن می شوند. در طول دهه گذشته، محققان کاهش سمیت باکتریهای زنده را با حذف ژنتیکی بخشهایی از باکتری که میتوانند باعث مسمومیت شوند، بررسی کردهاند. اما این می تواند منجر به جهش های ناخواسته در خود باکتری شود و ممکن است به طور قابل توجهی اثر درمانی را کاهش دهد.
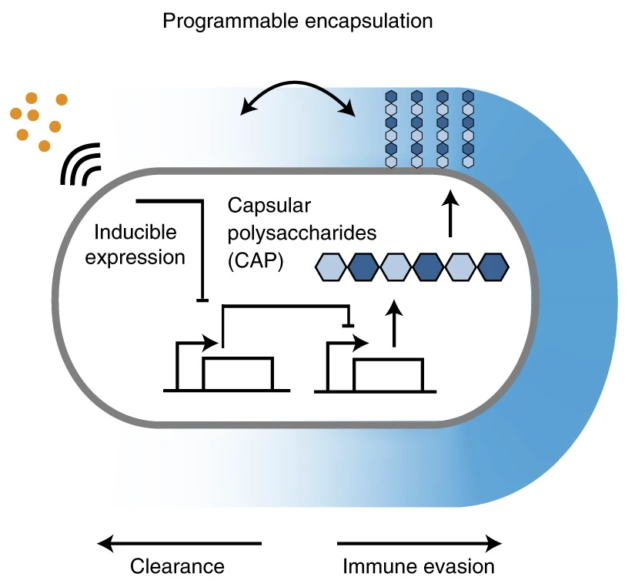
تیمی از مهندسان از دانشگاه کلمبیا اکنون یک رویکرد موثر برای افزایش انتقال باکتریهای زنده مهندسی شده به سلولها تعیین کرده است، در حالی که یکپارچگی باکتری را حفظ کرده و سمیت را به حداقل میرساند. گزارش یافته های خود در بیوتکنولوژی طبیعتمحققان روشی را برای پوشاندن باکتری های مهندسی شده با یک پلی ساکارید کپسولی القایی (iCAP) توصیف می کنند که وقتی وارد بدن می شود به شیوه ای هوشمندانه پاسخ می دهد.
پلی ساکارید کپسولی (CAP) لایه ای از مولکول های آب است که سطح باکتری های طبیعی را می پوشاند و به عنوان محافظی در برابر عفونت های خارجی عمل می کند. با تبدیل CAP به iCAP، محققان میتوانند از محرکهای خارجی قابل برنامهریزی استفاده کنند که باکتریهای مهندسیشده را قادر میسازد تا از حمله ایمنی فرار کنند، برای مدت زمان قابلتوجهی در محیط میزبان زنده بمانند و دوز درمانی قابل تحملی را ارائه کنند.
هدایت باکتری ها
سلولهای سرطانی دارای توانایی طبیعی برای فرار از سیستم ایمنی هستند که یکی از نشانههای مهم سرطان است. از آنجایی که باکتریهای مهندسیشده نیز برای فرار از حمله ایمنی مورد نیاز هستند، هدف قرار دادن باکتریها برای تومورها به یک کار دشوار تبدیل میشود، که به طراحی بسیار پیچیدهای نیاز دارد تا محلیسازی کافی باکتریها در تومورها را ممکن کند.
محققان از مدارهای ژن مصنوعی برای کنترل پویا نحوه تعامل باکتری ها با محیط اطراف خود با استفاده از iCAP استفاده کردند. علاوه بر محافظت در برابر فشارهای محیطی و تشکیل سدی برای دیواره باکتری، CAP همچنین نقش مهمی در سنجش پاسخ های ایمنی ایفا می کند. برای کنترل بیان CAP، نویسندگان یک القا کننده مولکول کوچک به نام IPTG معرفی کردند. القای CAP با IPTG، برهمکنش های باکتری را با ضد میکروبی های در حال گردش، باکتریوفاژها، اسیدها و سیستم ایمنی میزبان تعدیل کرد.
سیستم iCAP برای برنامه های کاربردی سرطان
در حالی که درمان های باکتریایی برای سرطان همچنان در حال پیشرفت هستند، توسعه یک سیستم قوی برای کشتن همه تومورها ممکن است غیرقابل حل به نظر برسد. با این حال، به عنوان نقطه شروع، محققان نشان دادند که سیستم iCAP میتواند تحویل درمانی را در مدلهای موش کنترل کند.
برای بررسی اثربخشی iCAP، محققان ابتدا زنده ماندن باکتری در خون کامل انسان را بررسی کردند. آنها دریافتند که باکتری های مهندسی شده به طور قابل توجهی بیشتر از باکتری های دارای CAP طبیعی زنده می مانند. علاوه بر این، پس از تجویز باکتری iCAP به موشها، آنها واکنشهای التهابی کمتری را در مقایسه با باکتریهای غیر مهندسی مشاهده کردند.
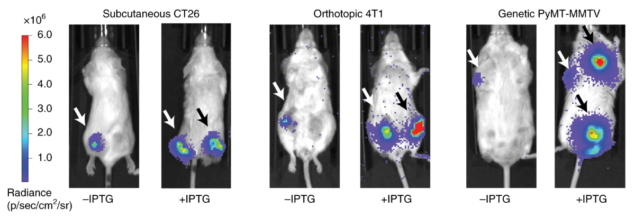
در موشهای حامل تومور، iCAP همچنین انتقال باکتریهای درمانی را به تومورهای دیستال متعدد در سراسر بدن، با افزایش قاچاق در مقایسه با باکتریهای طبیعی، فعال کرد. علاوه بر این، ارائه یک ساختار EcN iCAP مهندسی شده برای تولید یک سم ضد تومور منجر به کاهش رشد تومور در موشها شد و کارایی درمانی آن را نشان داد.
تال دانینونویسنده ارشد این مطالعه، اکنون قصد دارد استفاده از iCAP و سایر درمانهای مبتنی بر باکتری را برای تسریع ترجمه بالینی در آینده بیشتر بررسی کند.
پست باکتری های سرطان کش از سیستم ایمنی فرار می کنند به نظر می رسد برای اولین بار در دنیای فیزیک.
- 10
- a
- توانایی
- شتاب دادن
- حکومت
- پیشرفت
- در برابر
- معرفی
- جایگزین
- برنامه های کاربردی
- درخواست
- روش
- نویسندگان
- سد
- بودن
- سیاه پوست
- خون
- بدن
- علت
- باعث می شود
- مقایسه
- ادامه دادن
- کنترل
- میتوانست
- دهه
- دفاع
- تحویل داده
- تحویل
- تحویل
- نشان
- وابسته
- استقرار
- توصیف
- طرح
- در حال توسعه
- توزیع
- مواد مخدر
- به آسانی
- موثر
- قادر ساختن
- را قادر می سازد
- مورد تأیید
- محیط
- محیطی
- حوادث
- اکتشاف
- نام خانوادگی
- خارجی
- یافت
- از جانب
- بیشتر
- بعلاوه
- آینده
- رشد
- خیلی
- چگونه
- اما
- HTTPS
- انسان
- تصویر
- تصاویر
- مهم
- افزایش
- تمامیت
- بررسی
- خود
- لایه
- رهبری
- رهبری
- خطوط
- زنده
- زندگی
- محل
- روش
- مکانیزم
- قدرت
- مدل
- چندگانه
- طبیعی
- طبیعت
- دیگر
- برنامه
- بازی
- نقطه
- پتانسیل
- تولید کردن
- ارائه
- محدوده
- ضروری
- محققان
- نتیجه
- نشان
- قابل توجه
- پس از
- هوشمند
- برخی از
- مصنوعی
- محرک
- مهاجرت تحصیلی
- ماده
- سطح
- سیستم
- هدف گذاری
- تیم
- La
- سراسر
- ترجمه
- رفتار
- استفاده کنید
- مختلف
- آب
- در حین