درمان محرومیت از آندروژن (ADT) درمان اصلی سرطان پروستات متاستاتیک است، اما پیشرفت به سرطان پروستات مقاوم به اخته (CRPC) تقریباً جهانی است. در سالهای اخیر، مهارکنندههای قوی گیرنده آندروژن (AR) از جمله آنتاگونیست AR انزالوتامید توسعه یافتهاند.
در حالی که در بیشتر موارد موفقیت آمیز است، این داروها در نهایت می توانند کار خود را متوقف کنند، درک محدودی از چگونگی این تغییر وجود دارد. یک مطالعه جدید از دانشگاه میشیگان مرکز سرطان Rogel نشان میدهد که مهارکنندههای گیرنده آندروژن میتوانند اساساً عملکرد تومورهای پروستات را دوباره سیمکشی و شکل دهند و در موارد خاص حتی آنها را تهاجمیتر کنند.
Joshi Alumkal، M.D.، پروفسور انکولوژی خانواده ویچا و پروفسور داخلی، که تیم او این تحقیق را با همکاری آزمایشگاه ژنگ شیا در موسسه سرطان نایت دانشگاه علوم و بهداشت اورگان رهبری کرد، گفت: "بزرگترین نیاز برآورده نشده در کلینیک در حال حاضر درک راه حل های توموری است که در برابر داروهای هدف گیرنده گیرنده آندروژن مقاوم می شود، بنابراین ما می توانیم بهترین نحوه درمان بیماری را که تومورش شروع به رشد کرده است، تعیین کنیم."
هنگامی که انزالوتامید کار خود را متوقف می کند، گزینه های محدودی وجود دارد. ما نمی دانیم که چگونه و چرا اکثر تومورها مقاوم می شوند."
دانشمندان می خواستند در ابتدا آنچه در این تومورها وجود دارد و پس از شروع رشد تومورها در درمان با انزالوتامید چه اتفاقی افتاد را درک کنند. بیماران در یک کارآزمایی طولانی مدت برای جمع آوری بیوپسی های متاستاتیک قبل و بعد از ایجاد مقاومت درمانی تومور ثبت نام کردند. دانشمندان نمونههای مکرری را از ۲۱ بیمار بهدست آوردند که به آنها اجازه داد مکانیسمهای موجود در تومور هر بیمار را درک کنند.
آلومکال می گوید، این بزرگترین مجموعه بیوپسی متاستاتیک مشابه قبل و بعد از انزالوتامید است. برای درک مقاومت در برابر داروها، محققان اغلب نمونه هایی را از برخی از بیماران قبل از درمان و از گروه دیگری که تومورهای آنها مقاوم به درمان هستند جمع آوری می کنند. با این حال، این رویکرد بسیار دقیق تر است زیرا ممکن است تفاوت های قابل توجه دیگری بین این بیماران وجود داشته باشد. شما نمی توانید مشخص کنید که آیا تفاوت ها ارتباطی با قرار گرفتن در معرض مواد مخدر دارند یا بیشتر به تفاوت تومورها مربوط می شود.
روش نمونهبرداری متوالی تصویر واضحتری از چگونگی ظهور مقاومت انزالوتامید ارائه میدهد.
پس از مقایسه نمونه پایه با نمونه پیشرفت از همان بیمار، دانشمندان تغییرات قابل توجهی در بیان ژن در اکثر تومورها پیدا نکردند.
آلومکال می گوید، این که برنامه بیان ژن یک تومور قبل از درمان از نظر پیشرفت در زمانی که انزالوتامید مصرف می کرد بسیار شبیه به نظر می رسید بسیار قابل توجه است. این نشان می دهد که بسیاری از تومورها چگونه می توانند با وجود درمان با انزالوتامید، موتور گیرنده آندروژن را سازگار کنند و روشن نگه دارند.
اما این تنها شگفتی نبود.
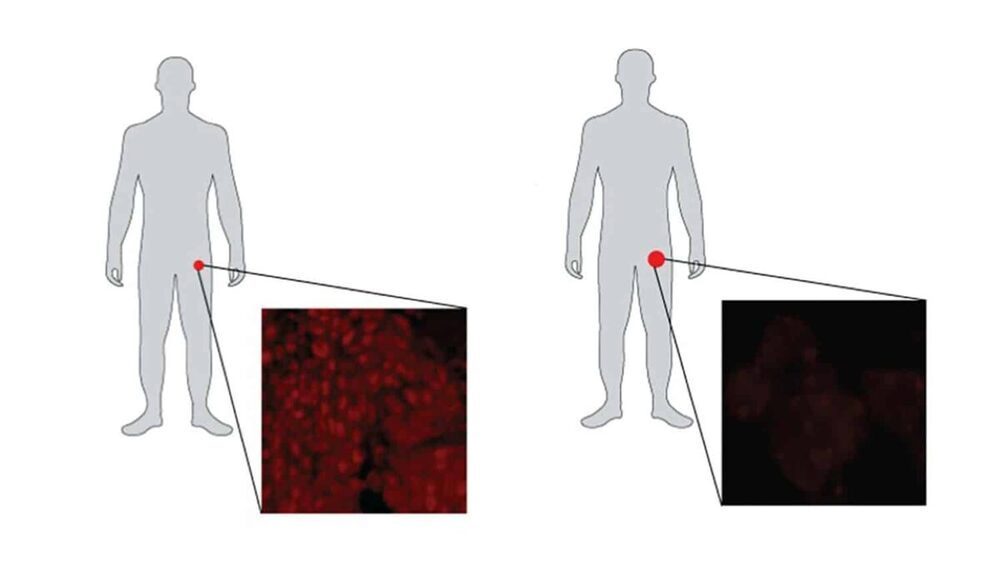
در سه مورد از 21 مورد، آلومکال و تیمش شاهد تغییر عمیقی در سیم کشی تومورها - یا برنامه بیان ژن - بودند.
آلومکال گفت، ما می دانستیم که گاهی اوقات تومورها مستقل از سوخت می شوند و دیگر به گیرنده آندروژن متکی نیستند. این تومورها در عوض یک برنامه بیان ژنی را فعال میکنند که در سلولهای عصبی رایجتر است، نه سلولهای پروستات، و به شکل تهاجمی به نام سرطان پروستات نورواندوکرین تغییر میکنند.
در 15 درصد موارد، تومورها نیز به دلیل دیگری مستقل از سوخت شدند. این تومورها به طور منحصربهفردی سیمکشی شده بودند و بیشتر با زیرشاخهای از سرطان پروستات به نام سرطان پروستات دو منفی سازگار بودند، به این معنی که تومورها دیگر گیرنده آندروژن را به عنوان موتور ندارند. اما آنها همچنین به سرطان پروستات نورواندوکرین تبدیل نشدند.
«در ابتدا، تقریباً تمام تومورهای پروستات گازهای گلولهای هستند: بسیار وابسته به سوخت هستند و به عنوان موتور توسط گیرنده آندروژن تغذیه میشوند. هنگامی که با درمانهای هورمونی درمان میشوند، بیشتر تومورها وابسته به سوخت باقی میمانند، اما مصرف سوخت را بهینهتر میکنند و میتوانند با بنزین کمتر جلوتر بروند.
کار ما نشان داد که اکثر تومورها - حتی پس از دریافت انزالوتامید - بسیار وابسته به سوخت باقی می مانند، که نشان می دهد ادامه هدف قرار دادن گیرنده آندروژن می تواند تفاوت زیادی در این تومورها ایجاد کند.
آلومکال دریافت که سه تومور به سرطان پروستات مضاعف منفی تبدیل میشوند - شبیه به یک وسیله نقلیه الکتریکی. موتور بنزینی با مجموعه ای کاملاً متمایز از ماشین آلات جایگزین شد که به تومورها اجازه رشد و بقا را می داد. جهشهای DNA یافت شده در بیوپسیهای اولیه و پیشرفت از این تومورهای مبدل یکسان بودند، که قویاً نشان میدهد که انزالوتامید به طور کامل موتور تومور وابسته به سوخت اصلی را مجدداً سیمکشی کرد تا در پیشرفت بیماری از سوخت مستقل شود. این یک تغییر چشمگیر است که سر خود را به اطراف بپیچید.»
تیم آلومکال ژنهای خاصی را کشف کردند که به شدت در تومورهای پایه بیان میشدند که در نهایت به سرطان پروستات دو منفی تبدیل شدند، علیرغم اینکه تومورهای پایه در زیر میکروسکوپ ظاهری مشابه داشتند. این یافته حاکی از آن است که برخی از تومورها در یک شرایط ترکیبی وجود دارند که در ابتدا وابسته به سوخت هستند اما مستعد ابتلا به سرطان پروستات دو منفی پس از درمان با انزالوتامید هستند.
آلومکال می گوید:, نتایج حاصل از روش نمونه گیری متوالی نشان می دهد که انزالوتامید باعث سازگاری تومورها می شود، در برخی موارد به طور چشمگیری.
آلومکال اشاره می کند که امضای ژنی که او شناسایی کرد مقدماتی است و تیم کار بیشتری برای انجام دادن دارد. با این حال، این واقعیت است که DNA ظاهر مشابه در مبدل ها به شدت نشان می دهد که انزالوتامید در حال برنامه ریزی مجدد تومورها است. کارهای بیشتری برای انجام دادن داریم، اما ممکن است بتوان بیمارانی را که در معرض بیشترین خطر مستقل شدن تومورشان پس از درمان با داروهایی مانند انزالوتامید هستند، از قبل شناسایی کرد.
مرجع مجله:
- Westbrook, T.C., Guan, X., Rodansky, E. et al. پروفایل رونویسی بیوپسیهای بیمار همسان، عوامل مولکولی شکلپذیری دودمان ناشی از انزالوتامید را روشن میکند. Nat Commun 13، 5345 (2022). DOI: 10.1038/s41467-022-32701-6