حملات سایبری به بیمارستانها میتواند تأثیر مخربی داشته باشد، بهویژه برای بخشهای رادیولوژی و رادیوتراپی که به ویژه برای عملکرد به فناوری وابسته هستند. نمونه بارز آن حمله سایبری سراسری به خدمات بهداشت عمومی ایرلند در ماه مه 2021 است که درمان های رادیوتراپی برنامه ریزی شده برای برخی از بیماران سرطانی را تا 12 روز قطع کرد.
در پی این حادثه، فیزیکدانان پزشکی در بیمارستان دانشگاه گالوی و دانشگاه ملی ایرلند گالوی شروع به توسعه یک ابزار داخلی برای کمک به ایجاد برنامه های درمان رادیوتراپی اصلاح شده پس از ایجاد وقفه کرد. ابزار - به نام EQD2VH – برنامههای جبران درمان را محاسبه میکند و امکان مقایسه بصری همه گزینههای طرح، و همچنین تجزیه و تحلیل فردی هر ساختار در برنامه بیمار را فراهم میکند. محققان ابزار نرم افزاری جدید را در مجله فیزیک پزشکی بالینی کاربردی.
رادیوتراپی معمولاً طی چند هفته در یک سری دوزهای کوچک پرتو (معمولاً 2 گری) به نام فراکسیون انجام می شود. شکاف های درمانی برنامه ریزی نشده – چه به دلیل حملات سایبری، خرابی ماشین آلات یا بیماری بیمار – می تواند باعث شکست های قابل توجهی شود. در طول چنین شکافهایی، سلولهای سرطانی به سرعت در بافت تومور جمعآوری میشوند، که منجر به کاهش دوز رادیوبیولوژیکی به حجم هدف برنامهریزی (PTV) میشود.

برای رفع این مشکل، EQD2VH از اطلاعات هیستوگرام دوز-حجم (DVH) استخراج شده از برنامه های اصلی بیمار برای انجام محاسبات فاصله درمان استفاده می کند. نویسنده اصلی، Katie O'Shea، از دانشگاه ملی ایرلند گالوی، و همکارانش توضیح میدهند که این نرمافزار دوز فیزیکی موجود در هر سطل دوز (محدوده دوز بین نقاط داده در یک DVH) را به دوز مؤثر بیولوژیکی (BED) تبدیل میکند. این هم برای اثرات جمعیت مجدد در PTV و هم اثرات آسیب های زیر کشنده به بافت طبیعی ترمیم نشده در اندام های در معرض خطر (OARs) را به حساب می آورد.
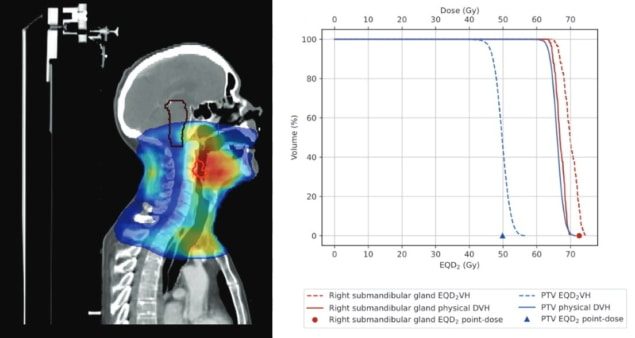
پس از اصلاح تبدیل BED برای محاسبه تغییرات دوز در هر ساختار، با استفاده از روش دز متغیر، ابزار BED را برای هر ساختار به دوز معادل در کسر 2 گری (EQD) تبدیل میکند.2). این امر هر درمان را به تقسیم بندی معمولی عادی می کند و امکان جمع کردن طرح هایی با طرح های تقسیم بندی مختلف را با هم فراهم می کند. EQD حاصل2 DVH مبتنی بر یک نمایش دوبعدی از تأثیر استراتژیهای جبران شکاف درمان بر روی توزیع دوز PTV و OAR در مقایسه با طرح درمان تجویز شده ارائه میکند.
برای ارزیابی EQD2VH به عنوان یک ابزار تصمیم گیری بالینی، محققان پنج بیمار با اولویت بالا با تومورهای در حال رشد سریع را انتخاب کردند که فاصله درمان آنها نباید بیش از دو روز باشد. این شامل چهار بیمار مبتلا به سرطان سر و گردن بود که تحت رادیوتراپی تعدیلشده با شدت و یک بیمار سرطان ریه تحت رادیوتراپی سهبعدی منسجم قرار میگرفتند که وقفههای درمانی 3 یا 12 روزه داشتند. این موارد تیم را قادر ساخت تا استفاده از EQD را ارزیابی کند2VH برای بیماران با هر دو تقسیم بندی معمولی (2 گری) و غیر متعارف (2.2 گری) و زمان های فاصله درمانی متفاوت (از 46 تا XNUMX روز پس از درمان).
برنامههای درمانی اصلاحشده برای هر بیمار بر اساس برنامههای اولیه آنها با دوز به ازای هر کسر یا تعداد فراکسیونها تغییر کرده بود. O'Shea توضیح می دهد که برنامه و برنامه بازنگری شده هر بیمار از ترکیبی از تقسیم دو بار در روز، درمان های آخر هفته و افزایش دوز به حجم هدف برای کاهش اثرات جمعیت مجدد سلولی استفاده می کند.
این طرحها درمان را به شش فراکشن در هفته محدود میکردند و از تقسیمبندی دو بار در روز در روزهای متوالی جلوگیری میکردند. اگر درمان تجویز شده نتواند در بازه زمانی مورد نیاز تکمیل شود، محققان برنامههایی را با استفاده از هیپوفرکشناسیون (ارائه افزایش دوز به ازای هر کسر) بررسی کردند. آنها قادر به مقایسه بصری و کمی برنامه های اصلاح شده مختلف با طرح اولیه بیمار بودند تا تعیین کنند کدام دوز بهترین دوز را با کمترین دوز به OAR ها به PTV تحویل می دهد.
محققان خاطرنشان می کنند که نمایش دوبعدی هر ساختار فردی در EQD2VH تجزیه و تحلیل عمیق تری نسبت به روش محاسبه نقطه دوز 1 بعدی توصیه شده توسط کالج سلطنتی رادیولوژیست ها (RCR) ارائه می دهد که در حال حاضر برای مدیریت شکاف های رادیوتراپی استفاده می شود. یک نمایش 1 بعدی از توزیع دوز در یک حجم، OAR هایی را که معمولاً توزیع دوز غیریکنواختی دارند را در نظر نمی گیرد و می تواند دوز OAR را بیش از حد تخمین بزند. علاوه بر این، EQD2ابزار VH می تواند برنامه هایی را برای هر طول شکاف درمانی ایجاد کند، در حالی که دستورالعمل های RCR بر اساس فاصله استاندارد چهار تا پنج روزه است.
مزایای اضافی ابزار جدید شامل توانایی نظارت بر هر OAR در برنامه بیمار برای به حداقل رساندن افزایش بیشتر دوز است که می تواند باعث سمیت حاد بیشتری شود. کاربران همچنین میتوانند تأثیر دورههای مختلف فاصله درمان را بر درمان بیمار محاسبه کنند. این قابلیت می تواند به تعیین اینکه اگر شکاف در کلینیک برنامه ریزی شده خیلی طولانی باشد یا اینکه بیمار می تواند با خیال راحت منتظر از سرگیری درمان بماند، باید بیمار را به کلینیک دیگری منتقل کرد یا خیر.

COVID-19 چگونه بر ارائه پرتودرمانی تأثیر گذاشته است؟
EQD2VH همچنین می تواند تغییرات در زمان کلی درمان و آسیب های کشنده را در بافت نرمال توضیح دهد، که یک سیستم تجاری ممکن است قادر به انجام آن نباشد. مهمتر از همه، این ابزار برای کارکرد نیازی به اتصال به شبکه بیمارستانی ندارد – حتی اگر سرورهای بیمارستان هنوز در اثر حمله سایبری فلج شده باشند، می توان از آن استفاده کرد.
ما هنوز در حال ارزیابی EQD هستیم2مارگارت مور، محقق اصلی از بیمارستان دانشگاه گالوی، می گوید VH به عنوان یک ابزار تصمیم گیری. این بخشی از یک پروژه فعلی است که بیمارانی را که چندین درمان مجدد دریافت میکنند برای رژیمهای تسکیندهنده که در آن دوز به ازای فراکسیون غیراستاندارد است و ممکن است انتخابی از طرحهای تقسیمبندی وجود داشته باشد، بررسی میکند. تبدیل دوز درمان از تعدادی درمان با تقسیم بندی های مختلف به EQD2 اجازه می دهد تا دوز رادیوبیولوژیکی برای بافت های هدف و OAR ها برای یک نمای کلی دوز جمع آوری شود، که می تواند به تصمیم گیری برای انتخاب درمان بیشتر کمک کند.