میکروسکوپ فلورسانس سلول های زنده ابزاری ضروری برای مطالعه دینامیک سیستم های بیولوژیکی فراهم می کند. اما بسیاری از فرآیندهای بیولوژیکی - مانند تقسیم سلولی باکتریایی و تقسیم میتوکندریایی، به عنوان مثال - به صورت پراکنده اتفاق میافتند و گرفتن آنها را دشوار میکند.
تصویربرداری مداوم از یک نمونه با نرخ فریم بالا تضمین میکند که وقتی چنین تقسیمبندیهایی اتفاق میافتد، قطعاً ثبت خواهند شد. اما تصویربرداری بیش از حد فلورسانس باعث سفید شدن نور می شود و می تواند نمونه های زنده را زودتر از موعد از بین ببرد. در همین حال، نرخ فریم پایینتر، خطر از دست دادن رویدادهای مورد علاقه را به همراه دارد. چیزی که نیاز است راهی برای پیش بینی زمان وقوع یک رویداد و سپس دستور دادن به میکروسکوپ برای شروع تصویربرداری با سرعت بالا است.
محققان موسسه فناوری فدرال سوئیس لوزان (EPFL) دقیقاً چنین سیستمی را ایجاد کرده اند. این تیم یک چارچوب اکتسابی مبتنی بر رویداد (EDA) ایجاد کرد که کنترل میکروسکوپ را برای تصویربرداری از رویدادهای بیولوژیکی با جزئیات در حالی که استرس روی نمونه را محدود میکند، خودکار میکند. EDA با استفاده از شبکه های عصبی برای شناسایی پیش سازهای ظریف رویدادهای مورد علاقه، پارامترهای اکتساب - مانند سرعت تصویربرداری یا مدت زمان اندازه گیری - را در پاسخ تطبیق می دهد.

یک میکروسکوپ هوشمند به نوعی مانند یک ماشین خودران است. محقق اصلی توضیح می دهد که باید انواع خاصی از اطلاعات، الگوهای ظریف را پردازش کند که سپس با تغییر رفتار خود به آنها پاسخ می دهد. سولیانا مانلی در بیانیه مطبوعاتی با استفاده از یک شبکه عصبی، میتوانیم رویدادهای بسیار ظریفتری را شناسایی کرده و از آنها برای ایجاد تغییرات در سرعت اکتساب استفاده کنیم.»
چارچوب EDA، شرح داده شده در روش های طبیعت، شامل یک حلقه بازخورد بین یک جریان تصویر زنده و کنترل های میکروسکوپ است. محققان از نرم افزار Micro-Manager برای گرفتن تصاویر از میکروسکوپ و یک شبکه عصبی آموزش دیده بر روی داده های برچسب دار برای تجزیه و تحلیل آنها استفاده کردند. برای هر تصویر، خروجی شبکه به عنوان یک پارامتر تصمیم گیری برای جابجایی بین تصویربرداری کند و سریع عمل می کند.
تشخیص رویداد
مانلی و همکارانش برای نشان دادن تکنیک جدید خود، EDA را در یک میکروسکوپ روشنایی ساختیافته فوری ادغام کردند و از آن برای ضبط فیلمهای تایم لپس با وضوح فوقالعاده تقسیمبندیهای میتوکندریایی و باکتریایی استفاده کردند.
تقسیم میتوکندری غیرقابل پیش بینی است و معمولاً هر چند دقیقه یک بار رخ می دهد و ده ها ثانیه طول می کشد. برای پیشبینی شروع تقسیم، تیم شبکه عصبی را برای تشخیص انقباضات، تغییر شکل میتوکندری که منجر به تقسیم میشود، همراه با حضور پروتئینی به نام DRP1 که برای تقسیمهای خود به خودی لازم است، آموزش دادند.
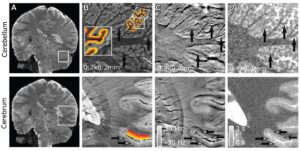
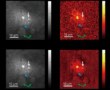
شبکه عصبی یک نقشه حرارتی از «نمرات رویداد» را با مقادیر بالاتر (زمانی که هم انقباضات و هم سطح DRP1 بالا هستند) خروجی میدهد که مکانهایی را در تصویر نشان میدهد که احتمال وقوع تقسیم در آنها بیشتر است. هنگامی که امتیاز رویداد از مقدار آستانه فراتر رفت، سرعت تصویربرداری برای ثبت جزئیات رویدادهای تقسیم افزایش می یابد. هنگامی که امتیاز به آستانه دوم کاهش یافت، میکروسکوپ برای جلوگیری از قرار گرفتن نمونه در معرض نور بیش از حد، به تصویربرداری با سرعت پایین تغییر می کند.
محققان EDA را روی سلولهایی انجام دادند که برچسبهای فلورسنت هدفمند میتوکندری را بیان میکردند. در طول هر اندازه گیری EDA، شبکه به طور متوسط 0.2 بار پیش سازهای تقسیم باکتریایی را تشخیص داد. این کار سرعت تصویربرداری را از آهسته (3.8 فریم در ثانیه) به سریع (10 فریم در ثانیه) برای میانگین 18 ثانیه تغییر داد و در نتیجه 1٪ فریم ها تصویربرداری سریع داشت. آنها اشاره می کنند که بسیاری از سایت ها DRPXNUMX را جمع آوری کردند اما منجر به تقسیم نشدند. این سایتها شبکه را راهاندازی نکردند، و توانایی آن را در تشخیص رویدادهای مورد علاقه نشان دادند.
برای مقایسه، تیم همچنین تصاویر را با سرعت ثابت و سریع جمع آوری کرد. EDA نسبت به تصویربرداری سریع با نرخ ثابت، نور سفید کردن نمونه کمتری را ایجاد کرد، که مشاهدات طولانیتر از هر نمونه را امکانپذیر کرد و شانس ثبت رویدادهای نادر تقسیم میتوکندری را افزایش داد. در برخی موارد، نمونه در طی مراحل تصویربرداری آهسته پس از فوتوبلیچینگ بهبود یافت و دوز تجمعی نور بیشتری را ممکن ساخت.
در حالی که بلیچینگ با EDA بیشتر از تصویربرداری آهسته ثابت بود، بسیاری از جلسات EDA بدون کاهش سلامت نمونه به 10 دقیقه رسیدند. محققان همچنین دریافتند که EDA انقباضات قبل از تقسیم و همچنین پیشرفت حالات غشایی که منجر به شکافت میشود را بهتر حل میکند، همانطور که توسط انفجار تصاویر سریع ثبت میشود.
مانلی توضیح میدهد: «پتانسیل میکروسکوپ هوشمند شامل اندازهگیری مواردی است که اکتسابهای استاندارد از دست میدهند. ما رویدادهای بیشتری را ثبت میکنیم، انقباضات کوچکتر را اندازهگیری میکنیم و میتوانیم هر بخش را با جزئیات بیشتری دنبال کنیم.»
تشخیص تقسیم باکتریایی
سپس، محققان از EDA برای مطالعه تقسیم سلولی در باکتری ها استفاده کردند C. crescentus. چرخه سلولی باکتری در مقیاس زمانی دهها دقیقه اتفاق میافتد و چالشهای مشخصی را برای میکروسکوپ سلول زنده ایجاد میکند. آنها داده ها را با سرعت تصویربرداری آهسته 6.7 فریم در ساعت، سرعت تصویربرداری سریع 20 فریم در ساعت یا با سرعت متغیر توسط EDA جمع آوری کردند.
این تیم متوجه شد که شبکه تشخیص رویداد توسعه یافته برای انقباضات میتوکندری می تواند مراحل نهایی تقسیم باکتری را بدون آموزش اضافی تشخیص دهد - احتمالاً به دلیل شباهت ها در شکل انقباض و وجود یک نشانگر مولکولی مشابه عملکردی.
تکنیک میکروسکوپی بهبودیافته سلول های زنده را با حساسیت هفت برابر بیشتر می بیند
مجدداً، EDA در مقایسه با تصویربرداری سریع ثابت، فتوبلیچینگ را کاهش داد و انقباضات را با قطر متوسط به طور قابل توجهی کمتر از تصویربرداری آهسته ثابت اندازهگیری کرد. EDA تصویربرداری از کل چرخه سلولی را فعال کرد و جزئیاتی از تقسیم سلولی باکتریایی ارائه کرد که به سختی می توان با استفاده از سرعت تصویربرداری ثابت عکسبرداری کرد..
مانلی می گوید دنیای فیزیک این تیم همچنین قصد دارد شبکه های عصبی را برای شناسایی انواع مختلف رویدادها آموزش دهد و از آنها برای برانگیختن پاسخ های سخت افزاری مختلف استفاده کند. او توضیح می دهد: «به عنوان مثال، ما استفاده از اغتشاشات اپتوژنتیک را برای تعدیل رونویسی در لحظات کلیدی تمایز سلولی تصور می کنیم. ما همچنین به استفاده از تشخیص رویداد به عنوان ابزاری برای فشردهسازی دادهها، انتخاب برای ذخیره یا تجزیه و تحلیل دادههایی که بیشترین ارتباط را با یک مطالعه خاص دارند، میاندیشیم.»
- برای اینکه محققان بتوانند EDA را بر روی طیف گسترده ای از میکروسکوپ ها پیاده سازی کنند، این تیم چارچوب کنترلی را به عنوان یک افزونه منبع باز برای نرم افزار Micro-Manager