ایمونوتراپی - استفاده از سیستم ایمنی بدن برای مبارزه با سرطان - این پتانسیل را دارد که مراقبت از سرطان را متحول کند. اما در حالی که سرطان های خون مانند لوسمی و لنفوم به خوبی به ایمونوتراپی سرطان پاسخ می دهند، تومورهای جامد پاسخ محدودی نشان می دهند.
یکی از دلایل احتمالی این تفاوت، بیان متنوع پروتئین های سطحی در سرطان های مختلف است. به عنوان مثال، پروتئین متصل به غشاء SLAMF7 - که سیستم ایمنی را فعال می کند و باعث فاگوسیتوز (بلع) سلول های سرطانی توسط سلول های ایمنی می شود - توسط سلول های سرطانی خون بیان می شود، اما نه توسط تومورهای جامد.
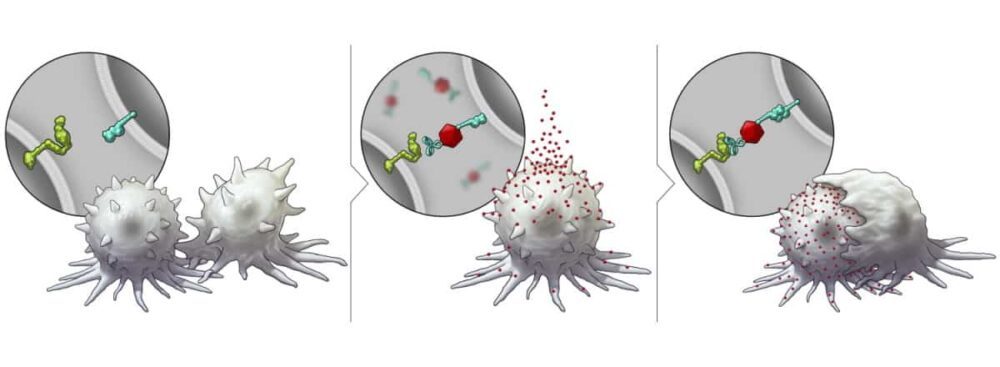
محققان با هدف پذیرش سلولهای تومور جامد برای ایمونوتراپی دانشگاه تگزاس MD Anderson Cancer Center یک پلت فرم نانوتکنولوژی توسعه داده اند که بیان SLAMF7 خود را تحریک می کند. شرح داده شده در نانوتکنولوژی طبیعتاین پلت فرم مبتنی بر نانوذرات تبدیلکننده تومور دوگانه (BiTNs) است که از یک هسته پلیمری کونژوگه با لیگاندهای هدفگیری تومور و SLAMF7 تشکیل شده است.
میگوید: «با این پلتفرم جدید، ما اکنون یک استراتژی برای تبدیل یک تومور جامد، حداقل از نظر ایمونولوژیکی، شبیه به یک تومور هماتولوژیک داریم، که اغلب نرخ پاسخ بسیار بالاتری به درمانهای ایمونوتراپی دارد.» ون جیانگ، که این مطالعه را همراه با بتی کیم. اگر بتوانیم این رویکرد را در کلینیک ترجمه و تأیید کنیم، ممکن است ما را قادر سازد تا به حداکثر سطح فعالیت داروهای ایمونوتراپی با سرطانهایی که بهطور سنتی به خوبی پاسخ نمیدهند نزدیکتر شویم.»
در شرایط آزمایشگاهی و در داخل بدن ارزیابی
محققان ابتدا این پلت فرم را بررسی کردند در شرایط in vitroبا استفاده از سلول های سرطان سینه HER2 مثبت. آنها BiTN های اختصاصی سلولی را برای این کاربرد با کونژوگه کردن نانوذرات با آنتی بادی های ضد HER2 برای اتصال به سلول های تومور و SLAMF7 برای فعال کردن پاسخ ایمنی ایجاد کردند. نانو مزدوج حاصل – BiTNاو - به طور انتخابی سلول های سرطان سینه HER2 مثبت را هدف قرار داده و آنها را با SLAMF7 برچسب گذاری کرده است.
تیم تایید کرد که BiTNاوسلولهای سرطانی برچسبگذاریشده سطح بالاتری از فاگوسیتوز را در مقایسه با نانوذرات غیرکونژوگه ایجاد کردند. BiTNاو همچنین سلولهای سرطان سینه را به درمان با آنتیبادی ضد CD47 حساس کرد، که سیگنال «مرا نخور» را از سلولهای تومور مسدود میکند و فعالیت فاگوسیتی را بیشتر میکند.
سپس، تیم BiTN را ارزیابی کرداو در موشهای مبتلا به تومورهای سرطان سینه از سلولهای TUBO، که نسخه جونده HER2 را بیان میکنند، یا سلولهای 4T1 که فاقد این گیرنده هستند. درمان با BiTNاو به علاوه anti-CD47 به طور قابل توجهی بار تومور را کاهش داد و بقای موش های مبتلا به تومورهای TUBO را طولانی کرد. اثر ضد توموری در تومورهای 4T1 مشاهده نشد.
محققان خاطرنشان کردند که درمان ترکیبی در مقایسه با BiTN ها یا ضد CD47 به تنهایی منجر به مهار تومور قابل توجهی شد. یک مطالعه سمیت طولانی مدت تفاوت معنی داری را در شمارش خون بین موش های درمان نشده و تحت درمان نشان نداد.
برای نشان دادن تطبیق پذیری پلت فرم BiTN، محققان نانوذرات را سفارشی کردند تا گیرنده تومور دیگری را هدف قرار دهند - گیرنده فولات که با سرطان سینه سه گانه منفی بیان می شود. آنها BiTN را ایجاد کردندFo با جایگزینی آنتی بادی ضد HER2 با فولات. BiTNFo سلول های سرطانی را هدف قرار داده و به سلول های بیان کننده SLAMF7 تبدیل می کند. همانطور که انتظار می رفت، انکوباسیون سلول های 4T1 با BiTNFo و anti-CD47 منجر به فاگوسیتوز بیشتر نسبت به سلولهای TUBO شد.
کیم در بیانیهای مطبوعاتی میگوید: «از آنجایی که این سازههای مهندسی شدهاند، میتوان از آن بهعنوان یک رویکرد plug-and-play برای ترکیب عوامل مختلف هدفگیری تومور یا مولکولهای ایمنی بر روی سطح نانوذره استفاده کرد.»
محققان همچنین BiTN را آزمایش کردندFo در یک مدل موش متاستاز خودبخودی 4T1، درمان تومورهای اولیه با BiTNFo و ضد CD47 قبل از عمل جراحی. این ترکیب از عود بیماری موضعی جلوگیری کرد اما متاستازهای دور را کاهش نداد یا بقای کلی را طولانی کرد. با این حال، افزودن anti-PD1 به درمان منجر به مهار متاستاز طولانیمدت شد و دو موش از هفت موش زنده ماندن طولانیمدت بدون تومور را نشان دادند.
ایمونوتراپی به همراه پرتوهای انفجاری تومورهای مغزی در موش ها را درمان می کند
در نهایت، برای تقویت بیشتر ارتباط ترجمه ای این مدل، تیم یک رژیم درمانی پس از جراحی را بررسی کرد. در اینجا، تومورهای موش در روز 12 بدون هیچ گونه پیش درمانی برداشته شدند و سپس از روز 15، حیوانات با ترکیب سه گانه BiTN تحت درمان قرار گرفتند.Fo, anti-CD47 و anti-PD1. این درمان بعد از عمل متاستاز و بقای طولانی مدت را مهار می کند - که نشان می دهد حتی بدون درمان داخل توموری، BiTNs می تواند به حذف سلول های تومور باقیمانده و کاهش بیماری سیستمیک کمک کند.
در مرحله بعد، محققان بر روی ترجمه این فناوری جدید به کلینیک تمرکز می کنند. جیانگ میگوید: «برای آسانتر کردن ترجمه بالینی، ما در حال بررسی یک استراتژی مبتنی بر پروتئین هستیم که در آن یک پروتئین دوتخصصی ایجاد میکنیم که میتواند مانند BiTN عمل کند. دنیای فیزیک. "این به مهندسی پروتئین/آنتی بادی نیاز دارد، اما به احتمال زیاد برآوردن تاییدیه های نظارتی آسان تر خواهد بود."