تومورها را می توان به روش های مختلفی از بین برد. رادیوتراپی از پرتوهای پرتوهای یونیزان برای آسیب رساندن به DNA و تخریب سلول های تومور استفاده می کند. یک رویکرد کمتر رایج، درمان فتودینامیک است که از یک داروی فعال شده با نور برای کشتن سلول های سرطانی از طریق آسیب میتوکندری استفاده می کند. سپس تکنیک نوظهور درمان رادیودینامیک (RDT) وجود دارد.
توضیح داد: «رادیودینامیک درمانی ترکیبی از رادیوتراپی به همراه فتودینامیک درمانی است چارلی ما از مرکز سرطان فاکس چیس، در سخنرانی اخیر نشست سالانه AAPM.
درمان فوتودینامیک معمولاً از نور لیزر مرئی برای فعال کردن یک داروی حساس به نور استفاده میکند که ترجیحاً در سلولهای تومور قرار دارد. داروی فعال شده اکسیژن منفرد بسیار سیتوتوکسیک تولید می کند که باعث مرگ سلولی می شود. با این حال، نفوذ محدود نور لیزر به بافت به این معنی است که این روش عمدتاً برای درمان تومورهای سطحی یا مکانهایی با دسترسی آندوسکوپی استفاده میشود. برای درمان تومورهای عمیق که درمان فتودینامیک نمی تواند به آنها برسد، RDT از پرتوهای فوتون با انرژی بالا برای فعال کردن حساس کننده نور استفاده می کند.
Ma توضیح داد: «در RDT، ما از 20 تا 30 درصد دوز رادیوتراپی استفاده می کنیم. و سپس از نور چرنکوف نیز استفاده می کنیم. وی خاطرنشان کرد که این اشعه چرنکوف که در طول رادیوتراپی به دلیل تعامل پرتو درمانی با بافت بیمار تولید می شود، توزیع نور تقریباً یکسانی با توزیع دوز پرتو درمانی خواهد داشت و بنابراین می توان به راحتی برنامه ریزی کرد.
دارو علاوه بر تجمع در تومور اولیه، توسط سلولهای متاستاتیک توزیع شده نیز جذب میشود که میتوانند با استفاده از دوز بسیار کم نور چرنکوف از بین بروند. ما گفت: «اکنون برای اولین بار، RDT رادیوتراپی را نه تنها موضعی و منطقهای، بلکه یک روش درمانی سیستمیک میسازد.
تیم Fox Chase از دارویی به نام اسید 5-aminolevulinic (5-ALA) برای RDT استفاده می کند. 5-ALA توسط میتوکندری در سلول های سرطانی جذب می شود و در تومورها 10 تا 20 برابر بیشتر از بافت های طبیعی جذب می شود. هنگامی که 5-ALA وارد سلول سرطانی می شود، به پروتوپورفیرین IX (PpIX)، یک حساس کننده نور با حداکثر طیف جذبی در حدود 380-430 نانومتر متابولیزه می شود. این برای نور لیزر قرمز که اغلب برای درمان فوتودینامیک استفاده می شود ایده آل نیست. با این حال، برای پیک جذب چرنکوف در 370 تا 430 نانومتر یک تطابق عالی است.
اثبات پیش بالینی
در چند سال گذشته، ما و تیمش مطالعات پیش بالینی زیادی را با استفاده از خطوط سلولی مختلف تومور و انرژیهای تابشی مختلف انجام دادهاند. او برخی از نتایج یک مطالعه بزرگ (چند صد حیوان) را به اشتراک گذاشت که RDT موش های حامل تومور را با استفاده از 100 میلی گرم بر کیلوگرم 5-ALA و تابش فوتون 6، 15 یا 45 MV ارزیابی کرد.
Ma خاطرنشان کرد که تومور بسیار تهاجمی است، با 4 گری پرتودرمانی به تنهایی تنها حدود 10 درصد از سلول های تومور را از بین می برد. علاوه بر این، RDT در 6 MV اثر درمانی را به طور قابل توجهی افزایش نداد. او خاطرنشان کرد: "به همین دلیل است که مردم نگران این بودند که نور چرنکوف کافی نیست." اما با 15 و 45 MV، تاخیر رشد تومور به مراتب بیشتری را مشاهده می کنید. ما هنوز در حال مطالعه هستیم که چرا این تغییر چشمگیر به دلیل انرژی وجود دارد، ما باید مکانیسم دقیق پشت آن را پیدا کنیم.
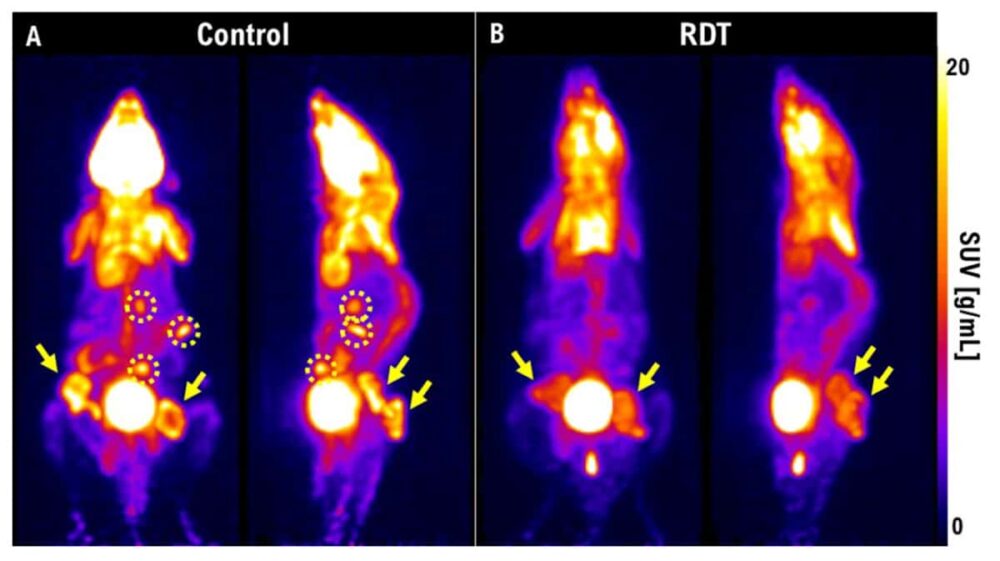
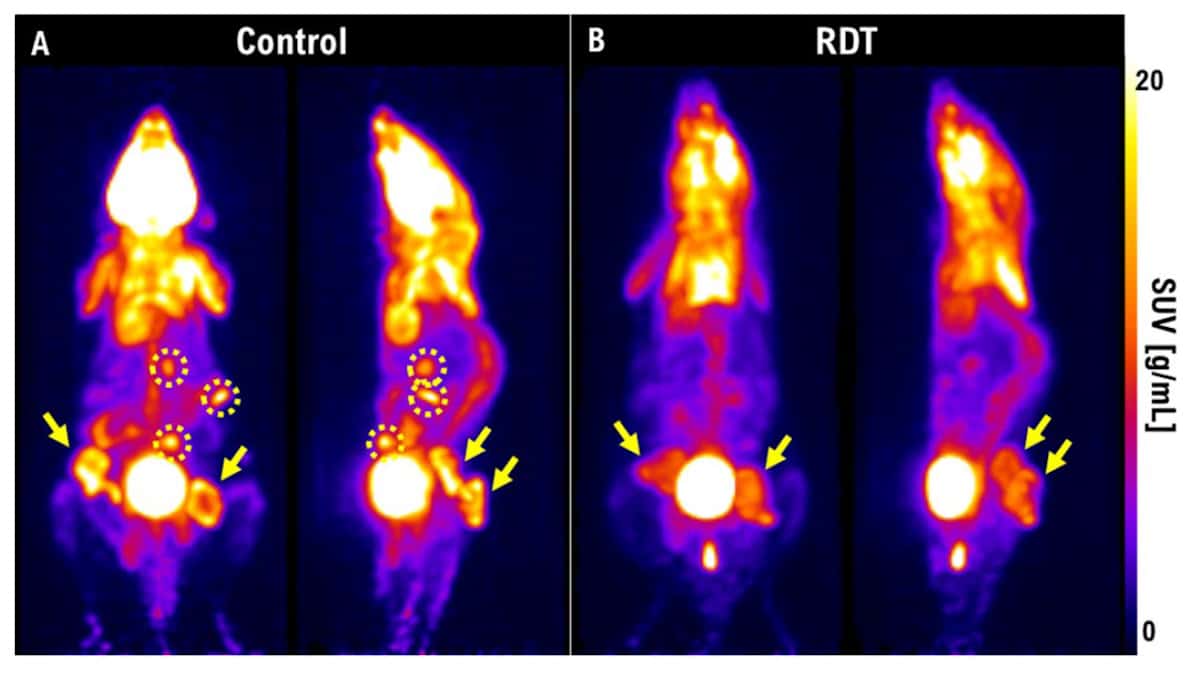
این تیم از PET برای تجسم کوچک شدن تومور پس از RDT استفاده کردند. یک هفته پس از درمان، تومورها در موشهای کنترل رشد کرده و متاستاز داده بودند، در حالی که آنهایی که تحت درمان با RDT قرار گرفتند، ضایعات بسیار کوچکتری داشتند و متاستاز نداشتند. ما همچنین مطالعه ای را در مورد سرطان تیروئید بسیار تهاجمی در خرگوش توضیح داد. یک هفته پس از 3 گری رادیوتراپی، تومور همچنان در حال رشد بود. اما اگر از RDT در 3 گری با 5-ALA استفاده کنیم، تومور در تصاویر PET دیده نمی شود. او تاکید کرد که PET یک راه عالی برای انجام ارزیابی اولیه درمان است و می تواند به تعیین اینکه آیا RDT در بیمار موثر است یا خیر کمک می کند.
فاکس چیس اکنون در حال انجام یک کارآزمایی بالینی بر روی RDT است، با فاز اول مطالعه که افزایش دوز (هم دوز پرتو و هم دوز دارو) را در تومورهای مرحله آخر بررسی میکند. ما با اشاره به اینکه تاکنون در هیچ موردی سمیتی رخ نداده است، گفت: این مرحله اکنون به سطح دوز نهایی رسیده است و تنها سه بیمار باقی مانده اند. در جای دیگر، دومین کارآزمایی RDT در بیمارستان دانشگاهی مونستر، بیمارانی را با اولین عود گلیوبلاستوما بررسی می کند.
موارد واقعی
در نهایت، ما نتایجی را از تعدادی از موارد واقعی ارائه کرد. او به حضار گفت: "شما از دیدن اینها هیجان زده خواهید شد" و خاطرنشان کرد که "معمولاً مردم باور نمی کنند که کار کند مگر اینکه یک ماه تصویربرداری با CT، MR یا PET داشته باشید."
در مثال اول، درمان متاستازهای کبدی، او نشان داد که یک ماه پس از RDT، تصویربرداری PET نشان داد که هیچ توموری باقی نمانده است. وی در ادامه یک مورد سرطان ریه با متاستاز را ارائه کرد: "شما می توانید نتایج بسیار چشمگیری را با تومورهای غیرفعال شده پس از RDT مشاهده کنید."
دستگاه قابل کاشت درمان فتودینامیک شخصی را ارائه می دهد
سایر درمانهای موفق RDT شامل سرطان مری، تومور ریه با متاستازهای متعدد استخوانی و بیماری که شیمیدرمانی شکست خورده بود اما سه روز پس از RDT پاسخ خوبی داشت. ما خاطرنشان کرد که اکثر بیماران سرطان در مراحل آخر داشتند و سایر درمانها ناموفق بودند. او افزود: "ما تاثیری را می بینیم، بنابراین امیدواریم بتوانیم بقای آنها را بهبود بخشیم."
Ma نتیجه گیری کرد: «RDT می تواند یک درمان موضعی، منطقه ای و سیستمیک باشد که رادیوتراپی و فتودینامیک درمانی را ترکیب می کند. "ما تعداد زیادی داریم در شرایط in vitro و در داخل بدن آزمایشهایی برای نشان دادن پتانسیل درمانی آن انجام میشود، و اگرچه آزمایشهای بالینی کم است، امیدوارم در آینده نتایج بیشتری داشته باشیم و این را به چیزی واقعا مفید تبدیل کنیم.»
- محتوای مبتنی بر SEO و توزیع روابط عمومی. امروز تقویت شوید.
- PlatoData.Network Vertical Generative Ai. به خودت قدرت بده دسترسی به اینجا.
- PlatoAiStream. هوش وب 3 دانش تقویت شده دسترسی به اینجا.
- PlatoESG. خودرو / خودروهای الکتریکی، کربن ، CleanTech، انرژی، محیط، خورشیدی، مدیریت پسماند دسترسی به اینجا.
- BlockOffsets. نوسازی مالکیت افست زیست محیطی. دسترسی به اینجا.
- منبع: https://physicsworld.com/a/radiodynamic-therapy-harnessing-light-to-improve-cancer-treatments/
- : دارد
- :است
- :نه
- $UP
- 10
- 100
- ٪۱۰۰
- 20
- 30
- a
- درباره ما
- دسترسی
- اضافه
- اضافه
- پس از
- مهاجم
- AL
- تنها
- همچنین
- هر چند
- an
- و
- حیوانات
- سالیانه
- هر
- روش
- هستند
- دور و بر
- AS
- ارزیابی
- At
- حضار
- BE
- پرتو
- پشت سر
- باور
- استخوان
- هر دو
- اما
- by
- نام
- CAN
- سرطان
- سلول های سرطانی
- نمی توان
- مورد
- موارد
- علل
- سلول ها
- مرکز
- تغییر دادن
- تعقیب
- محافل
- کلیک
- بالینی
- آزمایش های بالینی
- ترکیب
- ترکیب
- مشترک
- به این نتیجه رسیدند
- کنترل
- میتوانست
- روز
- مرگ
- تاخیر
- ارائه
- نشان دادن
- شرح داده شده
- از بین بردن
- نابود شده
- مشخص کردن
- دستگاه
- DID
- مختلف
- توزیع شده
- توزیع
- DNA
- do
- آیا
- نمایشی
- دارو
- دو
- در طی
- در اوایل
- به آسانی
- اثر
- موثر
- در جای دیگر
- سنگ سنباده
- تاکید
- انرژی
- تشدید
- ارزیابی
- در حال بررسی
- مثال
- عالی
- برانگیخته
- آزمایش
- توضیح داده شده
- ناموفق
- بسیار
- کمی از
- نهایی
- پیدا کردن
- نام خانوادگی
- بار اول
- پیروی
- برای
- روباه
- از جانب
- آینده
- تولید
- تولید می کند
- خوب
- بزرگ
- بیشتر
- در حال رشد
- رشد کرد
- رشد
- بود
- بهره برداری
- آیا
- he
- کمک
- خیلی
- خود را
- امید
- خوشبختانه
- اما
- HTTPS
- صد
- i
- دلخواه
- یکسان
- if
- تصویر
- تصاویر
- تصویربرداری
- بهبود
- in
- مشمول
- افزایش
- نشان دادن
- اطلاعات
- داخل
- در ارتباط بودن
- به
- موضوع
- IT
- ITS
- JPG
- تنها
- کشتن
- بزرگ
- لیزر
- نام
- ترک کرد
- کمتر
- سطح
- سبک
- محدود شده
- خطوط
- کبد
- محلی
- خیلی
- کم
- عمدتا
- ساخت
- باعث می شود
- بسیاری
- مسابقه
- حداکثر عرض
- به معنی
- مکانیزم
- میتوکندری
- ماه
- بیش
- اکثر
- mr
- بسیار
- چندگانه
- نیاز
- بعد
- نه
- طبیعی
- اشاره کرد
- یادداشت برداری
- اکنون
- عدد
- رخ داده است
- of
- غالبا
- on
- یک بار
- ONE
- فقط
- باز کن
- or
- دیگر
- خارج
- اکسیژن
- بیمار
- pacientes
- اوج
- نفوذ
- مردم
- برای
- انجام
- انجام
- انجام
- شخصی
- فاز
- فیزیک
- دنیای فیزیک
- برنامه ریزی
- افلاطون
- هوش داده افلاطون
- PlatoData
- به علاوه
- پتانسیل
- ارائه شده
- اصلی
- فراهم می کند
- رادیوتراپی
- رسیدن به
- رسیده
- واقعا
- اخیر
- عود
- قرمز
- منطقهای
- باقی مانده است
- پاسخ
- نتایج
- نشان داد
- سعید
- دوم
- دیدن
- مشاهده گردید
- چند
- به اشتراک گذاشته شده
- نشان داد
- به طور قابل توجهی
- سایت
- کوچکتر
- So
- تا حالا
- برخی از
- چیزی
- صحبت کردن
- طیف
- هنوز
- مطالعات
- مهاجرت تحصیلی
- در حال مطالعه
- موفق
- کافی
- بقاء
- سیستمیک
- صورت گرفته
- تیم
- نسبت به
- که
- La
- آینده
- شان
- سپس
- آنجا.
- اینها
- این
- کسانی که
- سه
- کوچک
- بدین ترتیب
- زمان
- بار
- به
- درمان
- رفتار
- محاکمه
- آزمایش های
- درست
- به طور معمول
- دانشگاه
- استفاده کنید
- استفاده
- استفاده
- با استفاده از
- مختلف
- بسیار
- از طريق
- قابل رویت
- بود
- مسیر..
- راه
- we
- هفته
- چه
- که
- در حین
- چرا
- اراده
- با
- در داخل
- با این نسخهها کار
- جهان
- نگران
- خواهد بود
- سال
- شما
- زفیرنت