ارتشی از ذرات خودکششی و پوشیده از رادیو ایزوتوپ را تصور کنید که 2500 تا 10,000 برابر کوچکتر از یک ذره گرد و غبار است که پس از تزریق به بدن، تومورهای سرطانی را جستجو کرده و به آنها می چسبند و آنها را از بین می برند. به نظر می رسد علمی تخیلی؟ برای موش های مبتلا به سرطان مثانه اینطور نیست.
محققان اسپانیایی گزارش کردند که نانوذرات حاوی ید رادیواکتیو که در واکنش با اوره به حرکت در میآیند، توانایی تشخیص تومورهای سرطانی مثانه را از بافت سالم دارند. این نانورباتها به ماتریکس خارج سلولی تومور نفوذ میکنند و در داخل آن تجمع مییابند و درمان رادیونوکلئید را قادر میسازند تا به هدف دقیق خود برسد. در مطالعه ای که در موسسه مهندسی زیستی کاتالونیا (IBEC) در بارسلونا، موشهایی که یک دوز از این درمان را دریافت کردند، در مقایسه با حیوانات درماننشده، 90 درصد کاهش اندازه تومورهای مثانه داشتند.
این رویکرد جدید ممکن است روزی انقلابی در درمان سرطان مثانه ایجاد کند. بر اساس گزارش رصدخانه جهانی سرطان سازمان جهانی بهداشت، سرطان مثانه دهمین سرطان شایع در جهان است، با بیش از 600,000 مورد جدید در سال 2022 تشخیص داده شده و بیش از 220,000 مرگ در سراسر جهان.
سرطان مثانه غیر تهاجمی عضلانی که 75 درصد موارد را تشکیل می دهد، در حال حاضر با برداشتن تومور و سپس تزریق داخل مثانه داروهای شیمی درمانی یا ایمونوتراپی به مثانه درمان می شود. با این حال، تحویل دارو به ویژه به دلیل نفوذپذیری کم یوروتلیوم (بافت پوشاننده داخل مجرای ادرار)، پر شدن محتوای ادرار و شستشوی بعدی داروها چالش برانگیز است. این فرآیند همچنین برای بیماران ناراحت کننده است، زیرا آنها باید در فواصل زمانی که دراز کشیده اند بدن خود را بچرخانند تا داروها بتوانند به همه طرف دیواره مثانه برسند. پس از درمان، 30 تا 70 درصد خطر عود در طی پنج سال وجود دارد.
برای بهبود نتایج بالینی، محقق اصلی ساموئل سانچز و همکارانش قصد دارند درمانهای نوآورانه و مؤثرتری برای سرطان مثانه ایجاد کنند و در این فرآیند، میزان عود را کاهش دهند. علاوه بر این، یک درمان با یک دوز به طور قابل توجهی هزینه درمان را کاهش می دهد، که در حال حاضر بین 14 تا XNUMX بستری شدن در بیمارستان نیاز دارد.
این تیم نانورباتهایی را از نانوذرات سیلیکا مزو متخلخل با اجزای عملکردی مختلف بر روی سطوح خود ساختند. اینها شامل رادیو ایزوتوپها برای تجسم PET یا درمان رادیونوکلئید و پروتئین اوره آز است که با اوره در ادرار واکنش میدهد و حرکت نانوربات را قادر میسازد.
نوشتن در نانوتکنولوژی طبیعتمحققان گزارش کردند که وقتی قطرهای از نانورباتها را به محلولی حاوی 300 میلیمولار اوره اضافه کردند، نانورباتها حرکتی ازدحام نشان دادند و جبهههای فعال و شدید و گردابهای سهبعدی تشکیل دادند. بدون اوره، نانورباتها به سادگی در نزدیکی محل افزودن رسوب کردند.
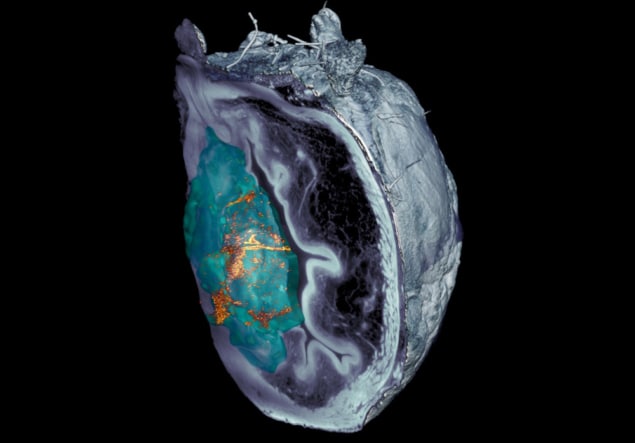
برای بررسی اینکه آیا نانوربات ها می توانند به تومور برسند یا خیر در داخل بدن، این تیم رفتار آنها را در موش های حامل تومور ارزیابی کردند. تصاویر توموگرافی گسیل پوزیترون (PET) نشان داد که سیگنالهای نانورباتهای نشاندار شده با رادیواکتیو با موقعیت تومور، همانطور که از طریق MRI تعیین میشود، با رادیواکتیویته عمدتاً در محل تومور هدف دیده میشوند. تنها موشهایی که با نانورباتها به همراه اوره تزریق شده بودند، تجمع قابلتوجهی در توده تومور نشان دادند - نانورباتهای تحویلشده در آب، و نانوذرات کنترل (بدون اوره آز) تحویلشده در آب یا اوره، حداقل جذب تومور را نشان دادند.
محققان پیشنهاد می کنند که تحرک نانوربات ها به آنها کمک می کند تا به توده تومور نفوذ کنند. نویسنده اول توضیح میدهد: «نانورباتها فاقد آنتیبادیهای خاص برای تشخیص تومور هستند و بافت تومور معمولاً سفتتر از بافت سالم است، اما در تومورهای مثانه اینطور نیست». Meritxell Serra Casablancas از IBEC ما مشاهده کردیم که این نانوروبات ها می توانند ماتریکس خارج سلولی تومور را با افزایش محلی pH از طریق یک واکنش شیمیایی خودکششی تجزیه کنند. این پدیده باعث نفوذ بیشتر تومور شد. محققان بر این باورند که نانورباتها با یوروتلیوم مانند یک دیوار برخورد میکنند، اما به توموری که اسفنجیتر است نفوذ میکنند.
این تیم خاطرنشان کرد که شناسایی نانوربات ها در تصاویر میکروسکوپی بافت تشریح شده چالش برانگیز بود. پس از شکست تکنیک های میکروسکوپ نوری کانفوکال، محققان در IRB بارسلونا یک سیستم میکروسکوپی مبتنی بر ورقه نور، بر اساس نور لیزر مسطح، ایجاد کرد که قادر به اسکن لایههای مختلف مثانه و ایجاد یک بازسازی سه بعدی از کل اندام است.
میگوید: «سیستم میکروسکوپ ورقه نوری الاستیک پراکندهای که ما ایجاد کردیم به ما امکان میدهد نور منعکسشده توسط خود تومور را حذف کنیم و به ما امکان میدهد نانوذرات را در سرتاسر اندام بدون برچسبگذاری قبلی، با وضوح بیسابقه شناسایی و مکانیابی کنیم.» جولین کلمبلی از IRB بارسلونا.

باکتری های مهندسی شده رادیوایزوتوپ های کشنده سرطان را به داخل تومورها جذب می کنند
برای ارزیابی اثر درمانی این روش، تیم نانورباتها را با ید-131 برچسبگذاری کردند.131I، یک رادیوایزوتوپ که معمولاً برای درمان رادیونوکلئید استفاده می شود)، و آنها را به موش های حامل تومور تزریق کردم. درمان با از دست دادن دوز 131I-nanobots موجود در اوره رشد تومور را متوقف می کند، در حالی که دوز بالایی دارد 131I-nanobots تجویز شده در اوره منجر به کاهش تقریباً 90 درصدی حجم تومور در مقایسه با حیوانات بدون درمان شد.
سانچز می گوید دنیای فیزیک گامهای بعدی این تیم عبارت است از کپسولهسازی داروهای کوچکی که در حال حاضر در شیمیدرمانی استفاده میشوند و همچنان به آزمایش کارایی نانورباتها به عنوان حاملهای دارو ادامه میدهند. آنها در نهایت قصد دارند نانوربات ها را بزرگ کنند و مسیرهای نظارتی را برای حرکت به سمت اولین آزمایشات بالینی در سه تا چهار سال آینده، از طریق اسپین آف IBEC مطالعه کنند. نانوربات های درمانی.
- محتوای مبتنی بر SEO و توزیع روابط عمومی. امروز تقویت شوید.
- PlatoData.Network Vertical Generative Ai. به خودت قدرت بده دسترسی به اینجا.
- PlatoAiStream. هوش وب 3 دانش تقویت شده دسترسی به اینجا.
- PlatoESG. کربن ، CleanTech، انرژی، محیط، خورشیدی، مدیریت پسماند دسترسی به اینجا.
- PlatoHealth. هوش بیوتکنولوژی و آزمایشات بالینی. دسترسی به اینجا.
- منبع: https://physicsworld.com/a/self-propelling-nanobots-shrink-bladder-tumours-in-mice-by-90/
- :است
- :نه
- $UP
- 000
- 10
- 135
- 14
- 2022
- 220
- 300
- 3d
- 600
- a
- توانایی
- مطابق
- حساب ها
- انباشتن
- تجمع
- فعال
- اضافه
- اضافه
- علاوه بر این
- اداره
- پس از
- هدف
- معرفی
- اجازه دادن
- همچنین
- an
- و
- حیوانات
- روش
- هستند
- ارتش
- بازداشت شد
- AS
- ارزیابی
- At
- ضمیمه کردن
- جذب
- نویسنده
- باکتری
- بارسلونا
- مستقر
- رفتار
- باور
- میان
- بدن
- بدن
- شکستن
- اما
- by
- CAN
- سرطان
- توانا
- حامل
- مورد
- موارد
- به چالش کشیدن
- شیمیایی
- بالینی
- آزمایش های بالینی
- همکاران
- برخورد
- COM
- مشترک
- عموما
- مقایسه
- اجزاء
- انجام
- محتوا
- ادامه دادن
- کنترل
- هزینه
- ایجاد شده
- ایجاد
- در حال حاضر
- روز
- مرگ و میر
- تحویل داده
- تحویل
- مشخص
- توسعه
- توسعه
- مختلف
- تمیز دادن
- مقدار
- پایین
- دارو
- مواد مخدر
- دو
- گرد و خاک
- اثر
- موثر
- بهره وری
- از بین بردن
- نشر
- قادر ساختن
- فعال
- را قادر می سازد
- را قادر می سازد
- تمام
- EU
- ارزیابی
- در نهایت
- معاینه کردن
- به نمایش گذاشته
- توضیح می دهد
- ناموفق
- داستان
- پر كردن
- نام خانوادگی
- پنج
- به دنبال
- پیروی
- برای
- چهار
- از جانب
- تابعی
- جهانی
- در سطح جهانی
- بیشتر
- رشد
- بود
- آیا
- سلامتی
- سالم
- کمک می کند
- اما
- HTTPS
- شناسایی
- شناسایی
- if
- تصاویر
- ایمن درمانی
- بهبود
- in
- شامل
- افزایش
- اطلاعات
- ابتکاری
- داخل
- قصد
- به
- موضوع
- IT
- ITS
- خود
- JPG
- برچسب زدن
- عدم
- لیزر
- لایه
- رهبری
- سبک
- پسندیدن
- پوشش دادن
- به صورت محلی
- کم
- توده
- ماتریس
- حداکثر عرض
- ممکن است..
- میکروسکوپ
- حداقل
- تحرک
- بیش
- اکثر
- حرکت
- حرکت
- MRI
- طبیعت
- نزدیک
- تقریبا
- نیاز
- جدید
- بعد
- توجه داشته باشید
- رمان
- رصد خانه
- of
- on
- ONE
- فقط
- or
- نتایج
- روی
- ویژه
- مسیرها
- pacientes
- نفوذ
- پدیده
- فیزیک
- دنیای فیزیک
- افلاطون
- هوش داده افلاطون
- PlatoData
- به علاوه
- موقعیت
- دقیق
- در درجه اول
- اصلی
- قبلا
- روند
- پروانه
- نیروی محرکه
- پروتئين
- نرخ
- رسیدن به
- واکنش
- واکنش نشان می دهد
- دریافت
- تشخیص
- عود
- كاهش دادن
- کاهش
- منعکس شده
- تنظیم کننده
- گزارش
- نیاز
- محققان
- وضوح
- انقلابی کردن
- خطر
- می گوید:
- مقیاس
- پویش
- پراکنده
- علم
- داستان تخیلی علمی
- جستجو
- مشاهده گردید
- نشان داد
- طرف
- سیگنال
- به طور قابل توجهی
- به سادگی
- تنها
- سایت
- شش
- اندازه
- کوچک
- کوچکتر
- So
- راه حل
- برای تلفن های موبایل
- اسپانیا
- خاص
- مراحل
- مهاجرت تحصیلی
- متعاقب
- قابل توجه
- نشان می دهد
- سیستم
- هدف
- تیم
- تکنیک
- می گوید
- آزمون
- نسبت به
- که
- La
- جهان
- شان
- آنها
- خودشان
- درمان
- اینها
- آنها
- این
- سه
- سه بعدی
- از طریق
- سراسر
- کوچک
- بار
- به
- طرف
- درمان
- رفتار
- درمان
- آزمایش های
- درست
- دور زدن
- به طور معمول
- بی سابقه
- بر
- جذب
- us
- استفاده
- مختلف
- از طريق
- تجسم
- حجم
- دیوار
- بود
- آب
- we
- بود
- چه زمانی
- چه
- که
- در حین
- با
- در داخل
- بدون
- جهان
- خواهد بود
- سال
- زفیرنت