Tutkijat Duke University Medical Center ovat kehittäneet syvään oppimiseen perustuvan tietokoneavusteisen havaitsemisjärjestelmän (CAD) vaikeasti havaittavien aivometastaasien tunnistamiseksi MR-kuvista. Algoritmi osoitti erinomaista herkkyyttä ja spesifisyyttä, mikä ylitti muut kehitteillä olevat CAD-järjestelmät. Työkalu näyttää potentiaalin mahdollistaa uusien aivometastaasien varhaisen tunnistamisen, jolloin ne voidaan kohdistaa stereotaktisella radiokirurgialla (SRS) niiden ilmestyessä ja joidenkin potilaiden kohdalla tarvittavien hoitojen määrää voidaan vähentää.
SRS, joka käyttää tarkasti kohdennettuja fotonisäteitä suuren säteilyannoksen kohdistamiseen aivokohteisiin yhdellä sädehoitokerralla, on kehittymässä tavanomaiseksi hoidoksi potilaille, joilla on rajoitettu määrä aivometastaaseja. Jotta etäpesäke voidaan kohdistaa, se on kuitenkin ensin tunnistettava MR-kuvasta. Valitettavasti noin 10 % ei ole, 30 % alle 3 mm:n kokoisista, vaikka asiantuntevat neuroradiologit arvioivat ne.
Kun nämä löytämättömät aivometastaasit – joita tutkijat kutsuvat retrospektiivisesti tunnistetuiksi metastaasiksi (RIM) – tunnistetaan myöhemmissä magneettikuvauksissa, tarvitaan yleensä toinen SRS-hoito. Tällainen hoito on kallista ja voi olla epämiellyttävää ja invasiivista, ja joskus se vaatii pään immobilisoimista kehyksellä, joka on kiinnitetty kalloon tapeilla.
Äskettäisessä ASTROn vuosikokouksessa Devon Godfrey selitti, että tutkijat suunnittelivat konvoluutiohermoverkkoon (CNN) perustuvan CAD-järjestelmän erityisesti parantamaan vaikeasti havaittavien RIM-solujen ja erittäin pienten prospektiivisesti tunnistettujen metastaasien (PIM) havaitsemista ja segmentointia. Godfrey ja kollegat kuvaavat tämän järjestelmän testausta ja validointia International Journal of Radiation Oncology Biology Physics.
Tiimi koulutti CAD-työkalun MRI-tiedoista (kontrastitehostettu spoiled gradient echo -sekvenssi) 135 potilaalta, joilla oli 563 aivometastaasia. Kuvat hankittiin käyttämällä 1.5 T ja 3.0 T MRI-skannereita eri toimittajilta useista Duke Healthin toimipisteistä. Aineisto sisälsi yhteensä 491 PIM:ää, joiden mediaanihalkaisija oli 6.7 mm, ja 72 RIM:tä 32 potilaalta, joiden mediaanihalkaisija oli 2.7 mm.
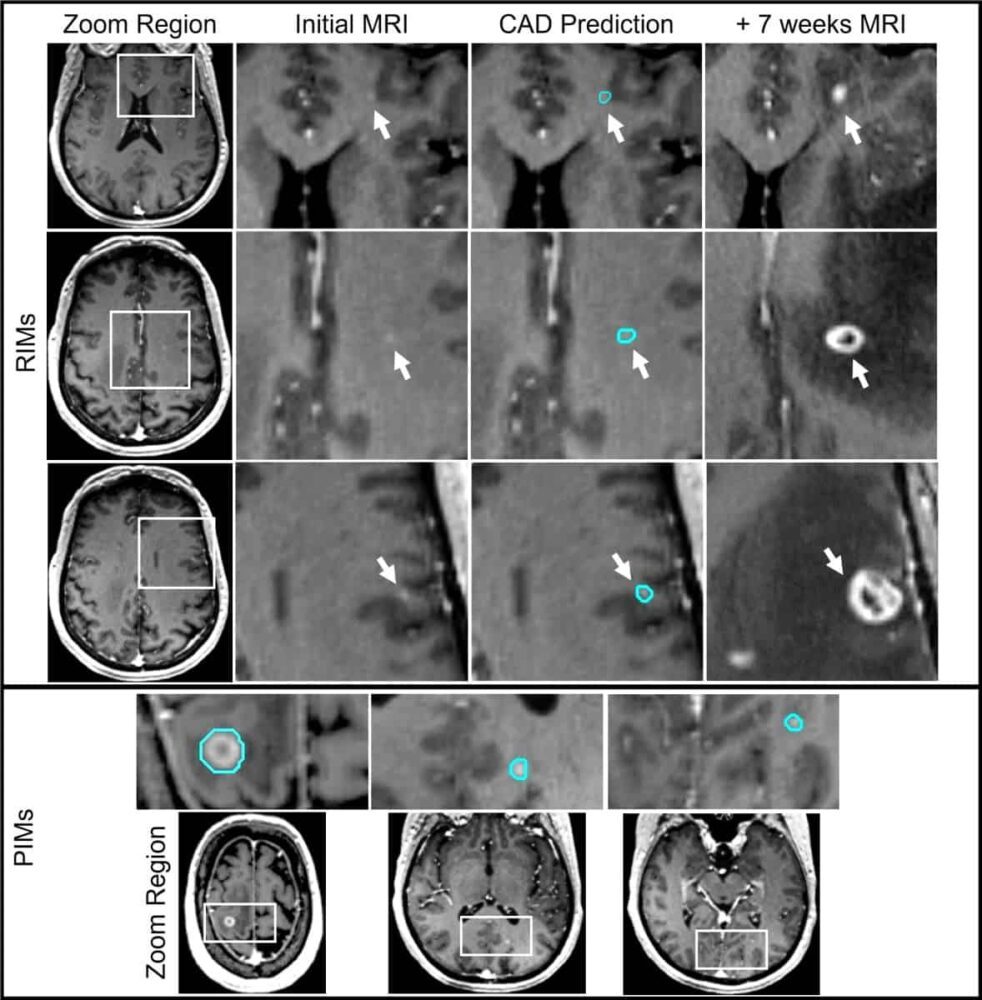
RIM:ien tunnistamiseksi tutkijat tarkastelivat kunkin potilaan alkuperäisiä MR-kuvia etsiäkseen merkkejä kontrastin lisääntymisestä tarkasta paikasta, jossa etäpesäke myöhemmin havaittiin. Tarkastelun jälkeen he luokittelivat jokaisen RIM:n joko täyttivän kuvantamisperusteiset diagnostiset kriteerit (+DC) tai niillä ei ollut riittävästi visuaalista tietoa (-DC), jotta ne voitaisiin tunnistaa metastaasiksi.
Tutkijat satunnaistivat RIM- ja PIM-aineiston viiteen ryhmään, joista neljä käytettiin mallien ja algoritmien kehittämiseen ja yhtä testiryhmänä. "Sekä +DC- että -DC RIM:ien sisällyttäminen johti korkeimpiin herkkyyksiin jokaiselle aivometastaasikategorialle ja -koon, samalla kun se palautti alimman väärien positiivisten osien ja korkeimman positiivisen ennustusarvon", he raportoivat. "Tämä osoittaa selkeän edun pienten haastavien aivometastaasien ylipainotetun otoksen sisällyttämisestä CAD-harjoitustietoihin."
PIM- ja +DC RIM:ille – joilla on selkeät metastaasien ominaisuudet magneettikuvauksessa – malli saavutti 93 %:n kokonaisherkkyyden, joka vaihteli 100 %:sta halkaisijaltaan yli 6 mm:n leesioissa ja 79 %:iin alle 3 mm:n leesioissa. Väärien positiivisten tulosten määrä oli myös vaikuttavan alhainen, keskimäärin 2.7 henkilöä kohden, verrattuna 35-XNUMX:een muissa CAD-järjestelmissä, joissa pienten leesioiden havaitsemisherkkyys on vertailukelpoinen.
CAD-järjestelmä pystyi myös havaitsemaan osan -DC RIM:istä sekä kehitys- että testisarjoista. Aivometastaasien tunnistaminen tässä varhaisessa vaiheessa olisi suuri kliininen etu, koska tällaisia vaurioita voitaisiin sitten tarkkailla perusteellisemmin kuvantamisella, mikä vaatisi tarvittaessa hoitoa.
Duke-tiimi työskentelee nyt parantaakseen CAD-työkalun tarkkuutta käyttämällä useita MR-sekvenssejä. Godfrey selittää, että aivojen MRI-tutkimukset sisältävät lähes aina useita MR-sekvenssejä, jotka tuottavat ainutlaatuista tietoa jokaisesta aivojen vokselista. "Uskomme, että näistä muista sarjoista saatavilla olevien lisätietojen sisällyttämisen pitäisi parantaa sen tarkkuutta", hän sanoo.
Godfrey huomauttaa, että tutkijat ovat vain viikkojen päässä käynnistämään simuloidun mahdollisen kliinisen käytön tutkimuksen olemassa olevasta CAD-järjestelmästä tutkiakseen, kuinka työkalu vaikuttaa sekä radiologien että säteilyonkologien kliiniseen päätöksentekoon.
Syväoppiminen auttaa radiologia havaitsemaan keuhkosyövän keuhkojen röntgenkuvissa
”Useille SRS:ää suorittaville neuroradiologeille ja neurosäteilyonkologeille esitetään aivojen MR-kuvauksia. Heitä pyydetään etsimään leesio, joka voi olla aivometastaasi, arvioimaan heidän luottamustasonsa, että se on, ja ilmoittamaan, hoitaisiko he vauriota SRS:llä sen perusteella, mikä se näkyy kuvissa", hän kertoo. Fysiikan maailma. "Sitten esitämme heille CAD-ennusteet ja arvioimme CAD:n vaikutuksen kunkin lääkärin kliinisiin päätöksiin."
Jos tämä simulaatiotutkimus tuottaa lupaavia tuloksia, Godfrey odottaa ottavansa käyttöön CAD-työkalun, joka auttaa tunnistamaan haastavia aivoetastaasseja tulevissa uusissa potilaissa, joita hoidetaan Duke Radiation Oncology -klinikalla tutkimusprotokollan mukaisesti, ehkä jo vuoden 2023 puolivälissä.