Kasvaimet voidaan tuhota monella tapaa. Sädehoito käyttää ionisoivaa säteilyä vaurioittamaan DNA:ta ja tuhoamaan kasvainsoluja. Harvempi lähestymistapa on fotodynaaminen hoito, jossa käytetään valolla aktivoitua lääkettä tappamaan syöpäsoluja mitokondriovaurioiden kautta. Sitten on nouseva radiodynaamisen terapian (RDT) tekniikka.
"Radiodynaaminen hoito on sädehoidon ja fotodynaamisen hoidon yhdistelmä", selitti Charlie Ma Fox Chase Cancer Centeristä puhuessaan äskettäin AAPM:n vuosikokous.
Fotodynaaminen hoito käyttää tyypillisesti näkyvää laservaloa valoherkän lääkkeen aktivoimiseen, joka on ensisijaisesti paikantunut kasvainsoluihin. Aktivoitu lääke tuottaa erittäin sytotoksista singlettihappea, joka aiheuttaa solukuoleman. Laservalon rajallinen tunkeutuminen kudokseen tarkoittaa kuitenkin sitä, että tekniikkaa käytetään pääasiassa pinnallisten kasvainten tai kohtien, joissa on endoskooppinen pääsy, hoitoon. RDT käyttää suurienergisiä fotonisäteitä valoherkistimen aktivoimiseksi syvälle juurtuneiden kasvainten hoitamiseksi, joihin fotodynaaminen hoito ei pääse.
"RDT:ssä käytämme 20-30 prosenttia sädehoidon annoksesta", Ma selitti. "Ja sitten käytämme myös Cherenkov-valoa." Hän totesi, että tällä Tšerenkovin säteilyllä, joka syntyy sädehoidon aikana, kun hoitosäde on vuorovaikutuksessa potilaan kudoksen kanssa, on lähes identtinen valon jakautuminen terapeuttisen säteilyannosjakauman kanssa ja on siten helposti suunniteltava.
Sen lisäksi, että lääke kerääntyy primaariseen kasvaimeen, se imeytyy myös jakautuneisiin metastaattisiin soluihin, jotka voidaan tappaa erittäin pienellä Tšerenkovin valoannoksella. "Nyt ensimmäistä kertaa RDT tekee sädehoidosta paitsi paikallisen ja alueellisen myös systeemisen hoitotekniikan", sanoi Ma.
Fox Chasen tiimi käyttää lääkettä nimeltä 5-aminolevuliinihappo (5-ALA) RDT:hen. Syöpäsolujen mitokondriot ottavat 5-ALA:ta vastaan, ja kasvaimissa 10-20 kertaa enemmän kuin normaaleissa kudoksissa. Syöpäsolun sisällä 5-ALA metaboloituu protoporfyriini IX:ksi (PpIX), valolle herkistäjäksi, jonka absorptiospektrin huippu on noin 380–430 nm. Tämä ei ole ihanteellinen punaiselle laservalolle, jota usein käytetään fotodynaamiseen hoitoon. Se on kuitenkin loistava vastine Tšerenkovin absorptiohuippulle 370–430 nm:ssä.
Prekliininen todiste
Muutaman viime vuoden aikana Ma ja hänen tiiminsä ovat tehneet monia prekliinisiä tutkimuksia käyttämällä erilaisia kasvainsolulinjoja ja erilaisia säteilyenergioita. Hän jakoi joitain tuloksia suuresta tutkimuksesta (useita satoja eläimiä), joissa arvioitiin kasvaimia kantavien hiirten RDT:tä käyttämällä 100 mg/kg 5-ALA:ta ja 6, 15 tai 45 MV fotonisäteilyä.
Ma huomautti, että kasvain oli erittäin aggressiivinen, sillä 4 Gy:n sädehoito yksin tappoi vain noin 10 % kasvainsoluista. Lisäksi RDT 6 MV:llä ei merkittävästi lisännyt terapeuttista vaikutusta. "Siksi ihmiset olivat huolissaan siitä, että Tšerenkovin valo ei riitä", hän huomautti. "Mutta 15 ja 45 MV:llä näet paljon enemmän kasvaimen kasvun viivettä. Tutkimme edelleen, miksi tämä dramaattinen muutos johtuu energiasta, meidän on löydettävä tarkka mekanismi sen takana.
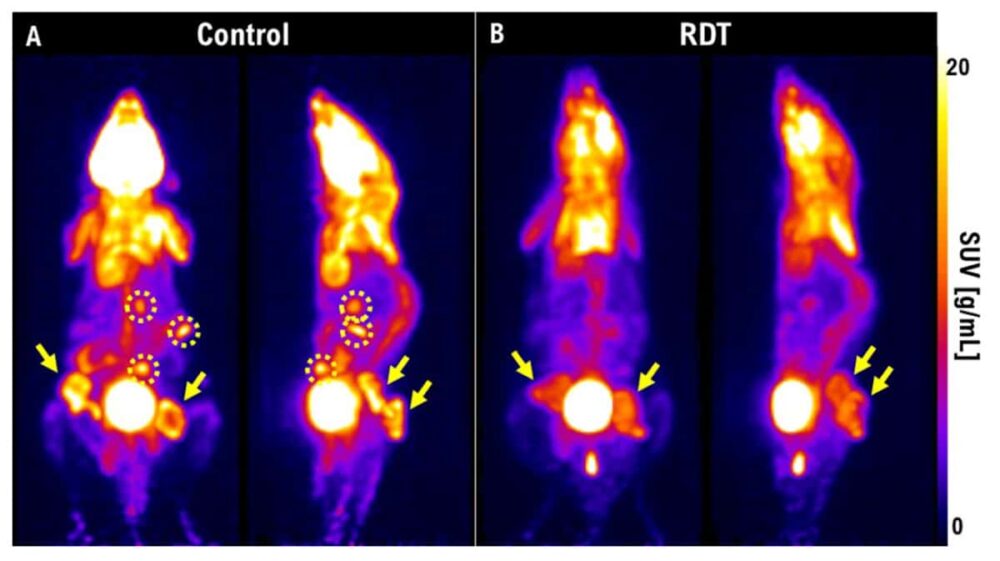
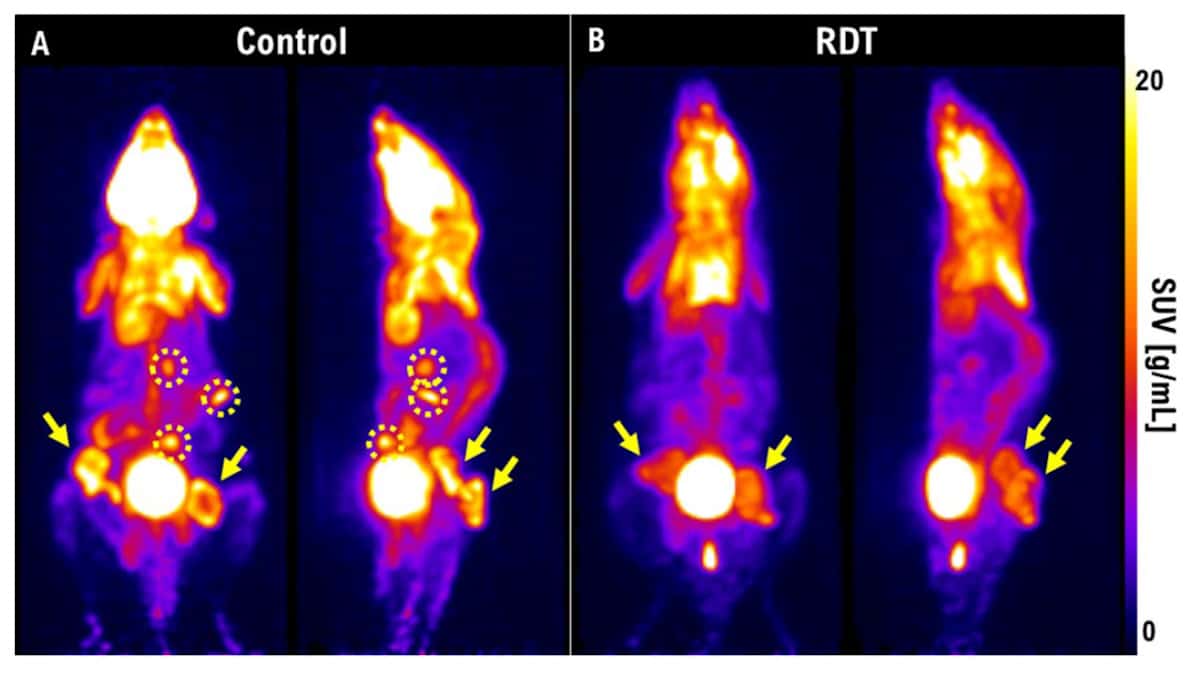
Ryhmä käytti PET:tä visualisoidakseen kasvaimen kutistumisen RDT:n jälkeen. Viikko hoidon jälkeen kontrollihiirten kasvaimet olivat kasvaneet ja metastasoituneet, kun taas RDT:llä hoidetuilla leesioilla oli paljon pienempiä vaurioita eikä etäpesäkkeitä. Ma kuvaili myös tutkimusta erittäin aggressiivisesta kilpirauhassyövästä kaneissa. Viikko 3 Gy:n sädehoidon jälkeen kasvain kasvoi edelleen. "Mutta jos käytämme RDT:tä 3 Gy:lla 5-ALA:n kanssa, kasvainta ei näkynyt PET-kuvissa." Hän korosti, että PET tarjoaa erinomaisen tavan suorittaa varhaisen hoidon arviointi ja voi auttaa määrittämään, olisiko RDT tehokas potilaalla.
Fox Chase suorittaa nyt kliinistä koetta RDT:llä, ja tutkimuksen ensimmäisessä vaiheessa tutkitaan annoksen nostamista (sekä säteilyannos- että lääkeannos) myöhäisvaiheen kasvaimissa. Tämä vaihe on nyt saavuttanut lopullisen annostason, kun potilasta on jäljellä enää kolme, sanoi Ma ja huomautti, että toistaiseksi missään tapauksessa ei ole ilmennyt toksisuutta. Muensterin yliopistollisessa sairaalassa toisessa RDT-tutkimuksessa tutkitaan potilaita, joilla on ensimmäinen glioblastooman uusiutuminen.
Tosielämän tapauksia
Lopuksi Ma esitteli tuloksia useista tosielämän tapauksista. "Olet innoissasi nähdessäsi nämä", hän kertoi yleisölle ja huomautti, että "yleensä ihmiset eivät usko, että se toimii, ellei sinulla ole kuukauden mittaista kuvantamista CT:llä, MR:llä tai PET:llä".
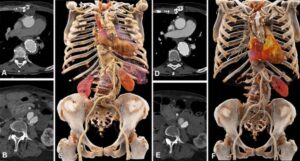
Ensimmäisessä esimerkissä, maksametastaasien hoidossa, hän osoitti, että kuukausi RDT:n jälkeen PET-kuvaus paljasti, ettei kasvaimia ollut jäljellä. Seuraavaksi hän esitteli tapauksen keuhkosyövästä, jossa oli etäpesäkkeitä: "Voit nähdä erittäin dramaattisia tuloksia, kun kasvaimet deaktivoituivat RDT: n jälkeen", hän sanoi.
Istutettava laite tarjoaa henkilökohtaista fotodynaamista hoitoa
Muita onnistuneita RDT-hoitoja olivat ruokatorven syöpä, keuhkokasvain, jossa oli useita luumetastaaseja, ja potilas, joka ei ollut saanut kemoterapiaa, mutta jolla oli hyvä vaste kolme päivää RDT:n jälkeen. Ma huomautti, että suurimmalla osalla potilaista oli myöhäisvaiheen syöpiä ja muut hoidot epäonnistuivat. "Näemme vaikutuksen, joten toivottavasti voimme parantaa heidän selviytymistään", hän lisäsi.
"RDT voi olla paikallinen, alueellinen ja systeeminen hoito, jossa yhdistyvät sädehoito ja fotodynaaminen hoito", Ma päätti. "Meillä on paljon vitro ja in vivo kokeiluja osoittaakseen sen terapeuttisen potentiaalin, ja vaikka kliinisiä tutkimuksia on vähän, toivon saavamme lisää tuloksia tulevaisuudessa ja tehdä tästä jotain todella hyödyllistä."
- SEO-pohjainen sisällön ja PR-jakelu. Vahvista jo tänään.
- PlatoData.Network Vertical Generatiivinen Ai. Vahvista itseäsi. Pääsy tästä.
- PlatoAiStream. Web3 Intelligence. Tietoa laajennettu. Pääsy tästä.
- PlatoESG. Autot / sähköautot, hiili, CleanTech, energia, ympäristö, Aurinko, Jätehuolto. Pääsy tästä.
- BlockOffsets. Ympäristövastuun omistuksen nykyaikaistaminen. Pääsy tästä.
- Lähde: https://physicsworld.com/a/radiodynamic-therapy-harnessing-light-to-improve-cancer-treatments/
- :on
- :On
- :ei
- $ YLÖS
- 10
- 100
- 15%
- 20
- 30
- a
- Meistä
- pääsy
- lisä-
- Lisäksi
- Jälkeen
- aggressiivinen
- AL
- yksin
- Myös
- Vaikka
- an
- ja
- eläimet
- vuotuinen
- Kaikki
- lähestymistapa
- OVAT
- noin
- AS
- arvioidessaan
- At
- yleisö
- BE
- Palkki
- takana
- Uskoa
- LUU
- sekä
- mutta
- by
- nimeltään
- CAN
- Syöpä
- Syöpäsolut
- ei voi
- tapaus
- tapauksissa
- syyt
- Solut
- keskus
- muuttaa
- jahdata
- piireissä
- napsauttaa
- Kliininen
- kliinisiä tutkimuksia
- yhdistelmä
- yhdistää
- Yhteinen
- päätökseen
- ohjaus
- voisi
- päivää
- Kuolema
- viivyttää
- Antaa
- osoittaa
- on kuvattu
- tuhota
- tuhonnut
- Määrittää
- laite
- DID
- eri
- jaettu
- jakelu
- dna
- do
- Dont
- dramaattisesti
- huume
- kaksi
- aikana
- Varhainen
- helposti
- vaikutus
- Tehokas
- muualla
- syntymässä
- korostettiin
- energia
- laajenemisen
- arviointi
- tutkii
- esimerkki
- erinomainen
- innoissaan
- kokeiluja
- selitti
- Epäonnistui
- paljon
- harvat
- lopullinen
- Löytää
- Etunimi
- ensimmäistä kertaa
- jälkeen
- varten
- kettu
- alkaen
- tulevaisuutta
- syntyy
- synnyttää
- hyvä
- suuri
- suurempi
- Kasvava
- täysikasvuinen
- Kasvu
- HAD
- valjastaminen
- Olla
- he
- auttaa
- erittäin
- hänen
- toivoa
- Toivon mukaan
- Kuitenkin
- HTTPS
- sata
- i
- ihanteellinen
- identtinen
- if
- kuva
- kuvien
- Imaging
- parantaa
- in
- mukana
- Kasvaa
- osoittaa
- tiedot
- sisällä
- vuorovaikutuksessa
- tulee
- kysymys
- IT
- SEN
- jpg
- vain
- Tappaa
- suuri
- laser
- Sukunimi
- vasemmalle
- vähemmän
- Taso
- valo
- rajallinen
- linjat
- Maksa
- paikallinen
- Erä
- Matala
- pääasiallisesti
- tehdä
- TEE
- monet
- ottelu
- max-width
- välineet
- mekanismi
- mitokondriot
- Kuukausi
- lisää
- eniten
- mr
- paljon
- moninkertainen
- Tarve
- seuraava
- Nro
- normaali
- huomattava
- huomata
- nyt
- numero
- tapahtui
- of
- usein
- on
- kerran
- ONE
- vain
- avata
- or
- Muut
- ulos
- Happi
- potilas
- potilaat
- Peak
- tunkeutuminen
- Ihmiset
- varten
- Suorittaa
- suoritettu
- esittävä
- yksilöllinen
- vaihe
- Fysiikka
- Fysiikan maailma
- suunnitteilla
- Platon
- Platonin tietotieto
- PlatonData
- plus
- mahdollinen
- esitetty
- ensisijainen
- tarjoaa
- Sädehoito
- tavoittaa
- saavutettu
- ihan oikeesti
- äskettäinen
- toistuminen
- punainen
- alueellinen
- pysyi
- vastaus
- tulokset
- Revealed
- Said
- Toinen
- nähdä
- nähneet
- useat
- yhteinen
- osoittivat
- merkittävästi
- Sivustot
- pienempiä
- So
- niin kaukana
- jonkin verran
- jotain
- puhuminen
- spektri
- Yhä
- opinnot
- tutkimus
- Opiskelu
- onnistunut
- riittävä
- eloonjääminen
- systeeminen
- otettava
- joukkue-
- kuin
- että
- -
- Tulevaisuus
- heidän
- sitten
- Siellä.
- Nämä
- tätä
- ne
- kolmella
- thumbnail
- Näin
- aika
- kertaa
- että
- kohdella
- hoito
- oikeudenkäynti
- tutkimuksissa
- totta
- tyypillisesti
- yliopisto
- käyttää
- käytetty
- käyttötarkoituksiin
- käyttämällä
- eri
- hyvin
- kautta
- näkyvä
- oli
- Tapa..
- tavalla
- we
- viikko
- onko
- joka
- vaikka
- miksi
- tulee
- with
- sisällä
- toimii
- maailman-
- huolestunut
- olisi
- vuotta
- Voit
- zephyrnet