Les cellules synthétiques, conçues pour imiter certaines des fonctions remplies par les cellules vivantes, sont prometteuses pour des applications en biotechnologie et en médecine. Cependant, même les plus petites cellules biologiques sont extrêmement complexes et la construction de cellules artificielles vivantes se heurte à de nombreux obstacles. Des chercheurs dans le Laboratoire Schulman à l'Université Johns Hopkins ont récemment fait des progrès vers l'un de ces défis : l'échange de matière et d'informations à travers les frontières cellulaires.
Ecrire dans Science Advances, les chercheurs – travaillant en collaboration avec le Groupe Aksimentiev à l'Université de l'Illinois à Urbana-Champaign - démontrer le transport sans fuite de petites molécules à travers des nanocanaux d'ADN modifiés sur des distances sans précédent. À l'avenir, leurs travaux pourraient contribuer à la construction de cellules artificielles, ainsi qu'à l'étude et à la manipulation de tissus vivants.
Les cellules des organismes multicellulaires ont besoin d'échanger de la matière et de communiquer pour assurer leur survie collective. Étant donné que chaque cellule est entourée d'une membrane lipidique impénétrable à de nombreuses molécules biologiques, l'évolution a produit des mécanismes permettant de franchir cette barrière. Les récepteurs de signalisation, les transporteurs et les pores relaient les informations et permettent le passage des molécules entre les cellules et leur extérieur, tandis que les contacts cellulaires tels que les jonctions lacunaires relient directement l'intérieur des cellules voisines et permettent la diffusion de petites molécules de cellule à cellule.
Pour imiter ces processus dans des systèmes artificiels, "les chercheurs ont développé des cellules synthétiques positionnées les unes à côté des autres qui peuvent communiquer à travers les pores protéiques de leurs membranes", explique le premier auteur Yi Li, qui a co-dirigé l'étude. "Cependant, développer des systèmes cellulaires synthétiques où les cellules peuvent communiquer et échanger des matériaux sur de plus longues distances reste un défi."
Les structures protéiques qui facilitent la communication de cellule à cellule en biologie sont construites "de bas en haut" à partir d'acides aminés - l'information codée dans leur séquence se traduit par une structure. Une autre macromolécule biologique, l'ADN, est principalement utilisée pour le stockage d'informations dans les cellules ; mais en raison de sa facilité de synthèse et de son potentiel à former des structures de haut niveau, le domaine de la nanotechnologie de l'ADN est allé bien au-delà de sa première preuve de concept il y a environ 30 ans. Depuis, les scientifiques ont assemblé des structures 2D et 3D de plus en plus sophistiquées à partir d'ADN, y compris des treillis, des tubes, des corps géométriques et même des rendus artistiques de visages souriants, dans des efforts appelés origami d'ADN.
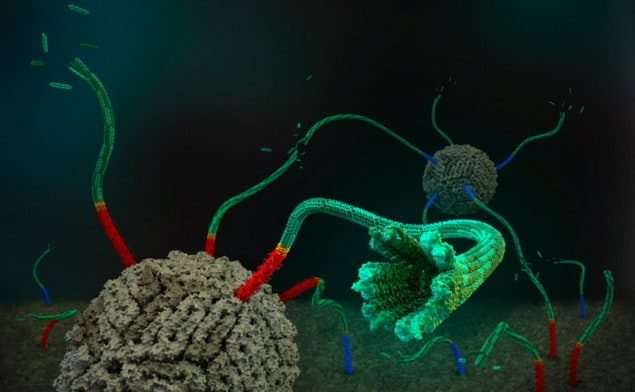
Dans leur étude, les chercheurs du Schulman Lab ont combiné des nanopores d'origami d'ADN, qui relient les membranes des vésicules ressemblant à des cellules et créent de petites ouvertures pour que les molécules se croisent, avec des nanotubes d'ADN auto-assemblés. En quantifiant le flux d'une molécule de colorant dans les vésicules, ils ont montré que des nanopores courts rendaient la membrane perméable au colorant. Ils ont également validé que la vitesse de ce transport est compatible avec la diffusion et ont découvert qu'un capuchon d'ADN spécialement conçu peut bloquer les pores et empêcher le colorant d'entrer.

L'équipe a ensuite étendu ces travaux aux nanotubes d'ADN d'une longueur médiane de 700 nm et maximale supérieure à 2 µm. Encore une fois, des expériences ont montré que l'influx de colorant est amélioré en présence des constructions d'ADN et que le capuchon peut arrêter la perméation. L'implication, dit Li, est que "les petites molécules peuvent traverser les tubes sans fuites, et nous nous attendons à ce que les grosses molécules, telles que les protéines, puissent également être transportées à travers ces nanotubes".
Les membres du groupe Aksimentiev ont effectué des simulations informatiques de la dynamique brownienne du système nanopore-colorant. Celles-ci ont illustré que pour les molécules inférieures à une taille seuil, la fuite à travers la paroi latérale du tube d'ADN dominait l'influx, tandis que pour les molécules plus grosses, la diffusion de bout en bout devient le mécanisme préféré .
Li explique que de telles simulations sont complémentaires des expériences de deux manières. "Ils peuvent être utilisés comme outils de conception pour aider les chercheurs à concevoir des structures nanométriques qui ont des fonctions spécifiques", dit-il, par exemple en "simulant la cinétique d'auto-assemblage de nos nanostructures d'ADN", mais ils permettent également de "valider des résultats expérimentaux et de fournir des informations supplémentaires sur les processus physiques ».

Conception d'ADN à faire soi-même
Rebecca Schulman – qui a codirigé la recherche – établit une analogie avec les tuyaux. « Cette étude suggère très fortement qu'il est possible de construire des nanotubes qui ne fuient pas en utilisant ces techniques simples d'auto-assemblage, où nous mélangeons des molécules dans une solution et les laissons simplement former la structure souhaitée. Dans notre cas, nous pouvons également attacher ces tubes à différents points d'extrémité pour former quelque chose comme de la plomberie. »
Le laboratoire a des plans ambitieux pour l'application de ces nanotubes. « Les développements futurs incluent la connexion de deux cellules artificielles ou plus avec nos nanotubes d'ADN et la démonstration du transport moléculaire entre elles. Nous pouvons potentiellement montrer [que] le transport de molécules de signalisation d'une cellule peut activer/désactiver l'expression génique dans une autre cellule », a déclaré Li. Monde de la physique. L'équipe espère également « utiliser des nanotubes pour contrôler la délivrance de molécules de signalisation ou de thérapeutiques aux cellules de mammifères, soit pour étudier les comportements de signalisation cellulaire, soit pour développer une stratégie de délivrance de médicaments ».