La myéline est une couche protectrice qui se forme autour des nerfs pour les isoler et accélérer la transmission des impulsions électriques. La démyélinisation, c'est-à-dire la perte de cette couche isolante, contribue à de nombreuses maladies neurologiques, notamment la sclérose en plaques, la maladie d'Alzheimer, les accidents vasculaires cérébraux et la démence. Une technique efficace pour détecter cette maladie potentiellement réversible pourrait améliorer les diagnostics des maladies cérébrales et permettre le suivi des traitements possibles. Cependant, à l’heure actuelle, aucun test d’imagerie ne permet d’identifier avec précision la démyélinisation.
Pour combler cette lacune, des chercheurs du Centre Gordon d'imagerie médicale du Massachusetts General Hospital et de la Harvard Medical School étudient l’utilisation d’un nouveau radiotraceur TEP – 18F-3-fluoro-4-aminopyridine (18F-3F4AP) – pour imager les lésions démyélinisées dans le cerveau. Ils ont maintenant testé le traceur chez l'homme pour la première fois, rapportant leurs résultats dans le Journal européen de médecine nucléaire et d'imagerie moléculaire.
"Disposer d'un outil d'imagerie spécifique à la démyélinisation peut aider à mieux comprendre la contribution de la démyélinisation à différentes maladies et à mieux surveiller une maladie ou la réponse à un traitement - par exemple, un traitement remyélinisant", explique le premier auteur. Pedro Brugarolas Dans un communiqué de presse.
18Le F-3F4AP est une version radiofluorée du médicament contre la sclérose en plaques, la 4-aminopyridine. Le traceur, qui pénètre dans le cerveau par diffusion passive, se lie aux axones démyélinisés de la même manière que le médicament lui-même. Des études antérieures ont démontré que la TEP avec 18Le F-3F4AP peut détecter des lésions dans un modèle de démyélinisation chez le rat et le traceur possède des propriétés appropriées pour l'imagerie du cerveau des macaques rhésus, ce qui a incité l'équipe à étudier son utilisation chez l'homme.
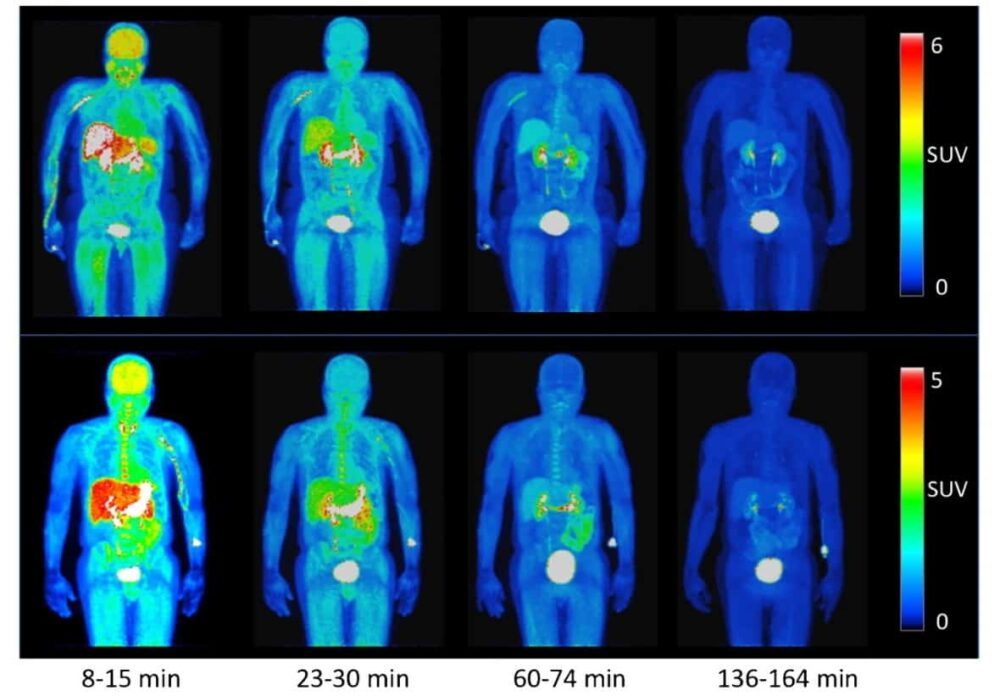
Brugarolas et ses collègues ont réalisé des TEP sur quatre volontaires sains après avoir administré 368 ± 17.9 MBq de 18F-3F4AP. Après un scanner à faible dose, ils ont commencé la TEP immédiatement après l'injection du traceur, enregistrant une série d'images dans sept positions du lit du scanner pour couvrir l'ensemble du corps. Pour capturer la cinétique du traceur et maximiser la qualité de l’image, le temps de balayage initial par position était de 1 min, passant à 2, 4 et 8 min par position. L’ensemble de l’acquisition TEP a duré 4 heures.
Les images TEP et les courbes temps-activité (TAC) qui en ont résulté ont révélé que le traceur se distribuait rapidement dans tout le corps, y compris le cerveau, et était rapidement éliminé par excrétion rénale. Huit à 8 minutes après l'injection, une activité maximale a été observée dans le foie, les reins, la vessie, la rate, l'estomac et le cerveau. Entre 14 et 22 minutes, l'activité la plus élevée concernait les reins, les voies biliaires et la vessie. Après 28 minutes, la majeure partie de l'activité avait disparu des organes et s'était accumulée dans la vessie.
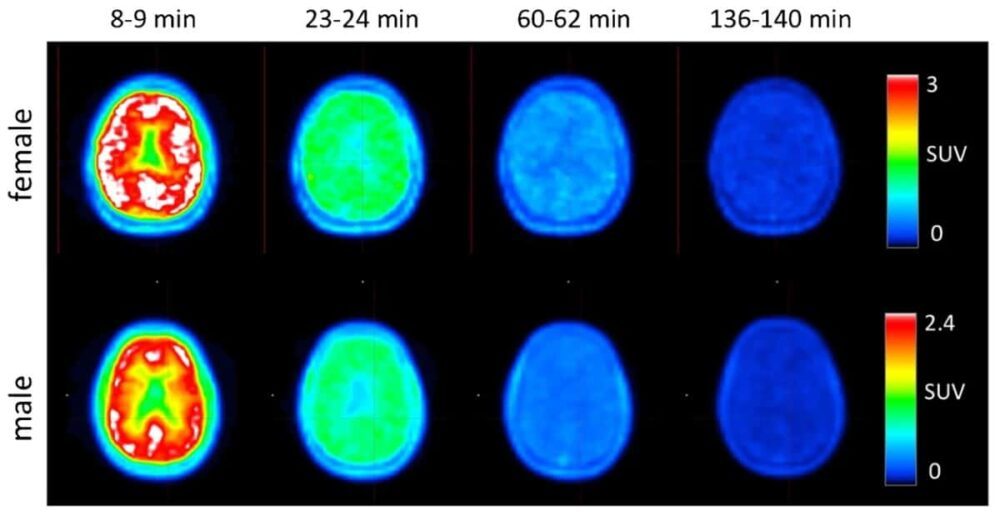
L’équipe a également utilisé les TAC intégrés pour effectuer la dosimétrie. La dose efficace moyenne était de 12.2 ± 2.2 µSv/MBq pour les quatre participants, sans aucune différence observée entre les volontaires masculins et féminins. Les chercheurs notent que cette dose efficace est significativement inférieure à celle estimée à partir d’études sur des primates non humains (21.6 ± 0.6 µSv/MBq), probablement en raison de la clairance plus rapide observée chez l’homme que chez les macaques rhésus. Cette dose était également inférieure à celle des autres traceurs TEP, tels que 18F-FDG.
Il est important de noter que le traceur et la procédure d’imagerie ont été bien tolérés par tous les participants, sans qu’aucun événement indésirable ne soit survenu pendant l’analyse. Il n’y avait aucune différence significative dans les signes vitaux des volontaires (température, pression artérielle et saturation en oxygène) avant et après l’analyse, ni aucun changement significatif dans les résultats des métabolites sanguins et de l’électrocardiogramme obtenus dans les 30 jours précédant et suivant l’analyse.

Le traceur PET mesure la démyélinisation chez la souris
Les chercheurs concluent que 18Le F-3F4AP pénètre facilement dans le cerveau et peut être utilisé sans danger chez l'homme, avec un niveau de dose de rayonnement acceptable. Ils suggèrent que leurs résultats ouvrent la porte à d'autres études étudiant la capacité du traceur à détecter des lésions démyélinisées dans différentes populations de patients.
Brugarolas raconte Monde de la physique que l'équipe poursuit actuellement deux petites études cliniques utilisant le nouveau traceur : pour étudier sa valeur pour imagerie de la sclérose en plaques; et d'évaluer son utilisation chez les patients atteints traumatisme crânien, troubles cognitifs légers et maladie d'Alzheimer.