रेडियोथेरेपी सबसे आम कैंसर उपचारों में से एक है, जो प्रभावी रूप से जीवित रहने के समय को बढ़ाता है और कैंसर रोगियों के लिए इलाज की दर में वृद्धि करता है। हालांकि, रेडियोथेरेपी-प्रेरित हड्डी क्षति - कम हड्डी द्रव्यमान, हड्डी की नाजुकता में वृद्धि और फ्रैक्चर और ऑस्टियोनेक्रोसिस के उच्च जोखिम सहित - एक आम समस्या बनी हुई है जिसमें वर्तमान में प्रभावी काउंटरमेशर्स की कमी है।
विकिरण ओस्टियोब्लास्ट्स नामक हड्डी बनाने वाली कोशिकाओं की वृद्धि, उत्तरजीविता और परिपक्वता को दबाकर इस क्षति का कारण बनता है, इस प्रकार हड्डी के गठन को रोकता है। एक संभावित उपाय गैर-आक्रामक विद्युत चुम्बकीय क्षेत्रों (ईएमएफ) के संपर्क में हो सकता है, जो ऑस्टियोब्लास्ट वृद्धि और भेदभाव को प्रोत्साहित करने के लिए जाने जाते हैं, और विकिरण के प्रभाव को कम कर सकते हैं। अब चीन में एक शोध दल ने इस तरह के उपचार की प्रभावकारिता को अधिकतम करने के लिए इष्टतम ईएमएफ तरंग की पहचान की है, जिसमें निष्कर्षों की रिपोर्ट की गई है विज्ञान अग्रिम.
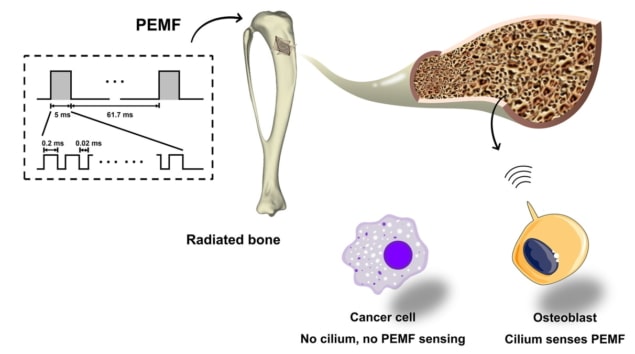
दा जिंग, से चौथा सैन्य चिकित्सा विश्वविद्यालय, और सहकर्मियों ने पहले साइनसॉइडल ईएमएफ, सिंगल-स्पंदित ईएमएफ और स्पंदित-फट ईएमएफ (पीईएमएफ) सहित विभिन्न तरंगों का उपयोग करके ईएमएफ उत्तेजना के लिए हड्डी की कोशिकाओं का अध्ययन किया। कोशिकाओं की प्रतिक्रिया का आकलन करने के लिए, उन्होंने रीयल-टाइम इंट्रासेल्युलर कैल्शियम आयन (Ca .) की निगरानी की2+) सिग्नलिंग, बाहरी उत्तेजनाओं के लिए सबसे शुरुआती सेलुलर प्रतिक्रियाओं में से एक।
टीम ने पाया कि PEMF ने अधिक मजबूत इंट्रासेल्युलर Ca . को प्रेरित किया2+ अन्य तरंगों की तुलना में विकिरणित अस्थिकोरक में संकेतन, अद्वितीय Ca . द्वारा विशेषता2+ कई Ca . के साथ दोलन2+ स्पाइक्स आगे के विश्लेषणों से पता चला है कि 2 mT के चुंबकीय क्षेत्र की तीव्रता और 15 Hz की आवृत्ति के साथ पहले से अज्ञात PEMF तरंग ने ऑस्टियोब्लास्ट में सबसे मजबूत प्रतिक्रिया प्राप्त की। इसके विपरीत, इस PEMF तरंग का अन्य प्रकार के विकिरणित अस्थि कोशिका (ऑस्टियोक्लास्ट और ऑस्टियोसाइट्स) पर कोई प्रभाव नहीं पड़ा।
इसके बाद, शोधकर्ताओं ने जांच की कि क्या PEMF इन इष्टतम मापदंडों का उपयोग करके विकिरण-प्रेरित हड्डी के नुकसान को कम कर सकता है vivo में. चूहों पर अध्ययन में, उन्होंने फोकल विकिरण (एक दिन अलग) की दो 8 Gy खुराक के लिए एक हिंडलिंब को उजागर किया और 45 दिनों के बाद हड्डी की संरचना का आकलन करने के लिए माइक्रो-सीटी का उपयोग किया। विकिरणित अंगों ने महत्वपूर्ण ट्रैब्युलर हड्डी के नुकसान का प्रदर्शन किया, जिसमें अस्थि मात्रा अंश में लगभग 50% की कमी और अनियंत्रित पक्ष की तुलना में अस्थि खनिज घनत्व शामिल है।
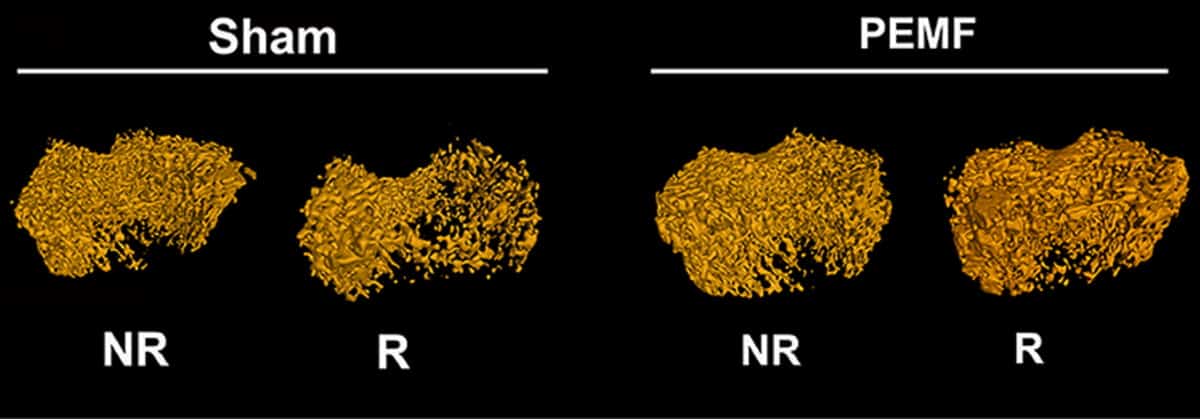
विकिरण के बाद 2 दिनों के लिए चूहों के एक दूसरे समूह को दैनिक पूरे शरीर का PEMF (45 घंटा / दिन) प्राप्त हुआ। इस उपचार ने ऑस्टियोब्लास्ट को बचाकर, विकिरणित हिंद अंगों में अस्थि द्रव्यमान और यांत्रिक गुणों को गैर-विकिरणित अंगों के स्तर तक बहाल कर दिया। टीम ने नोट किया कि PEMF का जानवरों के शरीर के वजन या भोजन के सेवन पर कोई प्रभाव नहीं पड़ा।
यह दिखाने के बाद कि PEMF जोखिम विकिरण-प्रेरित हड्डी के नुकसान को कम कर सकता है, यह भी आवश्यक है कि PEMF ट्यूमर के उपचार पर प्रतिकूल प्रभाव न डाले। इसे ध्यान में रखते हुए, शोधकर्ताओं ने ओस्टियोब्लास्ट्स और विभिन्न ट्यूमर कोशिकाओं (स्तन कैंसर, पेट के कैंसर, घातक मेलेनोमा और ओस्टियोसारकोमा कोशिकाओं) की संवेदनशीलता की तुलना पीईएमएफ से की।
विकिरण ने सेल व्यवहार्यता को कम कर दिया और सभी प्रकार की कोशिकाओं में एपोप्टोसिस को बढ़ावा दिया। महत्वपूर्ण रूप से, हालांकि पीईएमएफ ने ऑस्टियोब्लास्ट व्यवहार्यता में सुधार किया और ऑस्टियोब्लास्ट एपोप्टोसिस को रोक दिया, लेकिन किसी भी समय किसी भी ट्यूमर कोशिकाओं में व्यवहार्यता या एपोप्टोसिस पर इसका कोई प्रभाव नहीं पड़ा।
जीवित बायोइंक हड्डी की मरम्मत और पुनर्जनन को बढ़ा सकता है
शोधकर्ता इस चयनात्मकता का श्रेय प्राथमिक सिलिया - संवेदी अंगों की उपस्थिति को देते हैं जो बाह्य यांत्रिक संकेतों का पता लगाते हैं और उनका अनुवाद करते हैं - जो PEMF सेंसर के रूप में कार्य करते हैं। ये प्राथमिक सिलिया ऑस्टियोब्लास्ट में अत्यधिक प्रचुर मात्रा में हैं, लेकिन अधिकांश ट्यूमर कोशिकाओं में अनुपस्थित हैं। एक प्रयोग में जहां विकिरणित ऑस्टियोब्लास्ट में प्राथमिक सिलिया की पीढ़ी को अवरुद्ध कर दिया गया था, ऑस्टियोब्लास्ट अस्तित्व में पीईएमएफ-मध्यस्थता वृद्धि और भेदभाव लगभग पूरी तरह से गायब हो गया।
"यह देखते हुए कि, सभी अस्थि कोशिका प्रकारों में, ऑस्टियोब्लास्ट विकिरण के प्रति विशेष रूप से संवेदनशील होते हैं, यह PEMF रेजिमेन, जो ऑस्टियोब्लास्ट के विशिष्ट सक्रियण को प्रेरित करता है, विकिरण-प्रेरित हड्डी क्षति के खिलाफ एक आशाजनक और अत्यधिक कुशल दृष्टिकोण प्रतीत होता है," शोधकर्ताओं ने निष्कर्ष निकाला।