अमेरिकी खाद्य एवं औषधि प्रशासन (एफडीए) या जापानी फार्मास्यूटिकल्स एंड मेडिकल डिवाइसेज एजेंसी (पीएमडीए) जैसी नियामक एजेंसियों से बाजार में अपनी दवाओं को बेचने के लिए अनुमोदन प्राप्त करने वाली फार्मास्युटिकल कंपनियों को यह साबित करने के लिए सबूत प्रस्तुत करना होगा कि उनकी दवा अपने इच्छित उद्देश्य के लिए सुरक्षित और प्रभावी है। उपयोग। चिकित्सकों, सांख्यिकीविदों, रसायनज्ञों, फार्माकोलॉजिस्टों और अन्य नैदानिक वैज्ञानिकों की एक टीम नैदानिक परीक्षण सबमिशन डेटा और प्रस्तावित लेबलिंग की समीक्षा करती है। यदि समीक्षा स्थापित करती है कि यह साबित करने के लिए पर्याप्त सांख्यिकीय साक्ष्य हैं कि दवा के स्वास्थ्य लाभ जोखिमों से अधिक हैं, तो दवा को बिक्री के लिए अनुमोदित किया जाता है।
नैदानिक परीक्षण सबमिशन पैकेज में सारणीबद्ध डेटा, विश्लेषण डेटा, परीक्षण मेटाडेटा और सांख्यिकीय रिपोर्ट शामिल हैं जिनमें सांख्यिकीय तालिकाएं, लिस्टिंग और आंकड़े शामिल हैं। यूएस एफडीए के मामले में, इलेक्ट्रॉनिक कॉमन टेक्निकल डॉक्यूमेंट (ईसीटीडी) एफडीए के सेंटर फॉर बायोलॉजिक्स इवैल्यूएशन एंड रिसर्च (सीबीईआर) और सेंटर फॉर ड्रग इवैल्यूएशन एंड रिसर्च को आवेदन, संशोधन, पूरक और रिपोर्ट जमा करने का मानक प्रारूप है। सीडीईआर)। एफडीए और जापानी पीएमडीए के लिए, सीडीआईएससी मानक डेटा टेबुलेशन मॉडल (एसडीटीएम), सीडीआईएससी विश्लेषण डेटासेट मॉडल (एडीएएम) में विश्लेषण डेटा, और सीडीआईएससी डिफाइन-एक्सएमएल (ऑपरेशनल डेटा मॉडल के आधार पर) में परीक्षण मेटाडेटा में सारणीबद्ध डेटा जमा करना एक नियामक आवश्यकता है। (ओडीएम))।
इस पोस्ट में, हम प्रदर्शित करते हैं कि हम RStudio का उपयोग कैसे कर सकते हैं अमेज़न SageMaker इस तरह के नियामक सबमिशन डिलिवरेबल्स बनाने के लिए। यह पोस्ट क्लिनिकल परीक्षण प्रस्तुत करने की प्रक्रिया का वर्णन करती है, कि हम कैसे नैदानिक परीक्षण अनुसंधान डेटा को अंतर्ग्रहण कर सकते हैं, डेटा को सारणीबद्ध और विश्लेषण कर सकते हैं, और फिर सांख्यिकीय रिपोर्ट बना सकते हैं-सारांश तालिकाएं, डेटा लिस्टिंग और आंकड़े (टीएलएफ)। यह विधि फार्मास्युटिकल ग्राहकों को अपने AWS वातावरण में संग्रहीत नैदानिक डेटा से सहजता से कनेक्ट करने, R का उपयोग करके इसे संसाधित करने और नैदानिक परीक्षण अनुसंधान प्रक्रिया को तेज करने में मदद कर सकती है।
औषधि विकास प्रक्रिया
दवा विकास प्रक्रिया को मोटे तौर पर पांच प्रमुख चरणों में विभाजित किया जा सकता है, जैसा कि निम्नलिखित आकृति में दिखाया गया है।
लगभग 10 संभावित अणुओं में से एक दवा को सफल अनुमोदन प्राप्त करने में औसतन 15-1 साल और लगभग 3-10,000 बिलियन अमरीकी डालर का समय लगता है। अनुसंधान के शुरुआती चरणों (दवा खोज चरण) के दौरान, होनहार दवा उम्मीदवारों की पहचान की जाती है, जो आगे चलकर प्रीक्लिनिकल रिसर्च की ओर बढ़ते हैं। प्रीक्लिनिकल चरण के दौरान, शोधकर्ता प्रदर्शन करके दवा की विषाक्तता का पता लगाने की कोशिश करते हैं इन विट्रो में प्रयोगशाला में प्रयोग और vivo में जानवरों पर प्रयोग। प्रीक्लिनिकल परीक्षण के बाद, दवाएं नैदानिक परीक्षण अनुसंधान चरण में आगे बढ़ती हैं, जहां उनकी सुरक्षा और प्रभावकारिता का पता लगाने के लिए मनुष्यों पर उनका परीक्षण किया जाना चाहिए। शोधकर्ता नैदानिक परीक्षणों को डिजाइन करते हैं और नैदानिक परीक्षण प्रोटोकॉल में अध्ययन योजना का विवरण देते हैं। वे विभिन्न नैदानिक अनुसंधान चरणों को परिभाषित करते हैं- छोटे चरण 1 अध्ययनों से दवा सुरक्षा और खुराक निर्धारित करने के लिए, दवा प्रभावकारिता और साइड इफेक्ट निर्धारित करने के लिए बड़े चरण 2 परीक्षणों तक, दवा प्रभावकारिता, सुरक्षा और निर्धारित करने के लिए चरण 3 और 4 परीक्षणों को भी बड़ा करना। प्रतिकूल प्रतिक्रियाओं की निगरानी। सफल मानव नैदानिक परीक्षणों के बाद, दवा प्रायोजक दवा के विपणन के लिए एक नई दवा आवेदन (एनडीए) दायर करता है। नियामक एजेंसियां सभी डेटा की समीक्षा करती हैं, प्रिस्क्रिप्शन लेबलिंग जानकारी पर प्रायोजक के साथ काम करती हैं और दवा को मंजूरी देती हैं। दवा की मंजूरी के बाद, नियामक एजेंसियां पूरे उत्पाद की सुरक्षा सुनिश्चित करने के लिए बाजार के बाद की सुरक्षा रिपोर्ट की समीक्षा करती हैं।
1997 में, क्लिनिकल डेटा इंटरचेंज स्टैंडर्ड्स कंसोर्टियम (CDISC), एक वैश्विक, गैर-लाभकारी संगठन, जिसमें फार्मास्युटिकल कंपनियां, CRO, बायोटेक, शैक्षणिक संस्थान, स्वास्थ्य सेवा प्रदाता और सरकारी एजेंसियां शामिल हैं, को स्वयंसेवी समूह के रूप में शुरू किया गया था। सीडीआईएससी ने सबमिशन के माध्यम से संग्रह से डेटा के प्रवाह को सुव्यवस्थित करने के लिए डेटा मानकों को प्रकाशित किया है, और भागीदारों और प्रदाताओं के बीच डेटा इंटरचेंज की सुविधा प्रदान की है। सीडीआईएससी ने निम्नलिखित मानकों को प्रकाशित किया है:
- CDASH (क्लिनिकल डेटा एक्विजिशन स्टैंडर्ड्स हार्मोनाइजेशन) - एकत्रित डेटा के लिए मानक
- एसडीटीएम (अध्ययन डेटा सारणीकरण मॉडल) - सारणीबद्ध डेटा जमा करने के मानक
- एडीएएम (विश्लेषण डेटा मॉडल) - विश्लेषण डेटा के लिए मानक
- भेजें (गैर-नैदानिक डेटा के आदान-प्रदान के लिए मानक) - गैर-नैदानिक डेटा के लिए मानक
- पीआरएम (प्रोटोकॉल प्रतिनिधित्व मॉडल) - प्रोटोकॉल के लिए मानक
ये मानक प्रशिक्षित समीक्षकों को मानक टूल का उपयोग करके डेटा का अधिक प्रभावी ढंग से और तेज़ी से विश्लेषण करने में मदद कर सकते हैं, जिससे दवा अनुमोदन समय कम हो जाता है। एसडीटीएम प्रारूप का उपयोग करके सभी सारणीबद्ध डेटा जमा करने के लिए यूएस एफडीए और जापानी पीएमडीए से यह एक नियामक आवश्यकता है।
नैदानिक परीक्षण अनुसंधान प्रस्तुतियाँ के लिए आर
एसएएस और आर फार्मास्युटिकल उद्योग के भीतर उपयोग किए जाने वाले दो सबसे अधिक उपयोग किए जाने वाले सांख्यिकीय विश्लेषण सॉफ्टवेयर हैं। जब सीडीआईएससी द्वारा एसडीटीएम मानकों का विकास शुरू किया गया था, एसएएस फार्मास्युटिकल उद्योग और एफडीए में लगभग सार्वभौमिक उपयोग में था। हालाँकि, R आजकल जबरदस्त लोकप्रियता प्राप्त कर रहा है क्योंकि यह खुला स्रोत है, और नए पैकेज और पुस्तकालय लगातार जोड़े जाते हैं। छात्र मुख्य रूप से अपने अकादमिक और शोध के दौरान आर का उपयोग करते हैं, और वे इस परिचितता को आर के साथ अपनी नौकरी में ले जाते हैं। आर उभरती प्रौद्योगिकियों जैसे उन्नत गहन शिक्षण एकीकरण के लिए भी समर्थन प्रदान करता है।
एडब्ल्यूएस जैसे क्लाउड प्रदाता अब फार्मास्युटिकल ग्राहकों के लिए अपने बुनियादी ढांचे की मेजबानी करने के लिए पसंद का मंच बन गए हैं। एडब्ल्यूएस सेजमेकर जैसी प्रबंधित सेवाएं भी प्रदान करता है, जो क्लाउड में मशीन लर्निंग (एमएल) मॉडल बनाने, प्रशिक्षित करने और तैनात करने में आसान बनाता है। सेजमेकर वेब ब्राउज़र के माध्यम से कहीं से भी RStudio IDE तक पहुंच की अनुमति देता है। इस पोस्ट में बताया गया है कि कैसे सांख्यिकीय प्रोग्रामर और बायोस्टैटिस्टियन अपने नैदानिक डेटा को R वातावरण में अंतर्ग्रहण कर सकते हैं, R कोड कैसे चलाया जा सकता है, और परिणाम कैसे संग्रहीत किए जाते हैं। हम कोड के स्निपेट प्रदान करते हैं जो नैदानिक परीक्षण डेटा वैज्ञानिकों को XPT फ़ाइलों को R वातावरण में अंतर्ग्रहण करने, SDTM और ADaM के लिए R डेटा फ़्रेम बनाने और अंत में TLF बनाने की अनुमति देते हैं जिसे एक में संग्रहीत किया जा सकता है अमेज़न सरल भंडारण सेवा (अमेज़ॅन S3) ऑब्जेक्ट स्टोरेज बकेट।
सेजमेकर पर RStudio
2 नवंबर, 2021 को, AWS ने के सहयोग से आरस्टूडियो पीबीसी की घोषणा की सामान्य उपलब्धता सेजमेकर पर RStudio, क्लाउड में उद्योग का पहला पूरी तरह से प्रबंधित RStudio कार्यक्षेत्र IDE। अब आप अपना वर्तमान RStudio लाइसेंस ला सकते हैं ताकि कुछ आसान चरणों में अपने स्व-प्रबंधित RStudio वातावरण को SageMaker में आसानी से माइग्रेट कर सकें। इस रोमांचक सहयोग के बारे में अधिक जानने के लिए, देखें Amazon SageMaker पर RStudio की घोषणा.
RStudio वर्कबेंच के साथ, R डेवलपर्स के लिए RStudio सुइट RStudio Connect और RStudio पैकेज मैनेजर भी प्रदान करता है। RStudio Connect को डेटा वैज्ञानिकों को अंतर्दृष्टि, डैशबोर्ड और वेब एप्लिकेशन प्रकाशित करने की अनुमति देने के लिए डिज़ाइन किया गया है. यह डेटा वैज्ञानिकों के जटिल काम से एमएल और डेटा विज्ञान अंतर्दृष्टि साझा करना आसान बनाता है और इसे निर्णय निर्माताओं के हाथों में रखता है। RStudio Connect व्यापक खपत के लिए होस्टिंग और सामग्री को सरल और स्केलेबल बनाता है।
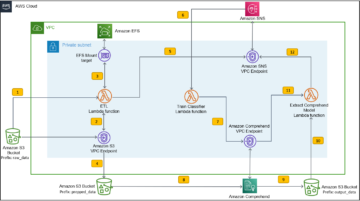
समाधान अवलोकन
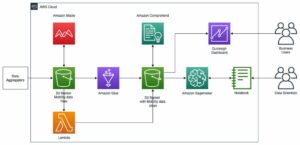
निम्नलिखित अनुभागों में, हम चर्चा करते हैं कि हम SageMaker पर RStudio में एक दूरस्थ रिपॉजिटरी या S3 बकेट से कच्चे डेटा को कैसे आयात कर सकते हैं। से सीधे जुड़ना भी संभव है अमेज़न रिलेशनल डेटाबेस सर्विस (अमेज़ॅन आरडीएस) और डेटा वेयरहाउस जैसे अमेज़न रेडशिफ्ट (देखें R को Amazon Redshift के साथ जोड़ना) सीधे RStudio से; हालाँकि, यह इस पोस्ट के दायरे से बाहर है। दो अलग-अलग स्रोतों से डेटा अंतर्ग्रहण करने के बाद, हम इसे संसाधित करते हैं और एक तालिका के लिए R डेटा फ़्रेम बनाते हैं। फिर हम टेबल डेटा फ्रेम को RTF फाइल में बदलते हैं और परिणामों को वापस S3 बकेट में स्टोर करते हैं। इन आउटपुट को संभावित रूप से नियामक सबमिशन उद्देश्यों के लिए उपयोग किया जा सकता है, बशर्ते पोस्ट में उपयोग किए गए आर पैकेज ग्राहक द्वारा नियामक सबमिशन के उपयोग के लिए मान्य किए गए हों।
सेजमेकर पर RStudio सेट करें
अपने परिवेश में सेजमेकर पर RStudio स्थापित करने के निर्देशों के लिए, देखें सेजमेकर पर RStudio के साथ शुरुआत करें. सुनिश्चित करें कि SageMaker पर RStudio की निष्पादन भूमिका के पास S3 बकेट में डेटा डाउनलोड और अपलोड करने की पहुंच है जिसमें डेटा संग्रहीत है। R संकुल को कैसे प्रबंधित करें और SageMaker पर RStudio का उपयोग करके अपने विश्लेषण को प्रकाशित करने के तरीके के बारे में अधिक जानने के लिए, देखें डेटा वैज्ञानिकों के लिए सेजमेकर पर पूरी तरह से प्रबंधित RStudio की घोषणा.
RStudio में डेटा डालें
इस चरण में, हम अपने R सत्र के लिए इसे उपलब्ध कराने के लिए विभिन्न स्रोतों से डेटा अंतर्ग्रहण करते हैं। हम एसएएस एक्सपीटी प्रारूप में डेटा आयात करते हैं; हालाँकि, यदि आप अन्य स्वरूपों में डेटा अंतर्ग्रहण करना चाहते हैं, तो प्रक्रिया समान है। SageMaker पर RStudio का उपयोग करने के लाभों में से एक यह है कि यदि स्रोत डेटा आपके AWS खातों में संग्रहीत है, तो SageMaker मूल रूप से डेटा का उपयोग करके एक्सेस कर सकता है AWS पहचान और अभिगम प्रबंधन (आईएएम) भूमिकाएं।
रिमोट रिपोजिटरी में संग्रहीत डेटा तक पहुंचें
इस चरण में, हम ADaM डेटा आयात करते हैं FDA का GitHub रिपॉजिटरी. हम एक स्थानीय निर्देशिका बनाते हैं जिसे कहा जाता है data डेटा को स्टोर करने और जनसांख्यिकी डेटा डाउनलोड करने के लिए RStudio वातावरण में (dm.xpt) दूरस्थ भंडार से। इस संदर्भ में, स्थानीय निर्देशिका आपके निजी अमेज़ॅन ईएफएस स्टोरेज पर बनाई गई निर्देशिका को संदर्भित करती है जो डिफ़ॉल्ट रूप से आपके आर सत्र पर्यावरण से जुड़ी होती है। निम्नलिखित कोड देखें:
जब यह चरण पूरा हो जाए, तो आप देख सकते हैं dm.xpt पर नेविगेट करके डाउनलोड किया जा रहा है फ़ाइलें, तिथि, डीएम.एक्सपीटी.
Amazon S3 में संग्रहीत डेटा एक्सेस करें
इस चरण में, हम अपने खाते में S3 बकेट में संग्रहीत डेटा डाउनलोड करते हैं। हमने FDA के GitHub रिपॉजिटरी से S3 बकेट नाम की सामग्री की प्रतिलिपि बनाई है aws-sagemaker-rstudio इस उदाहरण के लिए। निम्नलिखित कोड देखें:
जब चरण पूरा हो जाए, तो आप देख सकते हैं pp.xpt पर नेविगेट करके डाउनलोड किया जा रहा है फ़ाइलें, तिथि, पीपी.एक्सपीटी.
प्रक्रिया XPT डेटा
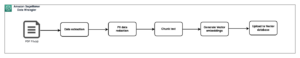
अब जब हमारे पास R परिवेश में SAS XPT फ़ाइलें उपलब्ध हैं, तो हमें उन्हें R डेटा फ़्रेम में बदलने और उन्हें संसाधित करने की आवश्यकता है। हम उपयोग करते हैं haven XPT फ़ाइलों को पढ़ने के लिए पुस्तकालय। हम सीडीआईएससी एसडीटीएम डेटासेट मर्ज करते हैं dm और pp ADPP डेटासेट बनाने के लिए। फिर हम ADPP डेटा फ्रेम का उपयोग करके एक सारांश सांख्यिकीय तालिका बनाते हैं। सारांश तालिका तब आरटीएफ प्रारूप में निर्यात की जाती है।
सबसे पहले, XPT फाइलें का उपयोग करके पढ़ी जाती हैं read_xpt हेवन लाइब्रेरी का कार्य। फिर का उपयोग करके एक विश्लेषण डेटासेट बनाया जाता है sqldf का कार्य sqldf पुस्तकालय। निम्नलिखित कोड देखें:
फिर, से फ़ंक्शन का उपयोग करके एक आउटपुट डेटा फ़्रेम बनाया जाता है Tplyr और dplyr पुस्तकालय:
आउटपुट डेटा फ़्रेम को तब RStudio परिवेश में आउटपुट फ़ोल्डर में RTF फ़ाइल के रूप में संग्रहीत किया जाता है:
Amazon S3 पर आउटपुट अपलोड करें
आउटपुट जनरेट होने के बाद, हम डेटा को वापस S3 बकेट में डालते हैं। हम इसे फिर से सेजमेकर सत्र बनाकर प्राप्त कर सकते हैं, यदि कोई सत्र पहले से सक्रिय नहीं है, और आउटपुट फ़ोल्डर की सामग्री को S3 बाल्टी में अपलोड करने का उपयोग कर रहा है session$upload_data समारोह:
इन चरणों के साथ, हमने डेटा को अंतर्ग्रहण किया है, इसे संसाधित किया है, और परिणामों को नियामक अधिकारियों को प्रस्तुत करने के लिए उपलब्ध कराया है।
क्लीन अप
किसी भी अनपेक्षित लागत से बचने के लिए, आपको अपना वर्तमान सत्र छोड़ना होगा। पृष्ठ के ऊपरी दाएं कोने पर, पावर आइकन चुनें। यह स्वचालित रूप से अंतर्निहित उदाहरण को रोक देगा और इसलिए किसी भी अनपेक्षित गणना लागत को रोकना बंद कर देगा।
चुनौतियां
पोस्ट में S3 बकेट में या किसी दूरस्थ रिपॉजिटरी से संग्रहीत कच्चे डेटा को अंतर्ग्रहण करने के चरणों की रूपरेखा दी गई है। हालांकि, नैदानिक परीक्षण के लिए कच्चे डेटा के कई अन्य स्रोत हैं, मुख्य रूप से eCRF (इलेक्ट्रॉनिक केस रिपोर्ट फॉर्म) डेटा EDC (इलेक्ट्रॉनिक डेटा कैप्चर) सिस्टम में संग्रहीत है जैसे कि Oracle क्लिनिकल, मेडिडेटा रेव, ओपनक्लिनिका, या स्नोफ्लेक; प्रयोगशाला डेटा; eCOA (नैदानिक परिणाम मूल्यांकन) और ePRO (इलेक्ट्रॉनिक रोगी-रिपोर्ट किए गए परिणाम) से डेटा; ऐप्स और चिकित्सा उपकरणों से वास्तविक दुनिया का डेटा; और अस्पतालों में इलेक्ट्रॉनिक स्वास्थ्य रिकॉर्ड (ईएचआर)। इस डेटा को नियामक सबमिशन के लिए प्रयोग करने योग्य बनाने से पहले महत्वपूर्ण प्रीप्रोसेसिंग शामिल है। विभिन्न डेटा स्रोतों से कनेक्टर्स बनाना और उन्हें एक केंद्रीकृत डेटा रिपॉजिटरी (सीडीआर) या क्लिनिकल डेटा लेक में एकत्रित करना, जबकि उचित पहुंच नियंत्रण बनाए रखना, महत्वपूर्ण चुनौतियों का सामना करता है।
दूर करने के लिए एक अन्य महत्वपूर्ण चुनौती नियामक अनुपालन की है। नियामक सबमिशन आउटपुट बनाने के लिए उपयोग किया जाने वाला कंप्यूटर सिस्टम उपयुक्त नियमों के अनुरूप होना चाहिए, जैसे कि 21 सीएफआर भाग 11, एचआईपीएए, जीडीपीआर, या कोई अन्य जीएक्सपी आवश्यकताएं या आईसीएच दिशानिर्देश। यह एक मान्य और योग्य वातावरण में काम करने के लिए अनुवाद करता है जिसमें पहुंच, सुरक्षा, बैकअप और ऑडिटेबिलिटी के नियंत्रण होते हैं। इसका मतलब यह भी है कि कोई भी आर पैकेज जो नियामक सबमिशन आउटपुट बनाने के लिए उपयोग किया जाता है, उसे उपयोग करने से पहले मान्य किया जाना चाहिए।
निष्कर्ष
इस पोस्ट में, हमने देखा कि ईसीटीडी सबमिशन के लिए कुछ प्रमुख डिलिवरेबल्स सीडीआईएससी एसडीटीएम, एडीएएम डेटासेट और टीएलएफ थे। इस पोस्ट ने SageMaker पर RStudio में कुछ स्रोतों से डेटा को पहले अंतर्ग्रहण करके इन नियामक सबमिशन डिलिवरेबल्स को बनाने के लिए आवश्यक कदमों को रेखांकित किया। फिर हमने देखा कि कैसे हम अंतर्ग्रहीत डेटा को XPT स्वरूप में संसाधित कर सकते हैं; एसडीटीएम, एडीएएम और टीएलएफ बनाने के लिए इसे आर डेटा फ्रेम में परिवर्तित करें; और फिर अंत में परिणामों को S3 बकेट में अपलोड करें।
हमें उम्मीद है कि पोस्ट में दिए गए व्यापक विचारों के साथ, सांख्यिकीय प्रोग्रामर और बायोस्टैटिस्टियन आसानी से सेजमेकर पर RStudio में नैदानिक परीक्षण अनुसंधान डेटा को लोड करने, संसाधित करने और विश्लेषण करने की एंड-टू-एंड प्रक्रिया की कल्पना कर सकते हैं और एक कस्टम को परिभाषित करने के लिए सीखने का उपयोग कर सकते हैं। आपके नियामक सबमिशन के लिए उपयुक्त वर्कफ़्लो।
क्या आप शोधकर्ताओं, सांख्यिकीविदों और R प्रोग्रामर्स को उनके जीवन को आसान बनाने में मदद करने के लिए RStudio का उपयोग करने के किसी अन्य एप्लिकेशन के बारे में सोच सकते हैं? हमें आपके विचारों के बारे में सुनना अच्छा लगेगा! और यदि आपके कोई प्रश्न हैं, तो कृपया उन्हें टिप्पणी अनुभाग में साझा करें।
उपयुक्त संसाधन चुनें
अधिक जानकारी के लिए, निम्न लिंक पर जाएँ:
लेखक के बारे में
 रोहित बंगा लंदन, यूके में स्थित एक वैश्विक नैदानिक विकास उद्योग विशेषज्ञ है। वह प्रशिक्षण द्वारा एक जैव सांख्यिकीविद् हैं और हेल्थकेयर और लाइफसाइंस ग्राहकों को एडब्ल्यूएस पर अभिनव नैदानिक विकास समाधान तैनात करने में मदद करते हैं। हेल्थकेयर और लाइफसाइंस उद्योग के भीतर वास्तविक व्यावसायिक समस्याओं को हल करने के लिए डेटा साइंस, एआई / एमएल और उभरती प्रौद्योगिकियों का उपयोग कैसे किया जा सकता है, इस बारे में उनका जुनून है। अपने खाली समय में, रोहित स्कीइंग, बारबेक्यूइंग और परिवार और दोस्तों के साथ समय बिताने का आनंद लेते हैं।
रोहित बंगा लंदन, यूके में स्थित एक वैश्विक नैदानिक विकास उद्योग विशेषज्ञ है। वह प्रशिक्षण द्वारा एक जैव सांख्यिकीविद् हैं और हेल्थकेयर और लाइफसाइंस ग्राहकों को एडब्ल्यूएस पर अभिनव नैदानिक विकास समाधान तैनात करने में मदद करते हैं। हेल्थकेयर और लाइफसाइंस उद्योग के भीतर वास्तविक व्यावसायिक समस्याओं को हल करने के लिए डेटा साइंस, एआई / एमएल और उभरती प्रौद्योगिकियों का उपयोग कैसे किया जा सकता है, इस बारे में उनका जुनून है। अपने खाली समय में, रोहित स्कीइंग, बारबेक्यूइंग और परिवार और दोस्तों के साथ समय बिताने का आनंद लेते हैं।
 जॉर्जियोस शिनास ईएमईए क्षेत्र में एआई/एमएल के लिए एक विशेषज्ञ समाधान वास्तुकार है। वह लंदन में स्थित है और यूके और आयरलैंड में ग्राहकों के साथ मिलकर काम करता है। जॉर्जियो ग्राहकों को एमएलओपीएस प्रथाओं में विशेष रुचि के साथ एडब्ल्यूएस पर उत्पादन में मशीन लर्निंग एप्लिकेशन को डिजाइन और तैनात करने में मदद करता है और ग्राहकों को बड़े पैमाने पर मशीन लर्निंग करने में सक्षम बनाता है। अपने खाली समय में, वह यात्रा करना, खाना बनाना और दोस्तों और परिवार के साथ समय बिताना पसंद करते हैं।
जॉर्जियोस शिनास ईएमईए क्षेत्र में एआई/एमएल के लिए एक विशेषज्ञ समाधान वास्तुकार है। वह लंदन में स्थित है और यूके और आयरलैंड में ग्राहकों के साथ मिलकर काम करता है। जॉर्जियो ग्राहकों को एमएलओपीएस प्रथाओं में विशेष रुचि के साथ एडब्ल्यूएस पर उत्पादन में मशीन लर्निंग एप्लिकेशन को डिजाइन और तैनात करने में मदद करता है और ग्राहकों को बड़े पैमाने पर मशीन लर्निंग करने में सक्षम बनाता है। अपने खाली समय में, वह यात्रा करना, खाना बनाना और दोस्तों और परिवार के साथ समय बिताना पसंद करते हैं।
- AI
- ai कला
- ऐ कला जनरेटर
- ऐ रोबोट
- अमेज़न SageMaker
- अमेज़न सिंपल स्टोरेज सर्विस (S3)
- कृत्रिम बुद्धिमत्ता
- कृत्रिम बुद्धिमत्ता प्रमाणन
- बैंकिंग में आर्टिफिशियल इंटेलिजेंस
- आर्टिफिशियल इंटेलिजेंस रोबोट
- आर्टिफिशियल इंटेलिजेंस रोबोट
- कृत्रिम बुद्धि सॉफ्टवेयर
- AWS मशीन लर्निंग
- blockchain
- ब्लॉकचेन सम्मेलन एआई
- कॉइनजीनियस
- संवादी कृत्रिम बुद्धिमत्ता
- क्रिप्टो सम्मेलन एआई
- दल-ए
- ध्यान लगा के पढ़ना या सीखना
- इसे गूगल करें
- इंटरमीडिएट (200)
- जीवन विज्ञान
- यंत्र अधिगम
- प्लेटो
- प्लेटो एआई
- प्लेटो डेटा इंटेलिजेंस
- प्लेटो गेम
- प्लेटोडाटा
- प्लेटोगेमिंग
- स्केल एआई
- वाक्यविन्यास
- जेफिरनेट