Az életkorral összefüggő makuladegeneráció (AMD) a vakság vezető oka. Megindul a külső vér-retina-gáton (oBRB), amelyet a retina pigment epitélium (RPE), a Bruch-membrán és a choriocapillaris alkot. A fiziológiailag releváns humán oBRB modellek hiánya miatt az AMD kiindulási és progressziós mechanizmusait még jobban meg kell érteni.
A National Eye Institute (NEI) kutatócsoportja, amely a National Institutes of Health része, pácienst használt fel őssejtek és 3D bioprinting szemszövet előállítására, amely elősegíti a vakító betegségek mechanizmusának megértését. A tudósok olyan sejtek kombinációját nyomtatták ki, amelyek a külső vér-retina gátat alkotják.
A retina pigment epithelium (RPE), amelyet a vérerekben gazdag choriocapillaristól választ el Bruch membránja, a külső vér-retina gátat alkotja. A choriocapillaris és az RPE tápanyagokat és hulladékot cserélnek a Bruch-membrán ellenőrzése alatt. A Drusen, amelyek lipoprotein felhalmozódást jelentenek, a Bruch-membránon kívül fejlődnek ki AMD-ben, és akadályozzák annak működését. Az RPE lebomlása idővel a fotoreceptorok romlását és látásvesztést okoz.
A tudósok három éretlen érhártya sejttípust kombináltak egy hidrogélben: pericitákat, endothel sejteket és fibroblasztokat. Ezután egy biológiailag lebomló állványra nyomtatták a gélt. A sejtek napokon belül elkezdtek sűrű kapillárishálózattá érni.
A kilencedik napon a tudósok a retina pigment epiteliális sejtjeit ültették az állvány másik oldalára. A nyomtatott szövet a 42. napon érte el a teljes érettséget. A szövetelemzések, valamint a genetikai és funkcionális vizsgálatok azt mutatták, hogy a nyomtatott szövet a natív külső vér-retina gáthoz hasonlóan nézett ki és viselkedik.
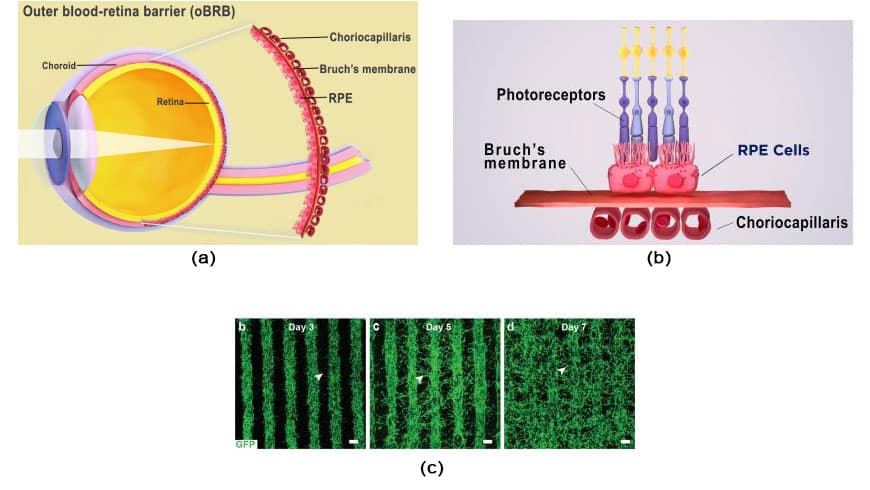
b. A szem külső vér-retina gátja a retina pigmenthámjából, a Bruch-membránból és a choriocapillarisból áll. A kép forrása: National Eye Institute.
c. Az erek növekedése az endothel-pericita-fibroblaszt sejtkeverék nyomtatott sorain keresztül. A 7. napon az erek kitöltik a sorok közötti teret, és kapillárisok hálózatát alkotják. A kép jóváírása: Kapil Bharti.
Amikor stressznek voltak kitéve, a nyomtatott szövetek korai stádiumú AMD-jellemzőket mutattak, például drusen-lerakódásokat az RPE alatt, és a késői stádiumú száraz stádiumú AMD-vé fejlődtek, ahol a szövetek lebomlását észlelték. Az alacsony oxigénszint nedves AMD-szerű megjelenést okozott az érhártya vaszkuláris hiperproliferációjával, amely az RPE alatti zónába költözött. Az AMD kezelésére alkalmazva az anti-VEGF gyógyszerek lassították az erek képződését és migrációját, miközben javították a szövetek alakját is.
Kapil Bharti, Ph.D., a NEI Szemészeti és Őssejt-transzlációs kutatásokkal foglalkozó szekciójának vezetője elmondta: „A sejtek nyomtatásával elősegítjük a normál külső vér-retina gát anatómiájához szükséges sejtjelek cseréjét. Például az RPE sejtek jelenléte indukálja génexpresszió a fibroblasztokban bekövetkező változások, amelyek hozzájárulnak a Bruch-membrán kialakulásához – ezt sok évvel ezelőtt javasolták, de modellünkig nem bizonyították.”
A tudósok két technológiai kérdéssel foglalkoztak: megfelelő biológiailag lebomló állvány létrehozásával és egységes nyomtatási mintázattal. Kifejlesztettek egy hőmérséklet-érzékeny hidrogélt, amely külön sorokat hozott létre, amíg a gél hideg volt, de feloldódott, amikor a gél felmelegedett. A szöveti architektúra pontosabb értékelési rendszerét a jó sorkonzisztencia tette lehetővé. Ezenkívül optimalizálták a fibroblasztok, endoteliális sejtek és periciták arányát a sejtkombinációban.
Marc Ferrer társszerző, Ph.D., az NIH Nemzeti Transzlációs Tudományok Központja 3D Tissue Bioprinting Laboratóriumának igazgatója és csapata szakértelmet biztosított a külső vér-retina gát szöveteinek „kútban” történő biogyártásában, ” elemző mérésekkel együtt, amelyek lehetővé teszik a gyógyszerszűrést.
[Beágyazott tartalmat]
"Együttműködési erőfeszítéseink a degeneratív szembetegségek nagyon releváns retinaszövet-modelljeit eredményezték" - mondta Ferrer mondott. "Az ilyen szövetmodellek számos potenciális felhasználási lehetőséget kínálnak a transzlációs alkalmazásokban, beleértve a terápiás fejlesztéseket is."
Journal Reference:
- Min Jae Song, Russ Quinn és társai. A bionyomtatott 3D külső retina gát RPE-függő choroidális fenotípust tár fel előrehaladott makuladegenerációban. Természeti módszerek, 2022; DOI: 10.1038/s41592-022-01701-1