A protonterápia nagymértékben konform dóziseloszlást tud biztosítani a tumor célpontjához, miközben minimalizálja a dózist a céltérfogaton kívüli szövetekben. Ezt az erősséget megvalósító kezelési tervek elkészítése a dozimetrikusok és orvosfizikusok elsődleges prioritása.
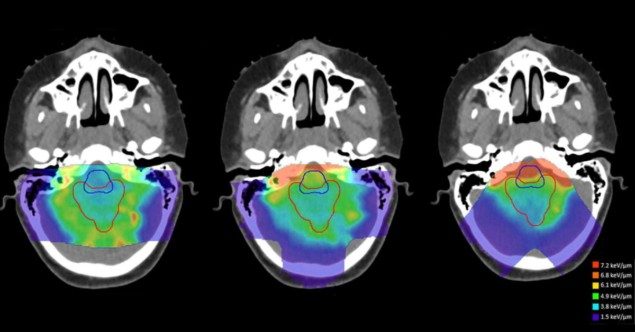
A protonok alapvetően más módon adják le a dózist, mint a röntgensugárzás, a külső sugárterápia egy másik fajtája. Ahogy egy proton eléri pályája végét, növekszik az energiája szövetbe történő átvitelének sebessége – lineáris energiaátvitele (LET), keV/µm-ben kifejezve.
A relatív biológiai hatékonyság (RBE) megragadja a növekvő LET biológiai következményeit, és a klinikai protonkezeléseknél gyakran alkalmaznak fix 1.1-es RBE értéket. A proton RBE azonban sok más tényezőtől is függ, beleértve a klinikai végpontokat, a szövettípust, a frakcionálási sémát, a betegspecifikus sugárérzékenységet, a fizikai dózist és a kísérleti mérések bizonytalanságait. Ennek eredményeként a fix RBE-érték használata a protonterápiában valószínűleg alábecsüli az RBE-t a magas LET-tartományban, ami a sugárzás által kiváltott toxicitások fokozott kockázatát eredményezheti.
Ennek ellenére a LET erősen korrelál az RBE-vel, és kulcsfontosságú tényező a változó RBE meghatározásában a protonterápiában. Mint ilyen, a kutatók a LET kiszámításának és értékelésének módszereit vizsgálják a kezelés tervezése során. Ezek a biológiai kezeléstervezési eszközök azonban korlátozottak, és amíg ki nem fejlesztik és tovább nem tanulmányozzák őket, a klinikáknak meg kell határozniuk saját kezelési tervezési gyakorlatukat, hogy minimalizálják az LET-t a célmennyiségeken kívül. Austin Faught, orvosfizikus at Szent Jude Gyermekkutató Kórház Tennessee-ben.
„A [LET-eloszlás] befolyásolása aktív kutatási terület, és néhány nagyszerű módszer fejlesztés alatt áll” – magyarázza Faught. „Az a probléma, amellyel szembe kell néznünk, hogy ezek nem állnak rendelkezésre egyszerűen házon belül kifejlesztett egyedi szoftverek vagy a gyártók által biztosított alkalmazások speciális kutatási változatai nélkül… [és] kevés olyan tanulmány létezik, amely kvantitatív útmutatást adna arra vonatkozóan, hogy mire kell törekednünk.”
A kezelés tervezési stratégiái
A LET-alapú tervértékelés és a fotonterápia optimalizálása felé tett lépésként Faught és csapata felmérést végzett azokról a tervezési stratégiákról, amelyek kereskedelmi forgalomban elérhetőek a klinikai csapatok számára az intenzitásmodulált protonterápia (IMPT) számára. Tanulmányuk, amelyről a Journal of Applied Clinical Medical Physics, bemutat néhány útmutatást a protonterápiás kezelést tervezők számára. „Szerettünk volna megvizsgálni néhány könnyen elérhető kezelési tervezési technikát, és azt, hogy ezek hogyan befolyásolhatják a LET-t” – magyarázza Faught.
A kutatók értékelték a dózissal súlyozott LET (LETd) nyolc előremutató kezelési tervezési megközelítés között, amelyeket egy hengeres vízfantomnál alkalmaztak, és négy gyermekkori agydaganatos esetet (Faught megjegyzi, hogy a sugárzás által kiváltott toxicitás a csoport fókuszterülete). Összehasonlították ezeket a tervezési stratégiákat egy ellentétes oldalsó sugárnyalábokat használó tervvel (a fantom esetében) vagy az eredeti klinikai tervvel (a betegek esetében), Monte Carlo másodlagos számításokat használva a dózis és a LET értékelésére.d.
A kutatók azt találták, hogy a kezelési terület geometriája járult hozzá a legnagyobb mértékben a magas LET-területek elhelyezkedéséhez. A magas LET-hez kapcsolódó biológiai bizonytalanságok lehetséges hatásainak mérséklésed, azt javasolják, hogy a kezelést tervezők nagy metszésszögeket alkalmazzanak a kezelési gerendák között, és kerüljék azokat a sugarakat, amelyek azonnal megállnak a kritikus szerkezetek közelében.
„Ez nagyszerű hír, mivel azt jelenti, hogy a kezelési területek számának gondos kiválasztása és a közeli egészségügyi szövetekhez való tájolásuk hatékony lehet” – mondja Faught. "Néhány tudatos, előzetes gondolkodással ezt minden kezelést tervező figyelembe veheti a tervezési folyamat során."
A kutatók azt is megállapították, hogy a tartományváltó használata jelentősen csökkentette az átlagos LET-etd a klinikai céltérfogatban. Ennek eredményeként azt javasolják, hogy a távolságváltókat és az alternatív helymeghatározási stratégiákat takarékosan használják, és csak akkor, ha a klinikák ki tudják számítani a kapott LET-et.d az alternatív tervezési stratégiák összehasonlítására.
A vizsgálat kis mintája miatt a kutatók nem tudtak egyértelmű tendenciát megállapítani a LET-bend eltérések a klinikai esetekben. Nem értékelték a kapcsolatot a LET változásai és a tumorkontroll vagy a normál szöveti szövődmények valószínűségének változása között.
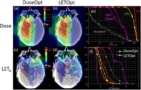
A LET-alapú tervek optimalizálják a protonterápiát
Míg az egyes tervezési megközelítések hatása a magas LET régiókra szerény volt, Faught szerint fontos felismerni, hogy a csapat kezelési tervezési stratégiái és ajánlásai bizonyítékokon alapulnak, és könnyen bedolgozhatók a klinikai gyakorlatba.
„Remélem, az egyik elvihető, hogy nekünk, mint területnek hasznára válnának azok a kereskedelmi eszközök, amelyek lehetővé teszik a kezeléstervezési rendszeren belül a LET kiszámítását. Még jobb, ha szeretnénk, ha a LET szem előtt tartásával optimalizálhatnánk. Ez a tanulmány jó híd volt mindaddig, amíg ezek az eszközök szélesebb körben elérhetővé nem válnak” – mondja Faught.