A részecsketerápia – a protonok vagy nehezebb ionok nyalábjaival végzett rákkezelés – nagymértékben megfelelő dózisbejuttatást és a normál szövetek nagyobb megkímélését biztosítja, mint a hagyományos foton-alapú sugárterápia. A hosszú távú ráktúlélők esetében azonban fontos a sugárzás által kiváltott másodlagos rák (SC) kockázata, amelyet figyelembe kell venni a kezelési mód kiválasztásakor.
Mivel az újabb kezelésekhez, például a proton- és szénion-terápiához kevés epidemiológiai adat áll rendelkezésre, egy csapat a GSI Helmholtz Nehézionkutatási Központ modellt fejleszt az SC-kockázatok összehasonlítására a részecsketerápiás módok között. A modell, leírta Antónia Hufnagl és a kollégák Orvosi fizika, végül beépíthető a kezelési tervezési rendszerekbe, hogy az SC kockázatát további optimalizálási kritériumként beépítsék.
Halálos versus rákkeltő események
Az SC kockázati modellek jellemzően úgy működnek, hogy figyelembe veszik a sejtpusztulás (amely a rák elnyomásához vezet) és a sejttranszformáció (a végül rákhoz vezető mutációk kiváltása) közötti egyensúlyt. Annak valószínűségét, hogy egy besugárzott térfogatban rák alakul ki, a lineáris-kvadratikus (LQ) modell segítségével határozzuk meg, amely egyszerű összefüggést ad a sejt túlélése és a leadott fotondózis között.
Ebben a tanulmányban a kutatók a lokális hatásmodellt (LEM) használták a részecsketerápia utáni SC-indukció relatív biológiai hatékonyságának (RBE) előrejelzésére. A részecskesugárzás megnövekedett RBE-jének figyelembe vétele érdekében a kockázati modell foton LQ paramétereit a LEM által megjósolt ion-nyaláb LQ paraméterekkel helyettesítették. Megközelítésük kulcsfontosságú jellemzője a LEM használata a sejtpusztítás és a rák kiváltása szempontjából.

„A LEM kettős használata az SC fejlődését meghatározó két fő folyamat, nevezetesen a sejttranszformáció és a sejtpusztulás közötti versengést tükrözi” – magyarázza a vezető szerző. Michael Scholz. „A dózis és/vagy a hatékonyság növelésével a sejtpusztítás elnyomhatja a transzformált sejtek életképességét. Ez olyan összetett kölcsönhatáshoz vezet, amelyet másként nem lehet egyszerűen egy egylépéses eljárásban tükrözni.”
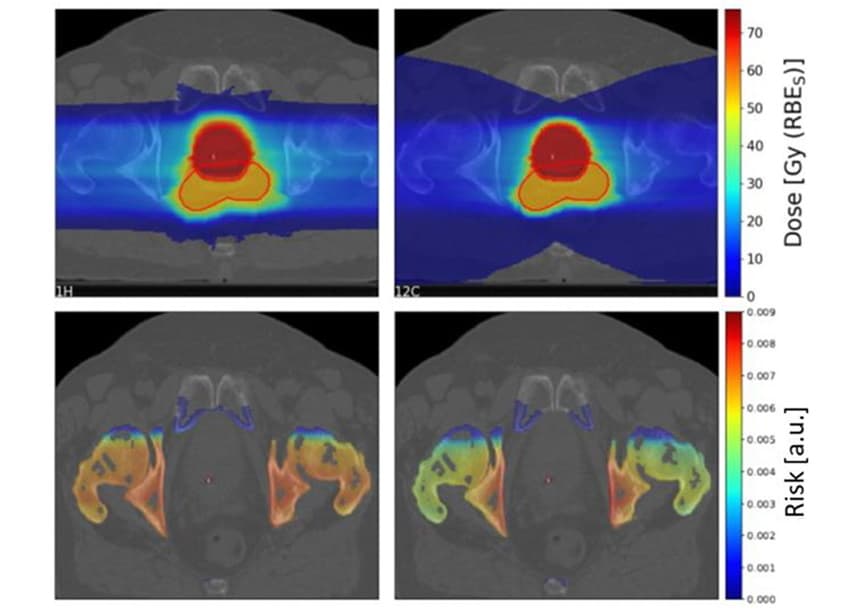
Annak vizsgálatára, hogy mely tényezők befolyásolják az SC kockázatát, a kutatók a TPS TRiP98 tervezési rendszert használták biológiailag optimalizált szén-ion- és protonkezelési tervek létrehozására idealizált geometria alapján. A tervek egy 4x4x4 cm-es célpontot sugároztak be egyetlen részecskesugárral vagy két egymással szemben lévő sugárral, a cél előtt egy 4x4x1 cm-es veszélyeztetett szervvel (OAR). A LEM bemeneteként használt foton LQ paraméterek bizonytalansága miatt a proton-szén-ion kockázati arányokat becsülték meg, nem pedig az egyéni kockázati értékeket.
Ezeknél az idealizált elrendezéseknél a modell nem mutatott egyértelmű preferenciát sem a protonok, sem a szénionok iránt, de összetett függést mutatott ki különböző paraméterektől. A szénionok csökkent oldalirányú szóródása alacsonyabb SC-kockázathoz vezet, mint a protonok a bemeneti csatornában. A szénionok azonban nagyobb dózist raknak le a célpont mögé a fragmentációs farok miatt, ami növeli a tumor mögötti OAR-ok SC kockázatát szén-ion besugárzás után.
Az egysugaras tervek esetében a teljes SC kockázat nagyjából másfélszer nagyobb volt a szénionok esetében, mint a protonok esetében. Két ellentétes nyalábbal a teljes SC kockázat 1.5-szor magasabb volt a protonok esetében, bár ez erősen változott a feltételezett érzékeny térfogat térbeli elhelyezkedésétől függően a céltérfogathoz képest.
A szövetek sugárérzékenysége (fotonokra) nagy hatással volt az SC kockázati arányára, a sugárrezisztens OAR-ek esetében előnyös volt a szén-ionos kezelés, az érzékeny OAR-ek pedig a protonnyalábokból. Ezzel szemben a frakcionálási séma csekély hatással volt a várható kockázati értékekre.
A páciens geometriája
A klinikai forgatókönyvek vizsgálata érdekében Scholz és munkatársai megbecsülték az SC kockázatát 10 prosztatarákos beteg esetében, akiket korábban fotonsugárterápiával kezeltek a Karolinska Egyetemi Kórházban. Kezelési terveket készítettek a betegek számára két oldalirányban ellentétes szkennelt proton és szén-ion mező felhasználásával.
Amint azt korábban láttuk, a szénionok fragmentációs farka nagy, alacsony dózisú területet eredményezett a cél mögött. A nagy dózisú célterület azonban jobban megfelelt a szén-ionnak, mint a protontervek.
A csapat a 10 betegnél négy OAR (hólyag, végbél, csontok és bőr) proton-szén-ion SC kockázati arányát számította ki. A csont és a bőr esetében a protontervek valamivel magasabb SC-kockázatot eredményeztek, mint a szén-ion tervek, a csontok és a bőr esetében 1.19 és 1.06 medián kockázati arány mellett. A hólyag és a végbél esetében azonban a protontervek szignifikánsan alacsonyabb SC kockázatot eredményeztek, a hólyag és a végbél kockázati aránya 0.68, illetve 0.49 volt.
A kutatók arra a következtetésre jutottak, hogy az ezzel a modellel nyert betekintések segíthetnek optimalizálni a jövőbeni kezeléseket. Jelenleg a relatív kockázati modellezés elsősorban a különböző betegcsoportok különböző kezelési forgatókönyveinek összehasonlítására alkalmas eszköz. Scholz azonban megjegyzi, hogy az ilyen modellek beépítése az egyes betegek kezelési tervezésébe egyszerű lenne.

A szén-ion rácsterápia kíméli az egészséges szöveteket
„Ehhez csak egy adott dóziseloszlás tervezését kell végrehajtani két különböző biológiai paraméterkészlettel, amelyek a sejtpusztulást, illetve a sejttranszformációs folyamatot reprezentálják” – magyarázza. "Ezután csak némi utófeldolgozásra van szükség a kapott 3D hatáseloszlások szabványos matematikai eszközökkel a megfelelő kockázati arány eloszlások származtatásához."
A következő lépés, mondja, a modell validálása a klinikai adatokkal való összehasonlítással. "Mivel jelenleg ezek az adatok szűkösek, fontos lépés lenne a megközelítés kiterjesztése a fotonkezelésekre, valamint a protonok és a fotonok, valamint a szénionok és a fotonok kockázati arányának meghatározása" - mondja Scholz. Fizika Világa.