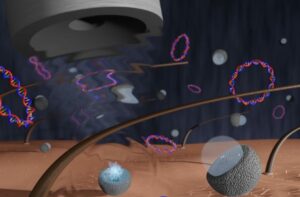
Képzeljünk el egy sereg önjáró, radioizotóppal borított részecskét, amelyek 2500-10,000 XNUMX-szer kisebbek egy porszemnél, amelyek a szervezetbe injektálva rákos daganatokat keresnek, és hozzátapadnak, elpusztítva azokat. Úgy hangzik, mint a sci-fi? Nem így van a hólyagrákos egereknél.
Spanyol kutatók arról számoltak be, hogy a radioaktív jódot tartalmazó nanorészecskék, amelyek karbamiddal reagálva meghajtásra kerülnek, képesek megkülönböztetni a rákos hólyagdaganatokat az egészséges szövetektől. Ezek a „nanobotok” behatolnak a daganat extracelluláris mátrixába, és felhalmozódnak benne, lehetővé téve, hogy a radionuklidterápia elérje a pontos célját. Egy tanulmányban, amelyet a Katalónia Biomérnöki Intézet (IBEC) Barcelonában az egyszeri adagot kapott egereknél a hólyagdaganatok mérete 90%-kal csökkent a kezeletlen állatokhoz képest.
Ez az újszerű megközelítés egy napon forradalmasíthatja a hólyagrák kezelését. Az Egészségügyi Világszervezet Global Cancer Observatory adatai szerint a hólyagrák a tizedik leggyakoribb rák a világon, 600,000-ben több mint 2022 220,000 új esetet diagnosztizáltak, és világszerte több mint XNUMX XNUMX halálesetet.
Az esetek 75%-át kitevő, nem izom-invazív hólyagrák kezelése jelenleg tumorreszekcióval, majd kemoterápiás vagy immunterápiás gyógyszerek intravezikális injekciójával történik a hólyagba. A gyógyszerbejuttatás azonban különösen nagy kihívást jelent az urothelium (a húgyutak belsejét bélelő szövet) alacsony permeabilitása, a vizelet tartalom feltöltése és a gyógyszerek ezt követő kimosása miatt. A folyamat a betegek számára is kényelmetlen, mivel hanyatt fekve időnként meg kell fordítaniuk a testüket, hogy a gyógyszerek a hólyag falának minden oldalára eljussanak. A kezelést követően öt éven belül 30-70%-os a kiújulás kockázata.
A klinikai eredmények javítása érdekében vezető kutató Samuel Sanchez és munkatársai célja, hogy innovatív és hatékonyabb húgyhólyagrák-kezeléseket fejlesszenek ki, és ennek során csökkentsék a kiújulási arányt. Ezen túlmenően, egy egyszeri dózisú terápia jelentősen csökkentené a kezelés költségeit, amely jelenleg hat és tizennégy kórházi kezelést tesz szükségessé.
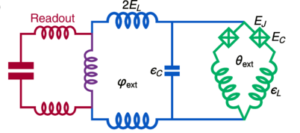
A csapat mezopórusos szilícium-dioxid nanorészecskékből készített nanobotokat, amelyek felületén különböző funkcionális komponensek találhatók. Ezek közé tartoznak a PET vizualizálására vagy radionuklid terápiára szolgáló radioizotópok, valamint a protein-ureáz, amely reakcióba lép a vizeletben lévő karbamiddal, és lehetővé teszi a nanobot meghajtását.
Írás Természet Nanotechnológia, a kutatók arról számoltak be, hogy amikor egy csepp nanobotot adtak egy 300 mM karbamidot tartalmazó oldathoz, a nanobotok rajzásos mozgást mutattak, aktív és erőteljes frontokat és háromdimenziós örvényeket alkotva. Karbamid nélkül a nanobotok egyszerűen ülepedtek a hozzáadási hely közelében.
Megvizsgálni, hogy a nanobotok el tudnak-e érni egy daganatot in vivo, a csapat felmérte viselkedésüket daganatos egereken. A pozitronemissziós tomográfia (PET) felvételei azt mutatták, hogy a radioaktívan jelölt nanobotoktól származó jelek az MRI-vel meghatározott tumorpozícióval egyidőben helyezkedtek el, és a radioaktivitás elsősorban a daganat célhelyén volt látható. Csak a nanobotokkal és karbamiddal injektált egerek mutattak jelentős felhalmozódást a tumortömegben – a vízben szállított nanobotok és a vízben vagy karbamidban szállított (ureáz nélküli) kontroll nanorészecskék minimális tumorfelvételt mutattak.
A kutatók azt sugallják, hogy a nanobotok mobilitása segít behatolni a tumor tömegébe. „A nanobotoknak hiányoznak a specifikus antitestek a daganat felismeréséhez, és a daganatszövet általában merevebb, mint az egészséges szövet, de ez nem így van a hólyagdaganatoknál” – magyarázza a szerző társszerzője. Meritxell Serra Casablancas az IBEC-től. „Megfigyeltük, hogy ezek a nanorobotok képesek lebontani a daganat extracelluláris mátrixát azáltal, hogy önjáró kémiai reakción keresztül helyileg növelik a pH-t. Ez a jelenség elősegítette a tumor nagyobb behatolását.” A kutatók úgy vélik, hogy a nanobotok úgy ütköznek az urotheliummal, mintha az fal lenne, de áthatolnak a szivacsosabb daganaton.
A csapat megjegyzi, hogy a nanobotok azonosítása a feldarabolt szövetek mikroszkópos felvételein kihívást jelentett. Miután a konfokális optikai mikroszkópos technikák kudarcot vallottak, a kutatók a IRB Barcelona kifejlesztett egy fénylap alapú, sík lézeres megvilágításon alapuló mikroszkópos rendszert, amely képes a hólyag különböző rétegeinek letapogatására és a teljes szerv 3D-s rekonstrukciójára.
„Az általunk kifejlesztett szórt elasztikus fénylap-mikroszkópos rendszer lehetővé tette, hogy kiküszöböljük a daganat által visszavert fényt, lehetővé téve számunkra, hogy előzetes jelölés nélkül, soha nem látott felbontásban azonosítsuk és lokalizáljuk a nanorészecskéket a szervben” Julien Colombelli az IRB Barcelonától.

A mesterséges baktériumok rákkeltő radioizotópokat vonzanak a daganatokba
A technika terápiás hatásának értékelése érdekében a csapat jód-131-gyel jelölte meg a nanobotokat.131Én, a radionuklid terápiában általánosan használt radioizotóp), és beadtam őket a daganatos egereknek. Kezelés vesztes dózissal 131A karbamidban lévő I-nanobotok megállították a tumor növekedését, miközben nagy dózisban 131A karbamidban beadott I-nanobotok közel 90%-kal csökkentették a daganat térfogatát a nem kezelt állatokhoz képest.
Sánchez elmondja Fizika Világa hogy a csapat következő lépései a kemoterápiában jelenleg használt kisméretű gyógyszerek kapszulázása és a nanobotok gyógyszerhordozóként való hatékonyságának további tesztelése. Végül az IBEC spinoffján keresztül szándékoznak bővíteni a nanobotokat, és megvizsgálják a szabályozási utakat, hogy a következő három-négy évben az első klinikai vizsgálatok felé haladjanak. Nanobots Therapeutics.
- SEO által támogatott tartalom és PR terjesztés. Erősödjön még ma.
- PlatoData.Network Vertical Generative Ai. Erősítse meg magát. Hozzáférés itt.
- PlatoAiStream. Web3 Intelligence. Felerősített tudás. Hozzáférés itt.
- PlatoESG. Carbon, CleanTech, Energia, Környezet, Nap, Hulladékgazdálkodás. Hozzáférés itt.
- PlatoHealth. Biotechnológiai és klinikai vizsgálatok intelligencia. Hozzáférés itt.
- Forrás: https://physicsworld.com/a/self-propelling-nanobots-shrink-bladder-tumours-in-mice-by-90/
- :is
- :nem
- $ UP
- 000
- 10
- 135
- 14
- 2022
- 220
- 300
- 3d
- 600
- a
- képesség
- Szerint
- Fiókok
- felhalmozásra
- felhalmozódás
- aktív
- hozzáadott
- mellett
- Ezen kívül
- beadott
- Után
- cél
- Minden termék
- lehetővé téve
- Is
- an
- és a
- állatok
- megközelítés
- VANNAK
- Hadsereg
- letartóztatott
- AS
- értékelni
- At
- csatolja
- vonz
- szerző
- Baktériumok
- barcelona
- alapján
- viselkedés
- Hisz
- között
- testületek
- test
- szünet
- de
- by
- TUD
- Rák
- képes
- hordozók
- eset
- esetek
- kihívást
- kémiai
- Klinikai
- klinikai vizsgálatok
- munkatársai
- Összeütközik
- COM
- Közös
- általában
- képest
- alkatrészek
- lefolytatott
- tartalom
- folytatódik
- ellenőrzés
- Költség
- készítette
- létrehozása
- Jelenleg
- nap
- halálesetek
- szállított
- kézbesítés
- eltökélt
- Fejleszt
- fejlett
- különböző
- különbséget tesz
- adag
- le-
- gyógyszer
- Kábítószer
- két
- Dust
- hatás
- Hatékony
- hatékonyság
- megszüntetése
- kibocsátás
- lehetővé
- engedélyezve
- lehetővé teszi
- lehetővé téve
- Egész
- EU
- értékelni
- végül is
- megvizsgálni
- kiállítva
- Elmagyarázza
- Sikertelen
- Fiction
- töltő
- vezetéknév
- öt
- követ
- következő
- A
- négy
- ból ből
- funkcionális
- Globális
- globálisan
- nagyobb
- Növekedés
- kellett
- Legyen
- Egészség
- egészséges
- segít
- azonban
- HTTPS
- azonosítani
- azonosító
- if
- képek
- immunterápia
- javul
- in
- tartalmaz
- növekvő
- információ
- újító
- belső
- szándékozik
- bele
- kérdés
- IT
- ITS
- maga
- jpg
- címkézés
- hiány
- lézer
- tojók
- Led
- fény
- mint
- bélés
- helyileg
- Elő/Utó
- Tömeg
- Mátrix
- max-width
- Lehet..
- Mikroszkópia
- minimális
- mobilitás
- több
- a legtöbb
- mozgás
- mozog
- MRI
- Természet
- Közel
- közel
- Szükség
- Új
- következő
- megjegyezni
- regény
- csillagvizsgáló
- of
- on
- ONE
- csak
- or
- eredmények
- felett
- különösen
- utak
- betegek
- behatolás
- jelenség
- Fizika
- Fizika Világa
- Plató
- Platón adatintelligencia
- PlatoData
- plusz
- pozíció
- pontos
- elsősorban
- Fő
- Előzetes
- folyamat
- Hajt
- meghajtás
- Fehérje
- Az árak
- el
- reakció
- reagál
- fogadó
- elismerik
- ismétlődés
- csökkenteni
- csökkentés
- tükrözi
- szabályozók
- jelentést
- megköveteli,
- kutatók
- Felbontás
- forradalmasítani
- Kockázat
- azt mondja,
- Skála
- letapogatás
- elszórt
- Tudomány
- Tudományos fantasztikum
- Keresés
- látott
- kimutatta,
- Sides
- jelek
- jelentősen
- egyszerűen
- egyetlen
- weboldal
- SIX
- Méret
- kicsi
- kisebb
- So
- megoldások
- hangok
- Spanyolország
- különleges
- Lépései
- Tanulmány
- későbbi
- lényeges
- javasol
- rendszer
- cél
- csapat
- technikák
- megmondja
- teszt
- mint
- hogy
- A
- a világ
- azok
- Őket
- maguk
- terápia
- Ezek
- ők
- ezt
- három
- háromdimenziós
- Keresztül
- egész
- miniatűr
- alkalommal
- nak nek
- felé
- kezelt
- kezelés
- kezelések
- vizsgálatok
- igaz
- FORDULAT
- jellemzően
- példátlan
- upon
- felvétel
- us
- használt
- különféle
- keresztül
- megjelenítés
- kötet
- Fal
- volt
- Víz
- we
- voltak
- amikor
- vajon
- ami
- míg
- val vel
- belül
- nélkül
- világ
- lenne
- év
- zephyrnet