A kórházak elleni számítógépes támadások pusztító hatást gyakorolhatnak, különösen a radiológiai és sugárterápiás osztályokra, amelyek működése különösen nagy a technológiától. Jó példa erre az írországi közegészségügyi szolgálatok elleni országos kibertámadás 2021 májusában, amely egyes rákos betegek tervezett sugárterápiás kezelését akár 12 napra is megszakította.
Ezt az esetet követően az orvosfizikusok a Galwayi Egyetemi Kórház és a Ír Nemzeti Egyetem, Galway elkezdett kifejleszteni egy házon belüli eszközt, amely segítséget nyújt a megszakítások után felülvizsgált sugárterápiás kezelési tervek elkészítéséhez. Az EQD nevű eszköz2VH – kiszámítja a kezelési kompenzációs terveket, és lehetővé teszi az összes tervopció vizuális összehasonlítását, valamint a páciens tervében szereplő egyes struktúrák egyedi elemzését. A kutatók az új szoftvereszközt a Journal of Applied Clinical Medical Physics.
A sugárterápiát leggyakrabban több héten át, kis sugárdózisok sorozatában (hagyományosan 2 Gy) hajtják végre, amelyeket frakcióknak neveznek. A nem tervezett kezelési hiányosságok – akár kibertámadások, gépek meghibásodása vagy betegbetegség miatt – jelentős visszaesést okozhatnak. Az ilyen hézagok alatt a rákos sejtek gyorsan újratelepednek a tumorszövetben, ami a radiobiológiai dózis csökkenését eredményezi a tervezési céltérfogathoz (PTV).

A probléma megoldására az EQD2A VH az eredeti betegtervekből kinyert dózis-térfogat hisztogram (DVH) információkat használ a kezelési rés kiszámításához. Katie O'Shea vezető szerző, az Ír Nemzeti Egyetem Galway munkatársa és munkatársai elmagyarázzák, hogy a szoftver az egyes adagtárolókban lévő fizikai dózist (a DVH adatpontjai közötti dózistartományt) biológiailag hatékony dózissá (BED) alakítja át. Ez magyarázza mind a PTV-ben bekövetkező repopulációs hatásokat, mind a veszélyeztetett szervekben (OAR) a javíthatatlan normál szövetek szubletális károsodásának hatásait.
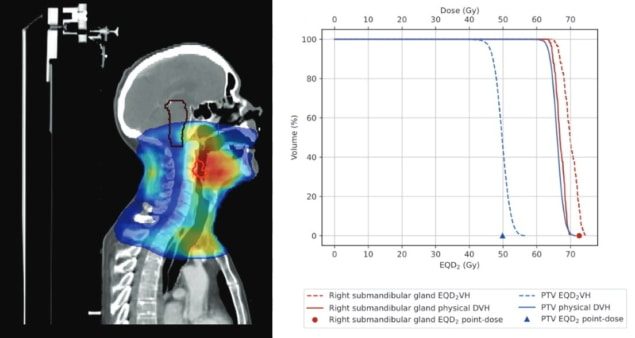
Miután módosította a BED-konverziót, hogy figyelembe vegye az egyes struktúrákban előforduló dózisváltozásokat, egy változó dózisú módszerrel, az eszköz átalakítja az egyes szerkezetek BED-jét 2 Gy-es frakciókban (EQD) kifejezett egyenértékdózissá.2). Ez normalizálja az egyes kezeléseket a hagyományos frakcionálásra, és lehetővé teszi a különböző frakcionálási sémákkal rendelkező tervek összegzését. Az eredményül kapott EQD2 A DVH 2D-ben mutatja be a kezelési hiánykompenzációs stratégiák hatását mind a PTV, mind az OAR dóziseloszlására, összehasonlítva az előírt kezelési tervvel.
Az EQD értékeléséhez2A VH klinikai döntéshozatali eszközeként a kutatók öt kiemelt fontosságú, gyorsan növekvő daganatos beteget választottak ki, akiknél a kezelési hézag nem haladhatja meg a két napot. Ebben négy fej-nyakrákos beteg intenzitásmodulált sugárkezelésen esett át, és egy tüdőrákos beteg 3D konformális sugárkezelésen esett át, akiknél 12 vagy 13 napos kezelési kihagyás volt. Ezek az esetek lehetővé tették a csapat számára az EQD használatának értékelését2VH hagyományos (2 Gy) és nem konvencionális (2.2 Gy) frakcionált és eltérő kezelési szünetekkel (46 és XNUMX nap között a terápiában) szenvedő betegek számára.
Az egyes betegek felülvizsgált kezelési tervei az eredeti terveken alapultak, vagy a frakciónkénti dózis vagy a frakciók száma megváltozott. O'Shea elmagyarázza, hogy minden egyes páciens felülvizsgált terve és ütemezése a napi kétszeri frakcionálást, a hétvégi kezeléseket és a megnövelt dózist alkalmazta a céltérfogatig, hogy csökkentsék a sejtrepopuláció hatását.
A tervek heti hat frakcióra korlátozták a kezelést, és kizárták a napi kétszeri frakcionálást az egymást követő napokon. Ha az előírt kezelést nem tudták a szükséges időkereten belül befejezni, a kutatók hipofrakcionációval (frakciónként megnövelt dózis beadása) vizsgálták a terveket. Képesek voltak vizuálisan és mennyiségileg összehasonlítani a különféle felülvizsgált terveket a páciens eredeti tervével, hogy meghatározzák, melyik adná a legjobb dózist a PTV-hez, és a legkisebb dózist az OAR-ekhez.
A kutatók megjegyzik, hogy az egyes struktúrák 2D-s ábrázolása az EQD-ben2A VH alaposabb elemzést nyújt, mint a Royal College of Radiologists (RCR) által javasolt 1D pontdózis-számítási módszer, amelyet jelenleg a sugárterápiás hiányosságok kezelésére használnak. A térfogaton belüli dóziseloszlás egydimenziós ábrázolása nem veszi figyelembe a tipikusan nem egyenletes dóziseloszlású OAR-okat, és túlbecsülheti az OAR-dózist. Ezen kívül az EQD2A VH eszköz bármilyen hosszúságú kezelési szünetre képes terveket készíteni, míg az RCR irányelvei a szokásos négy-öt napos szüneten alapulnak.
Az új eszköz további előnyei közé tartozik, hogy a páciens tervében minden egyes OAR-t nyomon lehet követni, így minimalizálva a további akut toxicitást okozó dózisemeléseket. A felhasználók azt is kiszámíthatják, hogy a különböző kezelési szünetek milyen hatással vannak a páciens kezelésére. Ez a képesség segíthet annak meghatározásában, hogy át kell-e vinni a pácienst egy másik klinikára, ha a tervezett klinikán túl hosszú a szakadék, vagy a beteg nyugodtan megvárhatja-e a kezelés folytatását.

Hogyan befolyásolta a COVID-19 a sugárterápia ellátását?
EQD2A VH figyelembe veheti a teljes kezelési idő változásait és a normál szövetek szubletális károsodását is, amit egy kereskedelmi rendszer nem biztos, hogy képes megtenni. A legfontosabb, hogy az eszköznek nem kell csatlakoznia a kórházi hálózathoz a működéséhez – akkor is használható, ha a kórház szervereit még mindig megbénítja egy kibertámadás.
„Még mindig értékeljük az EQD-t2A VH mint döntéshozatali eszköz” – mondja Margaret Moore, a kutatásvezető a Galway Egyetemi Kórházból. „Része egy jelenlegi projektnek, amely olyan palliatív kezelésben részesülő betegeket vizsgál, akiknél a frakciónkénti dózis nem szabványos, és ahol megfontolandó frakcionálási sémák közül lehet választani. A kezelési dózis átalakítása számos különböző frakcionált kezelésről EQD-re2 Lehetővé teszi a célszövetek és OAR-ok radiobiológiai dózisának összegyűjtését az átfogó dózis áttekintése érdekében, ami segíthet a további kezelés kiválasztásában.