Pengendalian jarak jauh terhadap reaksi kimia dalam lingkungan biologis dapat memungkinkan beragam aplikasi medis. Kemampuan untuk melepaskan obat kemoterapi sesuai target di dalam tubuh, misalnya, dapat membantu menghindari efek samping merusak yang terkait dengan senyawa beracun ini. Dengan tujuan ini, para peneliti di California Institute of Technology (Caltech) telah menciptakan sistem penghantaran obat yang benar-benar baru yang menggunakan ultrasound untuk melepaskan senyawa diagnostik atau terapeutik secara tepat kapan dan di mana pun dibutuhkan.
Platform ini, dikembangkan di laboratorium Maxwell Robb dan Mikhail Shapiro, didasarkan pada molekul peka gaya yang dikenal sebagai mekanofor yang mengalami perubahan kimia saat terkena gaya fisik dan melepaskan molekul muatan yang lebih kecil. Stimulus mekanis dapat diberikan melalui ultrasonografi terfokus (FUS), yang menembus jauh ke dalam jaringan biologis dan dapat diterapkan dengan presisi submilimeter. Namun, penelitian sebelumnya mengenai metode ini memerlukan intensitas akustik tinggi yang menyebabkan pemanasan dan dapat merusak jaringan di sekitarnya.
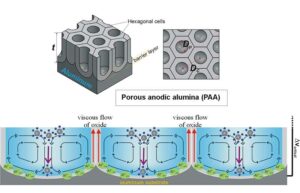
Untuk memungkinkan penggunaan intensitas USG yang lebih rendah – dan lebih aman, para peneliti beralih ke vesikel gas (GV), struktur nano protein berisi udara yang dapat digunakan sebagai agen kontras USG. Mereka berhipotesis bahwa GV dapat berfungsi sebagai transduser akustik-mekanis untuk memfokuskan energi ultrasonik: ketika terkena FUS, GV mengalami kavitasi dengan energi yang dihasilkan mengaktifkan mekanofor.
“Penerapan kekuatan melalui USG biasanya bergantung pada kondisi yang sangat intens yang memicu ledakan gelembung gas kecil yang terlarut,” jelas rekan penulis pertama. Molly McFadden dalam pernyataan pers. “Keruntuhannya adalah sumber kekuatan mekanis yang mengaktifkan mechanophore. Vesikel telah meningkatkan sensitivitas terhadap USG. Dengan menggunakannya, kami menemukan aktivasi mechanophore yang sama dapat dicapai dengan USG yang jauh lebih lemah.”
Melaporkan temuan mereka di Prosiding National Academy of Sciences, para peneliti menunjukkan bahwa pendekatan ini dapat memicu pelepasan molekul muatan dari polimer yang difungsikan mechanophore dari jarak jauh menggunakan FUS biokompatibel.
Perkembangan pengiriman obat
McFadden dan rekannya pertama kali mengidentifikasi parameter USG yang aman untuk aplikasi fisiologis. Eksperimen dengan FUS 330 kHz menunjukkan batas atas biokompatibel sebesar 1.47 MPa tekanan negatif puncak dengan siklus kerja 4.5% (3000 siklus per pulsa), menghasilkan intensitas akustik 3.6 W/cm2. Dalam hantu gel yang meniru jaringan, parameter ini menyebabkan peningkatan suhu maksimum hanya 3.6 °C.
Para peneliti kemudian menyelidiki apakah FUS dapat mengaktifkan polimer yang mengandung mechanophore menggunakan parameter biokompatibel ini. Mereka mempelajari polimer PMSEA yang mengandung mekanofor berpusat rantai yang diisi dengan molekul kecil fluorogenik. Mengekspos larutan encer polimer ini ke FUS biokompatibel dengan adanya GV menghasilkan peningkatan fluoresensi yang kuat, yang menunjukkan keberhasilan pelepasan muatan – sekitar 15% pelepasan setelah 10 menit paparan FUS. Yang penting, paparan FUS tanpa GV tidak memicu respons fluorogenik, menegaskan bahwa GV memainkan peran penting sebagai transduser akustik-mekanis.
Selanjutnya, para peneliti memeriksa apakah sistem tersebut cocok untuk pelepasan obat yang dipicu secara mekanis. Mereka mengkonjugasikan agen kemoterapi camptothecin ke mechanophore diikuti dengan polimerisasi untuk membuat PMSEA-CPT, dan menggunakan FUS untuk menghasilkan pelepasan terkontrol. Setelah 10 menit terpapar FUS plus GV biokompatibel, sekitar 8% camptothecin dilepaskan. Seperti yang ditemukan pada molekul fluorogenik, tidak ada pelepasan obat yang terdeteksi tanpa adanya GV.
Menurut rekan penulis pertama Yuxing Yao, ini adalah pertama kalinya FUS terbukti mengendalikan reaksi kimia tertentu dalam lingkungan biologis. “Sebelumnya USG telah digunakan untuk mengganggu atau memindahkan sesuatu,” kata Yao. “Tapi sekarang ini membuka jalan baru bagi kita dalam menggunakan mekanokimia.”
Untuk menilai potensi platform di masa depan untuk kemoterapi yang ditargetkan pada pasien, para peneliti menyelidiki sitotoksisitasnya in vitro pada sel Raji yang mirip limfoblas. Sel yang diinkubasi selama dua hari dengan PMSEA-CPT yang sebelumnya terpapar FUS dan GV menunjukkan penurunan viabilitas yang signifikan. Sebaliknya, tidak ada sitotoksisitas signifikan yang terlihat pada sel yang diinkubasi dengan PMSEA-CPT yang belum terpapar FUS atau PMSEA-CPT yang terpapar FUS tetapi tanpa GV.

Perangkat implan yang dipicu cahaya memberikan penghantaran obat yang dapat diprogram
“Pelepasan muatan molekuler yang dipicu secara mekanis dari polimer dalam media berair menggambarkan kekuatan pendekatan ini untuk bioimaging non-invasif dan aplikasi terapeutik dari mekanokimia polimer,” tulis para peneliti. “Secara lebih luas, penelitian ini menunjukkan pendekatan untuk mencapai kendali jarak jauh terhadap reaksi kimia tertentu dalam kondisi yang relevan secara biomedis dengan presisi spatiotemporal dan penetrasi jaringan yang dihasilkan oleh FUS.”
Setelah pengujian awal di bawah kondisi laboratorium terkendali, para peneliti kini berencana menguji platform mereka pada organisme hidup. “Kami berupaya menerjemahkan penemuan mendasar ini menjadi in vivo aplikasi untuk pengiriman obat dan teknologi biomedis lainnya,” kata Robb Dunia Fisika.
- Konten Bertenaga SEO & Distribusi PR. Dapatkan Amplifikasi Hari Ini.
- PlatoData.Jaringan Vertikal Generatif Ai. Berdayakan Diri Anda. Akses Di Sini.
- PlatoAiStream. Intelijen Web3. Pengetahuan Diperkuat. Akses Di Sini.
- PlatoESG. Karbon, teknologi bersih, energi, Lingkungan Hidup, Tenaga surya, Penanganan limbah. Akses Di Sini.
- PlatoHealth. Kecerdasan Uji Coba Biotek dan Klinis. Akses Di Sini.
- Sumber: https://physicsworld.com/a/biocompatible-focused-ultrasound-delivers-cancer-drugs-on-target/
- :memiliki
- :adalah
- :bukan
- :Di mana
- 1
- 10
- 15%
- 3000
- a
- kemampuan
- Akademi
- dicapai
- mencapai
- mengaktifkan
- Activation
- diberikan
- Setelah
- Agen
- agen
- tujuan
- an
- dan
- aplikasi
- terapan
- pendekatan
- sekitar
- ADALAH
- sekitar
- AS
- menilai
- terkait
- At
- penulis
- berdasarkan
- BE
- menjadi
- biomedis
- tubuh
- Terikat
- secara luas
- tapi
- by
- california
- CAN
- Kanker
- Menyebabkan
- Sel
- Perubahan
- kimia
- Lihat Lebih Sedikit
- rekan
- Kondisi
- mengandung
- kontras
- kontrol
- dikendalikan
- bisa
- membuat
- dibuat
- siklus
- siklus
- merusak
- Hari
- mengurangi
- mendalam
- memberikan
- pengiriman
- mendemonstrasikan
- menunjukkan
- menunjukkan
- terdeteksi
- dikembangkan
- alat
- diagnostik
- MELAKUKAN
- penemuan
- Mengganggu
- beberapa
- obat
- Obat-obatan
- Terdahulu
- efek
- aktif
- energi
- sepenuhnya
- lingkungan
- penting
- contoh
- eksperimen
- Menjelaskan
- terkena
- Pencahayaan
- Temuan
- Pertama
- pertama kali
- Fokus
- terfokus
- diikuti
- Untuk
- kekuatan
- ditemukan
- dari
- fungsi
- mendasar
- masa depan
- GAS
- memiliki
- Memiliki
- meningkat
- membantu
- High
- Namun
- HTTPS
- diidentifikasi
- menggambarkan
- gambar
- ledakan
- penting
- in
- Meningkatkan
- diinkubasi
- informasi
- mulanya
- Lembaga
- ke
- isu
- NYA
- jpg
- dikenal
- laboratorium
- Labs
- Dipimpin
- meninggalkan
- MEMBATASI
- hidup
- menurunkan
- max-width
- maksimum
- mekanis
- Media
- medis
- Aplikasi Medis
- metode
- menit
- molekuler
- molekul
- pindah
- banyak
- nasional
- dibutuhkan
- negatif
- New
- tidak
- sekarang
- of
- on
- hanya
- pembukaan
- or
- Lainnya
- parameter
- path
- pasien
- Puncak
- penetrasi
- untuk
- hantu
- fisik
- Fisika
- Dunia Fisika
- rencana
- Platform
- Platform
- plato
- Kecerdasan Data Plato
- Data Plato
- Bermain
- plus
- polimer
- potensi
- kekuasaan
- tepat
- Ketelitian
- kehadiran
- pers
- tekanan
- sebelumnya
- diprogram
- Protein
- memberikan
- disediakan
- menyediakan
- nadi
- jarak
- reaksi
- Reaksi
- melepaskan
- dirilis
- relevan
- terpencil
- wajib
- peneliti
- tanggapan
- dihasilkan
- Terungkap
- benar
- Peran
- aman
- lebih aman
- sama
- mengatakan
- terlihat
- Kepekaan
- pengaturan
- sisi
- penting
- kecil
- lebih kecil
- larutan
- sumber
- tertentu
- Pernyataan
- rangsangan
- kuat
- belajar
- studi
- Belajar
- sukses
- cocok
- sistem
- target
- ditargetkan
- Teknologi
- Teknologi
- mengatakan
- uji
- tes
- bahwa
- Grafik
- Sumber
- mereka
- Mereka
- kemudian
- Ini
- mereka
- hal
- ini
- Melalui
- kuku ibu jari
- waktu
- untuk
- menterjemahkan
- memicu
- dipicu
- benar
- Berbalik
- dua
- bawah
- menjalani
- us
- menggunakan
- bekas
- kegunaan
- menggunakan
- biasanya
- sangat
- melalui
- kelangsungan hidup
- adalah
- we
- ketika
- apakah
- yang
- dengan
- dalam
- tanpa
- kerja
- dunia
- menulis
- zephyrnet.dll