HONG KONG, 17 febbraio 2022 – (ACN Newswire) – SinoMab BioScience Limited ("SinoMab" o la "Società", insieme alle sue controllate, il "Gruppo", codice azionario: 3681.HK), un'azienda biofarmaceutica con sede a Hong Kong società dedicata alla ricerca, sviluppo, produzione e commercializzazione di prodotti terapeutici per il trattamento di malattie immunologiche, è lieta di annunciare che, l'11 febbraio 2022 (ora locale EST), è stata presentata una richiesta di sperimentazione di un nuovo farmaco ("IND"), per il Il prodotto terapeutico per l'asma SM17 (anticorpo monoclonale umanizzato anti-IL17RB iniettabile) di prima classe (FIC) è stato presentato e accettato dalla Food and Drug Administration ("FDA") statunitense. La Società prevede di avviare lo studio First-In-Human negli Stati Uniti nel primo trimestre del 2022, una volta che l’IND sarà approvato dalla FDA.
 |
SM17 è il primo anticorpo monoclonale al mondo contro IL17BR sviluppato in collaborazione da SinoMab e LifeArc (un ente di beneficenza per la ricerca medica con sede nel Regno Unito). SM17 ha un'ampia gamma di indicazioni, comprese indicazioni con grandi volumi di mercato come l'asma e malattie con tassi di mortalità elevati come la fibrosi polmonare idiopatica. Rispetto ad altri prodotti sul mercato, SM17 gode di vantaggi di differenziazione. Con i dati preclinici e il meccanismo d'azione unico dell'SM17, l'azienda ritiene che l'SM17 abbia potenzialmente un effetto più ampio e più benefico sul trattamento dell'asma rispetto ad altri biologici approvati.
Nel mercato globale, il numero di pazienti con asma è in graduale aumento e si prevede che raggiungerà i 247.5 milioni entro il 2023 e aumenterà ulteriormente a 267.7 milioni entro il 2030. Il numero di pazienti affetti da asma nella RPC sta aumentando a un ritmo maggiore rispetto al tasso globale e si prevede che raggiungerà i 25.6 milioni entro il 2023 e aumenterà ulteriormente a 27.8 milioni entro il 2030. In termini di dimensioni del mercato, si prevede che il mercato globale dell'asma raggiungerà i 25.1 miliardi di dollari entro il 2023 e i 34.6 miliardi di dollari entro il 2030. Tuttavia, il mercato dell'asma nel Si prevede che la RPC raggiungerà i 36.4 miliardi di RMB entro il 2023 e i 65.0 miliardi di RMB entro il 2030. In termini di opzioni terapeutiche, il trattamento tradizionale dell'asma si basa sui corticosteroidi per via inalatoria, ma sono soggetti a gravi effetti avversi, soprattutto negli adolescenti. La resistenza ai farmaci può anche svilupparsi se usata per lungo tempo. L'introduzione di SM17 dovrebbe fornire una migliore opzione di trattamento in termini di equilibrio tra efficacia e sicurezza.
Il Dr. Shui On LEUNG, Presidente, Direttore Esecutivo e Amministratore Delegato di SinoMab ha affermato che: "a seguito dell'accettazione della domanda IND per SN1011 per il trattamento della sclerosi multipla da parte dell'NMPA, l'accettazione della domanda IND SM17 da parte della FDA pienamente dimostra l'esecuzione efficiente del nuovo programma di ricerca e sviluppo di farmaci dell'azienda. C'è ancora un'esigenza medica insoddisfatta per ulteriori terapie efficaci, in particolare per i pazienti che non rispondono ai trattamenti attuali. Siamo quindi fiduciosi nelle enormi prospettive di sviluppo clinico di SM17. Il nostro core prodotti, tra cui SM03, SN1011 e SM17, stanno facendo progressi nella ricerca e sviluppo clinico senza intoppi, guidando l'azienda a muoversi costantemente verso la commercializzazione. In futuro, accelereremo l'implementazione dei nostri progetti per portare benefici ai pazienti e creare valore per gli azionisti attraverso l'innovazione".
Informazioni su SM17
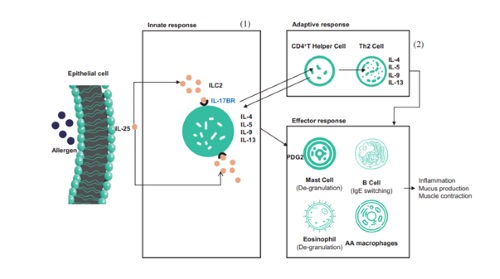
SM17 è noto per essere il primo anticorpo monoclonale IgG4-k umanizzato al mondo per lo sviluppo di nuovi farmaci, che prendono di mira IL-17RB. E IL-17RB è una glicoproteina transmembrana singola di tipo I appartenente alla famiglia dei recettori IL-17. Il legame di SM17 a IL-17RB potrebbe sopprimere le risposte immunitarie Th2 indotte da una categoria di citochine chiamata "alarmin", che ha dimostrato di essere implicata nella patogenesi della malattia allergica e nelle risposte virali delle vie aeree. Si prevede che un approccio alternativo mirato ai mediatori a monte della cascata infiammatoria Th2, come le "alarmine", abbia un effetto più ampio sull'infiammazione delle vie aeree e fornisca un controllo dell'asma più efficace rispetto alle terapie attualmente disponibili, e sono stati utilizzati prodotti con meccanismo d'azione simile a quello dell'SM17 approvato dalla FDA.
Informazioni su SinoMab BioScience Limited
SinoMab BioScience Limited (codice azionario: 3681.HK) è dedicato alla ricerca, sviluppo, produzione e commercializzazione di terapie per il trattamento delle malattie immunologiche. Il prodotto di punta dell'azienda SM03 è un potenziale mAb globale first-in-target contro CD22 per il trattamento dell'artrite reumatoide (RA) ed è attualmente in studio clinico di Fase III per l'artrite reumatoide in Cina, che è stato riconosciuto come uno dei più significativi progetti di sviluppo significativo di nuovi farmaci del dodicesimo piano quinquennale e del tredicesimo piano quinquennale. Inoltre, la Società possiede altri potenziali farmaci candidati first-in-target e first-in-class, alcuni dei quali sono già in fase clinica, con indicazioni che coprono l'artrite reumatoide (RA), il lupus eritematoso sistemico (LES), il pemfigo volgare (PV), linfoma non Hodgkin (NHL), asma e altre malattie con importanti esigenze cliniche non soddisfatte.
Copyright 2022 ACN Newswire. Tutti i diritti riservati. www.acnnewswire.com SinoMab BioScience Limited ("SinoMab" o la "Società", insieme alle sue controllate, il "Gruppo", codice azionario: 3681.HK), una società biofarmaceutica con sede a Hong Kong dedicata alla ricerca, sviluppo, produzione e commercializzazione di terapie per il trattamento di malattie immunologiche
- 11
- 2022
- 7
- accelerare
- Newswire ACN
- Action
- aggiuntivo
- vantaggi
- Tutti
- già
- Annunciare
- Applicazioni
- approccio
- disponibile
- crede
- vantaggi
- Miliardo
- presidente
- Beneficenza
- capo
- amministratore delegato
- Cina
- codice
- commercializzazione
- azienda
- fiducioso
- di controllo
- copyright
- potuto
- Corrente
- dati
- dedicato
- sviluppare
- Mercato
- Direttore
- Malattia
- malattie
- guida
- droga
- farmaci
- effetto
- Efficace
- enorme
- particolarmente
- esecutivo
- Direttore esecutivo
- previsto
- famiglia
- fda
- Nome
- i seguenti
- cibo
- futuro
- globali
- Alta
- HTTPS
- Compreso
- Aumento
- Innovazione
- conosciuto
- grandi
- Limitato
- locale
- Lunghi
- maggiore
- Fare
- consigliato per la
- Rappresentanza
- medicale
- milione
- Responsabile
- Opzione
- Opzioni
- Altro
- fase
- Prodotto
- Prodotti
- Programma
- progetti
- fornire
- Trimestre
- R&D
- gamma
- riparazioni
- Sicurezza
- Suddetto
- significativa
- simile
- Taglia
- Stage
- azione
- Studio
- presentata
- Attraverso
- tempo
- insieme
- tradizionale
- trattamento
- prova
- noi
- unico
- Unito
- UK
- APPREZZIAMO
- OMS