By Kenna Hughes-Castleberry pubblicato il 07 ottobre 2022
Molte equazioni all'interno della fisica quantistica possono essere utili per guidare i ricercatori che stanno esaminando le interazioni chimiche. Sia come fisica quantistica che chimica lavorano sugli stessi livelli atomici, sono spesso usati in tandem tra loro per ottenere nuovi risultati. Recentemente, i ricercatori del Laboratorio nazionale di Los Alamos (LANL) ha portato questo abbinamento un ulteriore passo avanti aggiungendo machine learning processi per aiutare a prevedere l'interazione biochimica nelle simulazioni molecolari. Questo a sua volta potrebbe aiutare ad accelerare i passi nella progettazione di farmaci e in altri scenari del settore, rendendo i farmaci più sicuri e più veloci a lungo termine.
Utilizzo dell'apprendimento automatico per i set di dati
I processi di apprendimento automatico sono già in corso applicato all'informatica quantistica e alla fisica quantistica. Poiché l'apprendimento automatico prevede e crea modelli da grandi gruppi di dati, è vantaggioso per campi come la fisica quantistica o la chimica, che hanno molti pezzi in movimento. Secondo il ricercatore LANL Benjamin Nebgen: “prima dell'avvento dei metodi di apprendimento automatico (ML) nei campi della chimica e della scienza dei materiali, la più grande simulazione pratica della chimica e dei sistemi materiali era limitata a poche migliaia di atomi. Questo è troppo piccolo per catturare con precisione molti effetti che determinano proprietà chimiche o materiali come i percorsi dei grani o i rari percorsi reattivi”. Grazie ai vantaggi dell'apprendimento automatico, i ricercatori possono studiare scenari più complicati nelle simulazioni, comprese quelle incentrate sulla fisica quantistica e sulla chimica.
Per gli scienziati che progettano nuovi farmaci o studiando le reazioni chimiche, è importante comprendere appieno cosa sta accadendo con gli elettroni a livello quantico. "Il moto degli elettroni e dei nuclei atomici controlla quasi tutte le proprietà chimiche e materiali che definiscono la nostra esistenza moderna", ha detto Nebgen. “Ciò include la chimica di tutto, dalle droghe che assumiamo, ai detergenti per la casa che usiamo quotidianamente, ai carburanti delle nostre auto e camion. Inoltre, le proprietà dei materiali che compongono le nostre auto, case, strumenti, aerei e quasi tutto ciò con cui interagiamo quotidianamente sono controllate dalla stessa fisica sottostante”. Ciò consente ai ricercatori di sondare più a fondo le interazioni di una molecola a un livello fondamentale. Tuttavia, una volta raggiunto questo livello, ne consegue una matematica più complicata. "Le forze che agiscono sui singoli atomi che entrano nelle equazioni di Newton derivano dal moto degli elettroni, che sono intrinsecamente di natura quantistica", ha spiegato Nebgen. "Pertanto, gli elettroni devono essere trattati con l'equazione di Schrödinger, che è un problema matematico molto più impegnativo da risolvere".
LANL utilizza l'apprendimento automatico per creare modelli
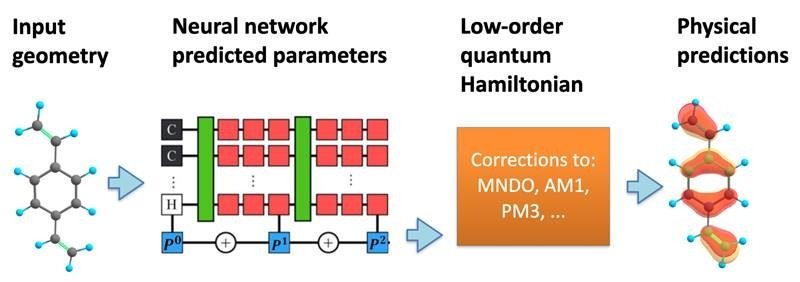
Per superare queste difficili equazioni, ricercatori come Nebgen stanno utilizzando strumenti di apprendimento automatico. Questi strumenti possono accelerare una simulazione chimica concentrandosi solo su alcuni degli elettroni più importanti del sistema, ha aggiunto Nebgen. Utilizzando uno strumento di apprendimento automatico chiamato rete neurale, Nebgen e il suo team sono stati in grado di creare un modello predittivo dei possibili stati elettronici e delle loro energie associate all'interno di una molecola. Da lì il team ha potuto prevedere con precisione alcuni dei possibili risultati della simulazione dati diversi input. Per le aziende biotecnologiche che spendono milioni di dollari per progettare e testare nuovi farmaci, modelli predittivi come questo potrebbero offrire molti vantaggi economici. Sebbene l'utilizzo dell'apprendimento automatico nell'industria farmaceutica non sia una novità, combinarlo con la potenza dell'informatica quantistica potrebbe creare la prossima generazione di tecnologia necessaria per lanciare farmaci futuri.
Kenna Hughes-Castleberry è una scrittrice presso Inside Quantum Technology e Science Communicator presso JILA (una partnership tra l'Università del Colorado Boulder e il NIST). I suoi ritmi di scrittura includono la tecnologia profonda, il metaverso e la tecnologia quantistica.