La terapia con particelle - trattamento del cancro che utilizza fasci di protoni o ioni più pesanti - fornisce una somministrazione di dosi altamente conforme e un maggiore risparmio di tessuti normali rispetto alla radioterapia convenzionale basata su fotoni. Ma per i sopravvissuti al cancro a lungo termine, il rischio di cancro secondario indotto da radiazioni (SC) è importante e dovrebbe essere considerato quando si seleziona la modalità di trattamento.
Con i dati epidemiologici scarsi per trattamenti più recenti come la terapia con protoni e ioni di carbonio, un team diretto al Centro GSI Helmholtz per la ricerca sugli ioni pesanti sta sviluppando un modello per confrontare i rischi SC tra le modalità di terapia con particelle. Il modello, descritto da Antonia Hufnagl e colleghi dentro Fisica medica, potrebbe infine essere incorporato nei sistemi di pianificazione del trattamento per includere il rischio SC come criterio di ottimizzazione aggiuntivo.
Eventi letali contro eventi cancerogeni
I modelli di rischio SC in genere funzionano considerando l'equilibrio tra l'uccisione cellulare (che porta alla soppressione del cancro) e la trasformazione cellulare (induzione di mutazioni che alla fine portano al cancro). La probabilità che un volume irradiato sviluppi il cancro è definita utilizzando il modello lineare-quadratico (LQ), che fornisce una semplice relazione tra la sopravvivenza cellulare e la dose di fotoni erogata.
In questo studio, i ricercatori hanno utilizzato il modello di effetto locale (LEM) per prevedere l'efficacia biologica relativa (RBE) dell'induzione di SC dopo la terapia con particelle. Per tenere conto dell'aumento dell'RBE della radiazione particellare, hanno sostituito i parametri LQ del fotone nel modello di rischio con i parametri LQ del fascio di ioni previsti dal LEM. Una caratteristica fondamentale del loro approccio è l'uso del LEM sia in termini di uccisione cellulare che di induzione del cancro.

"Il doppio uso del LEM riflette la competizione tra i due principali processi che determinano lo sviluppo di SC, vale a dire la trasformazione cellulare e l'uccisione cellulare", spiega l'autore senior Michael Scholz. “Con l'aumento della dose e/o dell'efficacia, l'uccisione cellulare può sopprimere la vitalità delle cellule trasformate. Ciò porta a un'interazione complessa, che non può essere semplicemente riflessa altrimenti in una procedura in un'unica fase.
Per studiare quali fattori influenzano il rischio di SC, i ricercatori hanno utilizzato il sistema di pianificazione TPS TRiP98 per generare piani di trattamento di ioni carbonio e protoni biologicamente ottimizzati basati su una geometria idealizzata. I piani hanno irradiato un bersaglio di 4x4x4 cm con un singolo fascio di particelle o due fasci opposti, con un organo a rischio (OAR) di 4x4x1 cm davanti al bersaglio. A causa delle incertezze nei parametri LQ del fotone utilizzati come input per il LEM, hanno stimato i rapporti di rischio protone-ione carbonio, piuttosto che i valori di rischio individuali.
Per queste configurazioni idealizzate, il modello non ha mostrato una chiara preferenza per i protoni o gli ioni di carbonio, ma ha rivelato una complessa dipendenza da vari parametri. La ridotta dispersione laterale degli ioni di carbonio porta a un rischio SC inferiore rispetto ai protoni nel canale di ingresso. Tuttavia, gli ioni di carbonio depositano una dose più elevata dietro il bersaglio a causa della coda di frammentazione, aumentando il rischio SC per OAR dietro il tumore dopo l'irradiazione con ioni di carbonio.
Per i piani a raggio singolo, il rischio SC totale era circa 1.5 volte superiore per gli ioni di carbonio che per i protoni. Con due fasci opposti, il rischio SC totale era 1.16 volte superiore per i protoni, anche se questo variava fortemente a seconda della posizione spaziale del volume sensibile presunto rispetto al volume target.
La radiosensibilità dei tessuti (ai fotoni) ha avuto un impatto importante sul rapporto di rischio SC, con OAR radioresistenti che beneficiano del trattamento con ioni di carbonio e OAR sensibili dai fasci di protoni. Al contrario, lo schema di frazionamento ha avuto un impatto minimo sui valori di rischio attesi.
Geometria paziente
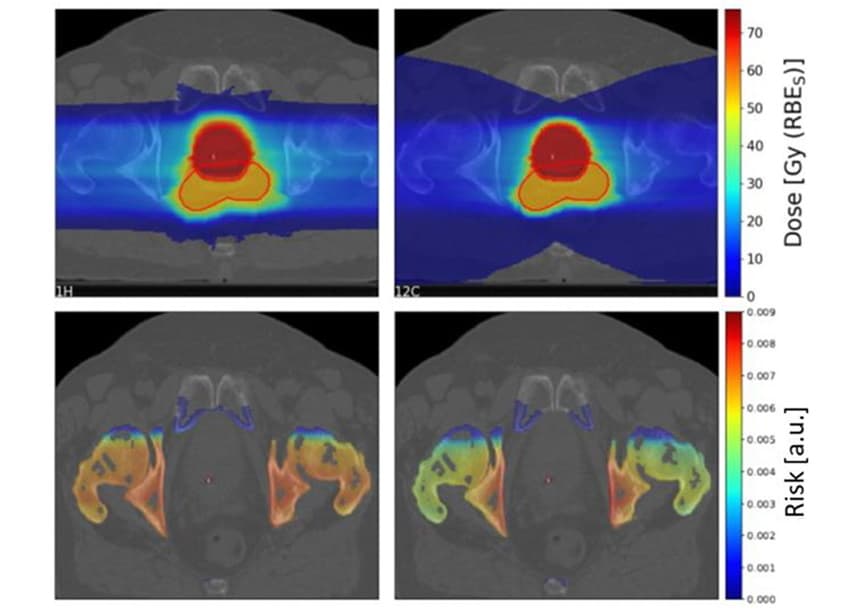
Per studiare gli scenari clinici, Scholz e colleghi hanno stimato i rischi di SC per 10 pazienti affetti da cancro alla prostata precedentemente trattati con radioterapia fotonica presso il Karolinska University Hospital. Hanno generato piani di trattamento per i pazienti utilizzando due campi di protoni e ioni di carbonio scansionati lateralmente opposti.
Come visto in precedenza, la coda di frammentazione degli ioni di carbonio ha prodotto un'ampia area a bassa dose dietro il bersaglio. Tuttavia, la regione bersaglio ad alta dose era più conforme per i piani di ioni carbonio rispetto ai piani di protoni.
Il team ha calcolato i rapporti di rischio SC protone-ione carbonio per quattro OAR (vescica, retto, ossa e pelle) per i 10 pazienti. Per le ossa e la pelle, i piani protonici hanno prodotto un rischio SC leggermente superiore rispetto ai piani a ioni di carbonio, con rapporti di rischio mediano di 1.19 e 1.06 rispettivamente per ossa e pelle. Per la vescica e il retto, tuttavia, i piani protonici hanno comportato rischi SC significativamente inferiori, con rapporti di rischio di 0.68 e 0.49 rispettivamente per vescica e retto.
I ricercatori concludono che le intuizioni ottenute da questo modello potrebbero aiutare a ottimizzare i trattamenti futuri. Attualmente, la modellazione del rischio relativo è principalmente adatta come strumento per confrontare diversi scenari di trattamento per diverse coorti di pazienti. Ma Scholz osserva che incorporare tali modelli nella pianificazione del trattamento per i singoli pazienti sarebbe semplice.

La terapia con griglia di ioni di carbonio risparmia i tessuti sani
"Richiede solo di eseguire la pianificazione per una data distribuzione della dose con due diversi set di parametri biologici che rappresentano rispettivamente l'uccisione cellulare e il processo di trasformazione cellulare", spiega. "Quindi, è necessaria solo una post-elaborazione delle risultanti distribuzioni di effetti 3D con strumenti matematici standard per derivare le corrispondenti distribuzioni del rapporto di rischio".
Il prossimo passo, dice, è convalidare il modello confrontandolo con i dati clinici. «Poiché al momento questi dati sono scarsi, l'estensione dell'approccio per includere anche i trattamenti con i fotoni e la determinazione dei corrispondenti rapporti di rischio di protoni contro fotoni e ioni carbonio contro fotoni sarebbe un importante passo successivo», dice Scholz. Mondo della fisica.