La capacità di unire l’elettronica e i sensori ottici con il corpo umano a livello di singola cellula potrebbe un giorno consentire il monitoraggio e il controllo remoto delle singole cellule in tempo reale. I progressi nella fabbricazione elettronica hanno reso possibile la creazione di transistor e sensori con risoluzione su scala nanometrica, mentre tecniche innovative di nanopatterning consentono l'assemblaggio di questi dispositivi su substrati flessibili. Tali processi, tuttavia, generalmente richiedono sostanze chimiche aggressive, temperature elevate o tecniche di vuoto che non sono adatte a cellule e tessuti viventi.
Per superare questi ostacoli, un gruppo di ricerca della Johns Hopkins University ha sviluppato un processo non tossico, ad alta risoluzione ed economico per stampare nanomodelli d’oro su tessuti e cellule viventi. Riportando i loro risultati in Nano Letters, dimostrano che la nuova tecnica può “tatuare” cellule e tessuti viventi con matrici flessibili di nanopunti e nanofili d’oro. In definitiva, il metodo potrebbe essere utilizzato per integrare dispositivi intelligenti con tessuti viventi per applicazioni quali la bionica e il biosensing.
"Se avessimo tecnologie per monitorare la salute delle cellule isolate, potremmo forse diagnosticare e curare le malattie molto prima e non aspettare che l'intero organo venga danneggiato", spiega il leader del team Davide Grazia in un comunicato stampa. “Stiamo parlando di mettere qualcosa come un tatuaggio elettronico su un oggetto vivente decine di volte più piccolo della capocchia di uno spillo. È il primo passo verso il collegamento di sensori ed elettronica su cellule vive”.
Grazie, Luo Gu e colleghi hanno progettato un processo di stampa a nanotrasferimento in tre fasi per legare nanomodelli d'oro alle cellule vive. Nella prima fase, hanno utilizzato la convenzionale litografia a nanoimpronta (NIL) per stampare matrici di nanopunti o nanofili d'oro su wafer di silicio rivestiti di polimero. Hanno poi sciolto il polimero, liberando i nanoarray per il trasferimento su vetrini coprioggetto.
Successivamente, i ricercatori hanno funzionalizzato la superficie dell'oro con cisteamina e hanno rivestito gli array NIL d'oro con uno strato di trasferimento di idrogel di alginato. Hanno dimostrato che questo approccio potrebbe trasferire in modo affidabile matrici di nanopunti e nanofili di 8 × 8 mm dal vetro agli idrogel morbidi e flessibili. Nella fase finale, gli array NIL d'oro vengono coniugati con gelatina per consentirne il trasferimento su cellule o tessuti viventi. La dissociazione dello strato di trasferimento dell'idrogel espone quindi il motivo dorato.
I ricercatori hanno studiato il comportamento delle cellule vive di fibroblasti seminate su matrici di punti d'oro di 250 nm di diametro (spaziatura da centro a centro di 550 nm) o fili d'oro di 300 nm di larghezza (spaziatura di 450 nm) su idrogel di alginato. Circa 24 ore dopo la semina, le cellule sull'idrogel stampato su nanofili migravano preferibilmente parallelamente ai nanofili, mentre quelle sui nanopunti mostravano una migrazione casuale, ma leggermente più veloce. Anche le cellule sui nanofili hanno mostrato un allungamento circa doppio di quelle sui nanopunti. Questi risultati dimostrano la capacità degli array NIL in oro di guidare l'orientamento e la migrazione delle cellule.
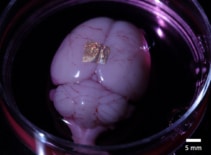
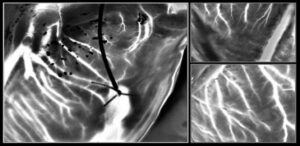
Oltre ad essere biocompatibile con cellule e tessuti, l'idrogel di alginato può anche trasferire array NIL d'oro su organi e cellule viventi. Per dimostrarlo, i ricercatori hanno posizionato idrogel stampati su nanofili sulla corteccia cerebrale di un intero cervello e su una fetta di cervello coronale.
Dopo 2 ore nei terreni di coltura e dopo la dissociazione dell'idrogel, i nanofili sono rimasti legati alla superficie dell'intero cervello. Al contrario, i nanofili sulla fetta di cervello non aderivano, suggerendo che la forza di adesione varia tra i diversi tipi di cellule e metodi di coltura. I ricercatori sottolineano che sono necessari ulteriori studi per caratterizzare e ottimizzare i meccanismi di adesione per un legame robusto a lungo termine.
Infine, per valutare la stampa a biotrasferimento a livello di singola cellula, i ricercatori hanno coltivato fogli cellulari monostrato su idrogel di alginato stampati con array NIL in oro. Dopo 24 ore, hanno capovolto gli idrogel seminati di fibroblasti su vetrini coprioggetto rivestiti di gelatina e hanno lasciato che le cellule si attaccassero ai vetrini coprioggetto durante la notte.
Dopo aver dissociato l'idrogel di alginato, la microscopia a fluorescenza ha rivelato che i fibroblasti modellati con nanopunti d'oro avevano una vitalità di circa il 97%, mentre quelli modellati con nanofili avevano una vitalità di circa il 98%, indicando che il processo di stampa è biocompatibile con le cellule vive. I colori riflettenti visti sul foglio cellulare di fibroblasti modellato suggeriscono che la forma della matrice NIL dorata è stata mantenuta.
Il processo di fabbricazione è compatibile anche con la fotolitografia su microscala, che ha consentito ai ricercatori di creare patch esagonali e triangolari di matrici NIL d'oro larghe 200 µm. Li hanno poi stampati tramite biotrasferimento su fogli cellulari, portando alla crescita selettiva delle cellule fibroblastiche sui micropatch. I filmati registrati per oltre 16 ore hanno mostrato che le cellule con macchie di nanofili stampate sulla parte superiore apparivano sane e in grado di migrare, con gli array che rimanevano sulle cellule molli anche mentre si muovevano.

Il minuscolo sensore misura simultaneamente l'attività elettrica e meccanica nelle cellule cardiache
"Abbiamo dimostrato che possiamo attaccare nanomodelli complessi alle cellule viventi, garantendo al tempo stesso che la cellula non muoia", afferma Gracias. "È un risultato molto importante che le cellule possano vivere e muoversi con i tatuaggi perché spesso c'è una significativa incompatibilità tra le cellule viventi e i metodi utilizzati dagli ingegneri per fabbricare l'elettronica."
Gracias e colleghi concludono che il loro processo di nanopatterning, combinato con tecniche di microfabbricazione standard, “apre opportunità per lo sviluppo di nuovi substrati di colture cellulari, materiali bioibridi, dispositivi bionici e biosensori”. Successivamente, intendono provare ad attaccare nanocircuiti più complessi che possano rimanere sul posto per periodi più lunghi, oltre a sperimentare diversi tipi di cellule.
- Distribuzione di contenuti basati su SEO e PR. Ricevi amplificazione oggi.
- PlatoData.Network Generativo verticale Ai. Potenzia te stesso. Accedi qui.
- PlatoAiStream. Intelligenza Web3. Conoscenza amplificata. Accedi qui.
- PlatoneESG. Automobilistico/VE, Carbonio, Tecnologia pulita, Energia, Ambiente, Solare, Gestione dei rifiuti. Accedi qui.
- Platone Salute. Intelligence sulle biotecnologie e sulle sperimentazioni cliniche. Accedi qui.
- Grafico Prime. Migliora il tuo gioco di trading con ChartPrime. Accedi qui.
- BlockOffset. Modernizzare la proprietà della compensazione ambientale. Accedi qui.
- Fonte: https://physicsworld.com/a/researchers-tattoo-gold-nanopatterns-onto-live-cells/
- :ha
- :È
- :non
- $ SU
- 16
- 200
- 24
- 8
- a
- capacità
- capace
- WRI
- attività
- aderire
- avanzamenti
- Dopo shavasana, sedersi in silenzio; saluti;
- anche
- tra
- an
- ed
- apparso
- applicazioni
- approccio
- circa
- SONO
- in giro
- Italia
- AS
- montaggio
- valutare
- At
- allegare
- BE
- perché
- essendo
- fra
- stile di vita
- legame
- Cervello
- ma
- Materiale
- Celle
- caratterizzare
- clicca
- colleghi
- combinato
- compatibile
- complesso
- concludere
- contrasto
- di controllo
- convenzionale
- costo effettivo
- potuto
- creare
- Cultura
- giorno
- dimostrare
- progettato
- sviluppato
- Mercato
- dispositivi
- DID
- *
- diverso
- malattie
- non
- In precedenza
- Elettronico
- Elettronica
- enable
- abilitato
- Ingegneri
- assicurando
- Intero
- Anche
- Spiega
- più veloce
- finale
- I risultati
- Nome
- flessibile
- Nel
- da
- ulteriormente
- GAO
- generalmente
- vetro.
- Oro
- Crescita
- guida
- ha avuto
- Avere
- capo
- Salute e benessere
- sano
- Cuore
- Alta
- ad alta risoluzione
- hopkins
- Tuttavia
- HTTPS
- umano
- Immagine
- importante
- in
- individuale
- informazioni
- creativi e originali
- integrare
- isolato
- problema
- IT
- johns
- Johns Hopkins University
- jpg
- strato
- leader
- principale
- lasciare
- Livello
- piace
- vivere
- vita
- a lungo termine
- più a lungo
- fatto
- Materiale
- max-width
- può essere
- analisi
- meccanico
- meccanismi di
- Media
- Unire
- metodo
- metodi
- Microscopia
- migrare
- migrato
- migrazione
- monitoraggio
- Scopri di più
- cambiano
- mosso
- Film
- molti
- di applicazione
- New
- GENERAZIONE
- oggetto
- ostacoli
- of
- di frequente
- on
- ONE
- su
- aprire
- Opportunità
- OTTIMIZZA
- or
- ancora
- Superare
- per una notte
- Parallel
- Patch
- Cartamodello
- periodi
- Fisica
- Mondo della fisica
- posto
- piano
- Platone
- Platone Data Intelligence
- PlatoneDati
- posizionato
- possibile
- stampa
- Stampa
- stampa
- processi
- i processi
- Mettendo
- casuale
- RAT
- di rose
- tempo reale
- registrato
- è rimasta
- rimanente
- a distanza
- Reportistica
- richiedere
- riparazioni
- ricercatori
- Risoluzione
- colpevole
- Rivelato
- robusto
- approssimativamente
- dice
- visto
- selettivo
- sensore
- Forma
- foglio
- ha mostrato
- mostrato
- significativa
- Silicio
- contemporaneamente
- Taglia
- inferiore
- smart
- Soft
- qualcosa
- Standard
- dichiarazione
- soggiorno
- step
- forza
- studi
- tale
- suggerire
- superficie
- parlando
- team
- tecniche
- Tecnologie
- decine
- di
- che
- Il
- loro
- poi
- Strumenti Bowman per analizzare le seguenti finiture:
- di
- questo
- quelli
- miniature
- tempo
- volte
- a
- top
- verso
- pista
- trasferimento
- trattare
- vero
- prova
- Due volte
- Tipi di
- in definitiva
- Università
- fino a quando
- uso
- utilizzato
- Vuoto
- molto
- vitalità
- aspettare
- Prima
- we
- WELL
- mentre
- quale
- while
- tutto
- largo
- con
- mondo
- zefiro