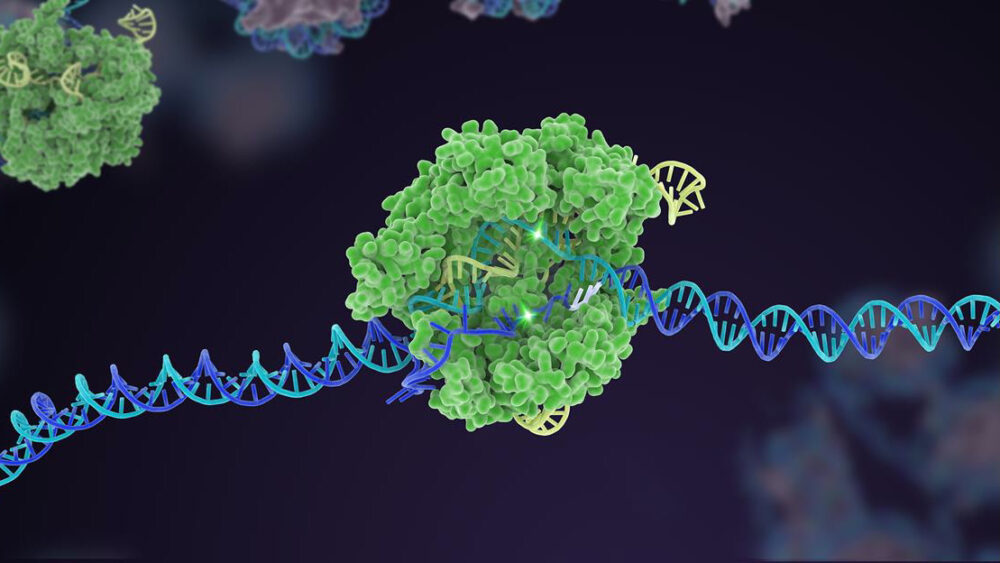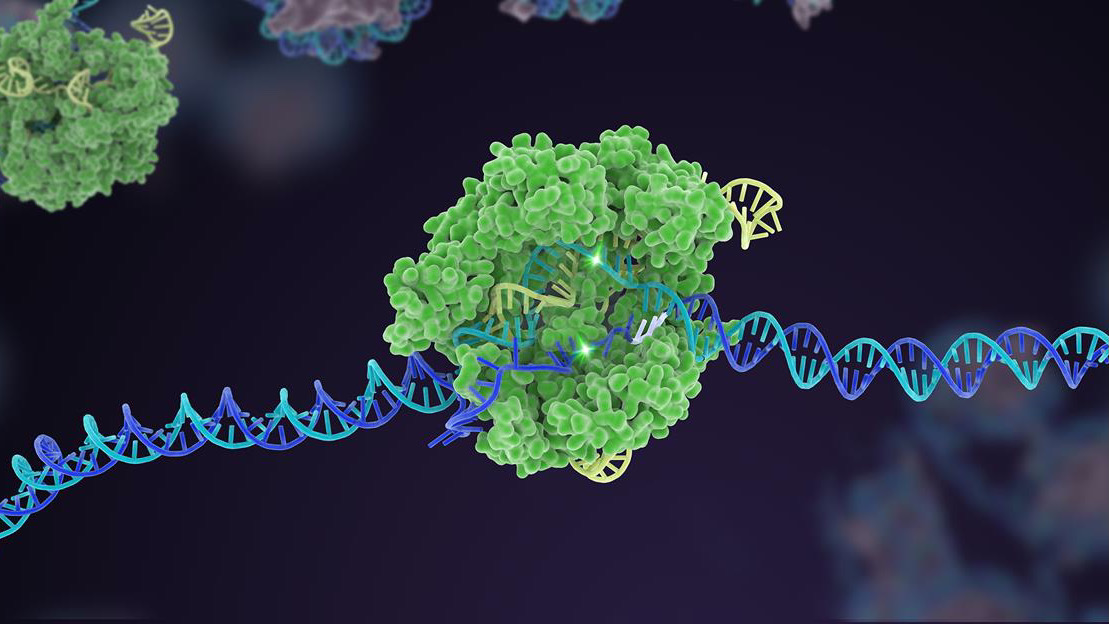
לפני עשר שנים, מנגנון הגנה לא מוכר של חיידקים זינק לתהילה כעורך גנום רב עוצמה. בעשור שחלפו מאז, CRISPR-Cas9 יצרה גרסאות מרובות, והתרחבה לארגז כלים מקיף שיכול לערוך את הקוד הגנטי של החיים.
הרחק ממרדף אחר מגדל השן, השימושים המעשיים שלו במחקר, בריאות וחקלאות הגיעו מהר וזועם.
ראית את הכותרות. ה-FDA אישר את השימוש בו ב התמודדות עם המוטציה הגנטית הבסיסית למחלת תאי חרמש. כמה חוקרים ערכו תאי חיסון כדי להילחם בסרטן דם בלתי ניתן לטיפול בילדים. אחרים לקחו השתלות איברים מחזיר לאדם מחלום למציאות בניסיון להקל על המחסור באיברים תורמים. העבודה האחרונה שואפת לעזור למיליוני אנשים עם כולסטרול גבוה - ואולי להביא טיפול גנטי מבוסס CRISPR להמונים - על ידי להפחית את הסיכויים שלהם למחלות לב עם זריקה בודדת.
אבל לד"ר ג'ניפר דודנה, שזכתה בפרס נובל לשנת 2020 על תפקידה בפיתוח CRISPR, אנחנו רק מגרדים את פני השטח של הפוטנציאל שלו. יחד עם הסטודנטית לתואר שני ג'וי וואנג, דודנה הניחה מפת דרכים לעשור הבא של הטכנולוגיה במאמר in מדע.
אם שנות ה-2010 היו מתמקדות בהקמת ארגז הכלים של CRISPR ובהוכחת יעילותו, בעשור זה הטכנולוגיה ממצה את מלוא הפוטנציאל שלה. מטיפולים מבוססי CRISPR ומסכים בקנה מידה גדול לאבחון מחלות ועד להנדסת יבולים בעלי תשואה גבוהה ומזון מזין, הטכנולוגיה "והשפעתה הפוטנציאלית עדיין בשלבים הראשונים שלהם", כתבו המחברים.
עשור של הבהרה
שפכנו הרבה דיו על התקדמות CRISPR, אבל כדאי לחזור על העבר כדי לחזות את העתיד - ואולי לחפש בעיות בדרך.
גולת כותרת מוקדמת אחת הייתה היכולת המדהימה של CRISPR להנדס במהירות מודלים של מחלות של בעלי חיים. צורתו המקורית גוזרת בקלות גן ממוקד בעובר מוקדם מאוד, שכאשר מושתל ברחם יכול ליצור עכברים מהונדסים גנטית תוך חודש בלבד, בהשוואה לשנה בשיטות קודמות. גרסאות נוספות של CRISPR, כמו עריכת בסיס - החלפת אות גנטית אחת באחרת - ועריכה ראשונית - שחותכת את ה-DNA מבלי לחתוך את שני הגדילים - הגבירו עוד יותר את הגמישות של ערכת הכלים בהנדסת אורגנואידים שהשתנו גנטית (לחשוב מיני מוחות) ובעלי חיים. CRISPR הקימה במהירות עשרות מודלים לכמה מהמחלות ההרסניות והמבלבלות ביותר שלנו, כולל סוגי סרטן שונים, אלצהיימר וניוון שרירים דושן - הפרעה ניוונית שבה השריר מתפוגג לאט. עשרות ניסויים מבוססי CRISPR נמצאים כעת בעבודה.
CRISPR גם האיץ את הבדיקות הגנטיות לעידן הביג דאטה. במקום לכוון לגן אחד בכל פעם, אפשר כעת להשתיק, או להפעיל, אלפי גנים במקביל, וליצור מעין אבן רוזטה לתרגום הפרעות גנטיות לשינויים ביולוגיים. זה חשוב במיוחד להבנת אינטראקציות גנטיות, כמו אלו בסרטן או הזדקנות שלא היינו מודעים להן בעבר, ולהשיג תחמושת חדשה לפיתוח תרופות.
אבל הישג מכריע עבור CRISPR היה עריכה מרובה. כמו הקשה בו זמנית על מקשי פסנתר מרובים, סוג זה של הנדסה גנטית מכוון למספר אזורי DNA ספציפיים, ומשנה במהירות את המבנה הגנטי של הגנום במכה אחת.
הטכנולוגיה פועלת בצמחים ובבעלי חיים. במשך עידנים, אנשים גידלו בקפידה יבולים עם תכונות רצויות - בין אם זה צבע, גודל, טעם, תזונה או חוסן מחלות. CRISPR יכול לעזור לבחור תכונות מרובות או אפילו לביית יבולים חדשים בדור אחד בלבד. שוורים חסרי קרניים שנוצרו על ידי CRISPR, עגבניות עשירות בחומרים מזינים, וחיות משק יתר שריריות ודגים הם כבר מציאות. עם אוכלוסיית העולם הגיע ל-8 מיליארד ב-2022 ו מיליונים הסובלים מרעב, גידולי CRISPRed עשויים להוות חבל הצלה - כלומר, אם אנשים מוכנים לקבל את הטכנולוגיה.
הדרך קדימה
לאן אנחנו הולכים מכאן?
לכותבים, עלינו להגביר עוד יותר את האפקטיביות של CRISPR ולבנות אמון. המשמעות היא לחזור ליסודות כדי להגביר את דיוק העריכה והדיוק של הכלי. כאן, פלטפורמות להתפתחות מהירה של אנזימי Cas, מרכיב ה"מספריים" של מכונות CRISPR, הן קריטיות.
כבר היו הצלחות: גרסת Cas אחת, לדוגמה, משמש כמעקה בטיחות לרכיב המכוון - ה-sgRNA "כלב דם". ב-CRISPR הקלאסי, ה-sgRNA עובד לבד, אבל בגרסה המעודכנת הזו, הוא מתקשה להיקשר ללא סיוע של Cas. הטריק הזה עוזר להתאים את העריכה לאתר DNA ספציפי ומגביר את הדיוק כך שהחתך יעבוד כמצופה.
אסטרטגיות דומות יכולות גם להגביר את הדיוק עם פחות תופעות לוואי או להכניס גנים חדשים לתאים כגון נוירונים ואחרים שאינם מתחלקים עוד. למרות שכבר אפשרי עם עריכת פריים, היעילות שלה יכולה להיות נמוך פי 30 מאשר מנגנוני CRISPR קלאסיים.
"מטרה עיקרית לעריכת פריים בעשור הקרוב היא שיפור היעילות מבלי לפגוע בטוהר המוצר בעריכה - תוצאה שיש לה פוטנציאל להפוך את עריכת הפריים לאחד הכלים המגוונים ביותר לעריכה מדויקת", אמרו המחברים.
אבל אולי חשוב יותר הוא הלידה, שנותרה צוואר בקבוק במיוחד עבור טיפולים. נכון להיום, משתמשים ב-CRISPR בדרך כלל על תאים מחוץ לגוף המוזרמים בחזרה - כמו במקרה של CAR-T - או במקרים מסוימים, קשורים לנשא ויראלי או מובלעים בבועות שומן ומוזרקים לגוף. היו הצלחות: ב2021, ה-FDA אישר את זריקה ראשונה מבוססת CRISPR להתמודד עם מחלת דם גנטית, טרנסטירטין עמילואידוזיס.
עם זאת, שתי האסטרטגיות בעייתיות: לא הרבה סוגים של תאים יכולים לשרוד את הטיפול ב-CAR-T - למות כאשר הם מוכנסים מחדש לגוף - והכוונה לרקמות ואיברים ספציפיים נותרת לרוב מחוץ להישג ידם לטיפולים בהזרקה.
התקדמות מרכזית לעשור הבא, אמרו המחברים, היא להעביר את מטען CRISPR לתוך הרקמה הממוקדת ללא נזק ולשחרר את עורך הגנים במקום המיועד לו. כל אחד מהשלבים הללו, למרות שהוא לכאורה פשוט על הנייר, מציג את סט האתגרים שלו שידרשו גם הנדסה ביולוגית וגם חדשנות כדי להתגבר עליהם.
לבסוף, CRISPR יכול לעשות סינרגיה עם התקדמות טכנולוגית אחרת, אמרו המחברים. לדוגמה, על ידי שימוש בהדמיית תאים ולמידת מכונה, נוכל בקרוב להנדס עורכי גנום יעילים אף יותר. הודות ל רצף DNA מהיר וזול יותר, לאחר מכן נוכל לעקוב בקלות אחר השלכות עריכת גנים. נתונים אלה יכולים לספק מעין מנגנון משוב שבעזרתו ניתן להנדס עורכי גנום חזקים עוד יותר בלולאה טובה.
השפעה על העולם האמיתי
למרות שהרחבה נוספת של ארגז הכלים של CRISPR עומדת על הפרק, הטכנולוגיה בשלה מספיק כדי להשפיע על העולם האמיתי בעשור השני שלה, אמרו המחברים.
בעתיד הקרוב, אנו אמורים לראות "מספר מוגבר של טיפולים מבוססי CRISPR עוברים לשלבים מאוחרים יותר של ניסויים קליניים." בהסתכלות קדימה, הטכנולוגיה, או הגרסאות שלה, עשויות להפוך השתלות קסנו של חזיר לאיבר לאדם לשגרתי, ולא ניסיוני. בדיקות בקנה מידה גדול לגנים שמובילים להזדקנות או למחלות מוח או לב ניווניות - הרוצחים המובילים שלנו כיום - יכולים להניב טיפולים מונעים מבוססי CRISPR. זו משימה לא פשוטה: אנו זקוקים הן לידע על הגנטיקה העומדת בבסיס מחלות גנטיות רב-גוניות - כלומר, כאשר מספר גנים נכנסים לפעולה - והן לדרך להעביר את כלי העריכה ליעדם. "אבל היתרונות הפוטנציאליים עשויים להניע חדשנות בתחומים אלה הרבה מעבר למה שאפשרי היום", אמרו המחברים.
אבל עם כוח גדול יותר באה אחריות גדולה יותר. CRISPR התקדמה במהירות מסחררת, וסוכנויות הרגולציה והציבור עדיין נאבקים להדביק את הפער. אולי הדוגמה הידועה ביותר לשמצה הייתה זו של תינוקות CRISPR, שבו בוצעו ניסויים כנגד הנחיות אתיות גלובליות מונע קונסורציום בינלאומי לקביעת קו אדום לעריכת תאי נבט אנושיים.
באופן דומה, אורגניזמים מהונדסים גנטית (GMO) נותרו נושא שנוי במחלוקת. למרות ש-CRISPR הוא הרבה יותר מדויק מכלים גנטיים קודמים, זה יהיה תלוי בצרכנים להחליט אם לברך דור חדש של מזונות שהתפתחו על ידי האדם-צומח ובעלי חיים כאחד.
אלו הם שיחות חשובות שצריכות שיח גלובלי כאשר CRISPR נכנסת לעשור השני שלה. אבל בעיני המחברים, העתיד נראה מזהיר.
"בדיוק כמו במהלך הופעתה של עריכת גנום CRISPR, שילוב של סקרנות מדעית והרצון להועיל לחברה יניע את העשור הבא של חדשנות בטכנולוגיית CRISPR", אמרו. "על ידי המשך לחקור את העולם הטבעי, נגלה את מה שלא ניתן לדמיין ונכניס אותו לשימוש בעולם האמיתי לטובת כדור הארץ."
תמונת אשראי: NIH
- הפצת תוכן ויחסי ציבור מופעל על ידי SEO. קבל הגברה היום.
- Platoblockchain. Web3 Metaverse Intelligence. ידע מוגבר. גישה כאן.
- מקור: https://singularityhub.com/2023/01/25/crisprs-wild-first-decade-only-scratches-the-surface-of-its-potential/
- 2020
- a
- יכולת
- מוּאָץ
- לְקַבֵּל
- דיוק
- הישג
- מעשים
- נוסף
- לקדם
- מתקדם
- התקדמות
- הִתגַלוּת
- נגד
- סוכנויות
- סדר יום
- הזדקנות
- חקלאות
- קדימה
- מטרות
- להקל
- לבד
- כְּבָר
- למרות
- אלצהיימר
- תחמושת
- ו
- בעלי חיים
- בעלי חיים
- מאושר
- אזורים
- סיוע
- מחברים
- בחזרה
- בסיס
- יסודות
- תועלת
- הטבות
- ברקלי
- מעבר
- גָדוֹל
- נתונים גדולים
- B
- לאגד
- דם
- בלומברג
- גוּף
- לְהַגבִּיר
- שיפרה
- מוֹחַ
- להביא
- לִבנוֹת
- בניית אמון
- מחלת הסרטן
- לא יכול
- מקרה
- מקרים
- היאבקות
- תאים
- האתגרים
- סיכויים
- שינויים
- משתנה
- זול יותר
- קלאסי
- קליני
- ניסויים קליניים
- קוד
- צֶבַע
- שילוב
- איך
- לעומת
- רְכִיב
- מַקִיף
- מתפשר
- השלכות
- קונסורציום
- צרכנים
- ממשיך
- שנוי במחלוקת
- שיחות
- יכול
- אשראי
- CRISPR
- קריטי
- יבולים
- סקרנות
- כיום
- חותך
- גזירה
- נתונים
- עָשׂוֹר
- גופי בטחון
- למסור
- מסירה
- מתפתח
- צעצועי התפתחות
- לגלות
- מַחֲלָה
- מחלות
- ה-DNA
- מטה
- עשרות
- חלום
- נהיגה
- תרופה
- בְּמַהֲלָך
- כל אחד
- מוקדם
- בקלות
- עורך
- יְעִילוּת
- תופעות
- יְעִילוּת
- יעיל
- כמוס
- מהנדס
- הנדסה
- נכנס
- במיוחד
- נוסד
- מקימים
- אֶתִי
- אֲפִילוּ
- להתפתח
- דוגמה
- הרחבת
- לחקור
- מוניטין
- משק
- מהר
- ה-FDA
- מָשׁוֹב
- להלחם
- ראשון
- גמישות
- מרוכז
- מזונות
- טופס
- החל מ-
- מלא
- נוסף
- עתיד
- זכייה
- בדרך כלל
- ליצור
- דור
- הנדסה גנטית
- גנטיקה
- גלוֹבָּלִי
- Go
- מטרה
- הולך
- בוגר
- יותר
- הנחיות
- כותרות
- בריאות
- לֵב
- לעזור
- עוזר
- כאן
- גָבוֹהַ
- להבליט
- HTTPS
- בן אנוש
- הדמיה
- פְּגִיעָה
- חשוב
- שיפור
- in
- כולל
- להגדיל
- גדל
- עליות
- מדהים
- חדשנות
- יחסי גומלין
- ברמה בינלאומית
- IT
- ג'ניפר
- רק אחד
- מפתח
- מפתחות
- רוצחים
- סוג
- ידע
- בקנה מידה גדול
- עוֹפֶרֶת
- למידה
- לְהַלווֹת
- מכתב
- החיים
- קו
- עוד
- הסתכלות
- נראה
- מכונה
- למידת מכונה
- מכונות
- ראשי
- לעשות
- איפור
- רב
- בוגר
- אומר
- מנגנון
- שיטות
- מיליונים
- מודלים
- שונים
- צג
- חוֹדֶשׁ
- יותר
- יותר יעיל
- רוב
- נע
- רב פנים
- מספר
- טבעי
- טבע
- ליד
- צורך
- נוירונים
- חדש
- הבא
- שירותי הבריאות
- NIH
- פרס נובל
- יָדוּעַ לְשִׁמצָה
- מספר
- ONE
- מְקוֹרִי
- אחר
- אחרים
- בחוץ
- להתגבר על
- שֶׁלוֹ
- מאמר
- מקביל
- עבר
- נתיב
- מדינה
- אֲנָשִׁים
- אוּלַי
- כוכב לכת
- צמחים
- פלטפורמות
- אפלטון
- מודיעין אפלטון
- אפלטון נתונים
- שפע
- אוכלוסייה
- אפשרי
- פוטנציאל
- פוטנציאל
- כּוֹחַ
- חזק
- מעשי
- דיוק
- לחזות
- חזה
- מתנות
- קודם
- קוֹדֶם
- ראשוני
- הפרס
- בעיות
- המוצר
- לספק
- ציבורי
- גם
- מהר
- לְהַגִיעַ
- מגיע
- ממשי
- עולם אמיתי
- מציאות
- לאחרונה
- Red
- רגולטורים
- לשחרר
- להשאר
- שְׂרִידִים
- לדרוש
- מחקר
- חוקרים
- כושר התאוששות
- אחריות
- עשיר
- מפת דרכים
- תפקיד
- אמר
- מדע
- לְגַשֵׁשׁ
- סריקה
- מסכים
- שְׁנִיָה
- סט
- מחסור
- צריך
- צד
- שתיקה
- פָּשׁוּט
- בו זמנית
- since
- יחיד
- אתר
- מידה
- לאט
- So
- חֶברָה
- כמה
- ספציפי
- מְהִירוּת
- מסחרי
- הסתובב
- שלבים
- צעדים
- עוד
- אבן
- אסטרטגיות
- מאבקים
- נאבק
- סטודנט
- כזה
- סֵבֶל
- משטח
- לשרוד
- יעד
- ממוקד
- מיקוד
- מטרות
- המשימות
- טכנולוגי
- טכנולוגיה
- אל האני
- היסודות
- העולם
- שֶׁלָהֶם
- תוֹרַת הָרִפּוּי
- אלפים
- זמן
- פִּי
- ל
- היום
- יַחַד
- ארגז כלים
- כלים
- חלק עליון
- נושא
- מגדל
- ניסויים
- סומך
- תור
- סוגים
- UN
- בְּסִיסִי
- הבנה
- מְעוּדכָּן
- להשתמש
- שונים
- רב צדדי
- גרסה
- ברוך הבא
- מה
- מה
- אם
- אשר
- בזמן
- מי
- בר
- יצטרך
- מוכן
- לְלֹא
- נצחנות
- תיק עבודות
- עובד
- עוֹלָם
- שנה
- שנים
- תְשׁוּאָה
- זפירנט