תשאלו חוקר סרטן מהו הטיפול פורץ הדרך של העשור, והם יגידו לכם ש-CAR T לוקח את הכתר.
הטיפול מהנדס גנטית את תאי החיסון של האדם עצמו, והופך אותם לחיילי על שצדים תאי דם סרטניים. במהירות מדהימה, יש טיפולי CAR T מרובים אושרה על ידי ה-FDA עבור סוגי סרטן דם שלא ניתן היה לטפל בהם בעבר. עד כה, למעלה מ-15,000 חולים טופלו בטיפול.
לד"ר קארל יוני, חלוץ הטכנולוגיה באוניברסיטת פנסילבניה, אנחנו רק מגרדים את פני השטח של הפוטנציאל של CAR T.
ב פרספקטיבה מאמר שפורסם ב טבע השבוע, יוני ועמיתיו קבעו דרך קדימה.
בשורשו, טיפול ב-CAR T נוגע ל"אינסטינקט הרוצח" הטבעי של סוג של תא חיסון, הנקרא תא T, ומכוון אותו למטרה מסוימת - למשל, תאי סרטן בדם. אבל עם עיצוב מחדש קפדני, ניתן להנדס גנטית טיפול ב-CAR T כדי להתמודד עם מגוון רחב של האויבים הרפואיים הבולטים של האנושות: מחלות אוטואימוניות, אסטמה ו לֵבמחלות כבד וכליות הנגרמות על ידי התקשות שרירים יותר ויותר.
מסקרן אפילו יותר, CAR T עשוי לעזור לנקות תאי "זומבי" מזדקנים, הקשורים למחלות הקשורות לגיל, או להילחם ב-HIV ומחלות זיהומיות ויראליות אחרות.
"אנחנו רק מתחילים לממש את מלוא הפוטנציאל של הסם החי הזה", אמר המחברים.
מה זה שוב CAR T?
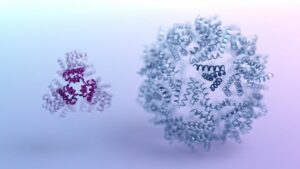
CAR T מייצג "טיפול בקולטן כימרי לאנטיגן T". אני אוהב לחשוב על זה כעל ראש תפוחי אדמה עם קטעי הצמד-אנד-פליי.
"תפוח האדמה" הליבה הוא תא ה-T החיסוני, משפחה של תאים שבדרך כלל סוקרים את גופנו כדי לחפש ולהשמיד פולשים כמו סרטן או זיהומים. הוסף לזה "חלקים" של מכונית: "ווים" של חלבון מהונדסים גנטית שיכולים לתפוס חלבון ספציפי בתא חולה.
CAR T פותח לראשונה כדי להילחם ב-HIV - עם תוצאות חסרות ברק - אך הוא עלה לגדולה בשל יעילותו בטיפול בסרטן הדם. כך זה קורה בדרך כלל: תאי T של מטופל מבודדים מהוצאת דם ומשופרים גנטית עם מבני חלבון CAR במעבדה. לאחר שהוזרמו בחזרה לגוף, חיילי העל מתחמקים מההגנה של תאי הגידול, כאשר תא מהונדס בודד הורג מאות אם לא אלפי אויבים סרטניים.
CAR T הוא באמת "עמוד חדש של טיפול", אמרו המחברים. אם תאי T מעורבים במחלות אחרות, האם הטיפול יכול לעשות יותר?
מאבק איתן
המהלך הראשון להרחבת CAR T מעבר לסרטן הדם הוא התמקדות בסוגי סרטן מוצקים - חשבו על הלבלב, השד, המעי הגס ואחרים. למרבה הצער, התוצאות "מאכזבות במידה רבה" במספר ניסויים קליניים עד כה, אמרו המחברים.
אבל מהכישלונות האלה, למדנו המון. בניגוד לסרטני דם, גידולים מוצקים בונים "מבצר" ביולוגי מקומי ומוציאים כימיקלים שמרחיקים את תאי ה-T ומעכבים את פעילותם ההרסנית. רעיון אחד לעזור להם לפרוץ דרך הוא הזרקה ישירה של תאי CAR T לגידולים. אחר הוא להשתמש CRISPR לצייד תאי CAR T עם פרופיל גנטי - הוספה או מחיקה של גנים מסוימים - שמתחמק מההגנות הללו.
למרבה הצער, חסמים אחרים נותרו. גידולים מוצקים מורכבים לרוב מאמלגם של תאים, שלכל אחד מהם טביעת אצבע מובהקת של חלבוני פני השטח. זה מקשה על עיצוב CAR T יחיד לצוד את כל התאים הסרטניים. יעדי חלבון מסוימים, הנקראים אנטיגנים, מנקדים גם את החלק החיצוני של תאים בריאים, וגורמים לנזק נלווה.
אז יש סיכוי לעורר הוריקן חיסוני. כאן, תאי CAR T מתרחבים במהירות בתוך הגוף כדי להילחם ביעד הסרטני שלהם, אך בתורם דוחפים את המערכת החיסונית של הגוף למצב משבר - מצב שנקרא "תסמונת שחרור ציטוקינים". התוצאה הסופית עלולה להיות הרסנית, עם חום, ירידה מהירה בלחץ הדם, ואפילו אי ספיקת איברים רבים.
כמו בכל תרופה אחרת, המינון הוא המפתח. אחת הדרכים הפוטנציאליות למנוע דחף חיסוני היא לתת לתאי T דחיפה מוגבלת בזמן. במקום להוסיף CAR ישירות לקוד הגנטי של התא שהופך אותם לצמיתות לחיילי-על CAR T, פתרון עוקף הוא שימוש ב-mRNA - ה"מתרגם" של הגנים. התוצאה הסופית דומה, כשהתא מתאים לפעולה עם חלבוני ה-CAR החדשים שלו. אבל בניגוד להחדרות גנטיות, mRNA הוא זמני, כלומר תאי CAR T יכולים להשיל את דמות חיילי העל שלהם ולחזור לזהות תאי ה-T הרגילה שלהם - בתורו לאפשר למערכת החיסון להירגע.
יקום מתרחב
קשה לפצח סוגי סרטן מוצקים, אבל החדשות הטובות הן שההגנות שלהם לא קיימות עבור מחלות אחרות. לדוגמה, להפרעות אוטואימוניות, סוכרת, התקשות שרירי הלב או תאי זומבים בדרך כלל אין מבצר מגן, כלומר קל יותר ל-CAR T להיכנס ולשמור על הפעילות ההורגת שלהם. בניגוד לסוגי סרטן - הידועים לשמצה ביכולתם לעבור מוטציה - למחלות אלו יש לרוב פרופיל גנטי יציב, כך שמכוניות CAR יכולות לשמור על יעילותן.
עד כה, השימוש המבטיח ביותר ב-CAR T מחוץ לסרטן הוא למחלות אוטואימוניות.
חזרה ל- 2022, ניסוי קליני קטן בחולים עם זאבת אדמנתית מערכתית (SLE) - הפרעה אוטואימונית מסכנת חיים - מצא שתאי CAR T התרחבו במהירות בגופם והקלו על התסמינים.
SLE הוא הסוג הנפוץ ביותר של זאבת. כאן, מערכת החיסון של הגוף מנהלת מלחמה על הרקמות שלה. האשם העיקרי הוא סוג אחר של תא חיסון, הנקרא תא B, אשר בדרך כלל מייצר נוגדנים כדי להדוף זיהומים. במחלות אוטואימוניות, תאי B בטעות חבר בתור אויב, מתייגים רקמות בריאות - לב, ריאות, כליות - כמטרות לחיסול.
לאחר טיפול ב-CAR T, אף אחד מחמשת האנשים בניסוי לא הסתמך יותר על תרופות מדכאות חיסון יומיות. באופן מפתיע, תאי ה-B שלהם חזרו כמה חודשים לאחר מכן, אך ללא תסמינים או נזק לאיברים שלהם.
באחר הוכחה של רעיון או תאוריה, צוות השתמש ב-CAR T עבור חולה עם תסמונת אנטי-סינטטאז, מחלה אוטואימונית הורסת את הריאות והשרירים וגורמת לדלקת פרקים. שלושה חודשים לאחר מכן, השרירים של החולה השתפרו, יחד עם פחות דלקות בריאות.
מדענים הם עכשיו מתנסה עם CAR T בדגמי עכברים של אסתמה קשה, כאשר התאים מגינים מפני התקפים קשים הנמשכים זמן רב לאחר הטיפול עצמו. מאמצים אחרים הם התמודדות עם מחלות אוטואימוניות, כגון דלקת מפרקים שגרונית וטרשת נפוצה, המשפיעות על מעטפת המגן סביב העצבים.
למרות שהן מבטיחות, תצורות CAR T הנוכחיות אינן מבחינות בין תאי B בריאים או חולים. מאמצים מרובים מייעלים את ה"ווים" של CAR כדי למקד ספציפית למזיקים. מחקר אחד בעכברים להמופיליה - הפרעת דימום - גילו שהעיצובים החדשים יותר השאירו תאי B בריאים לבד. ניסויים קליניים לבדיקת העיצוב נמצאים בעיצומם.
המערב הפרוע
כאן CAR T נעשה ניסיוני באמת.
קח פיברוזיס לב - התקשות של שרירי הלב - אשר יכול לקרות לאחר פציעה או מחלה כרונית או במהלך ההזדקנות, ובסופו של דבר מוביל לאי ספיקת לב. יש מעט אפשרויות טיפול.
בהוכחה לקונספט, מחקר בשנה שעברה נמצא שתכנות מחדש ישירות של תאי T בתוך גופם של עכברים באמצעות mRNA הפך רקמת צלקת בליבם לאחר הזרקה בודדת. פיברוזיס לא קורה רק ללבבות. גם הכבד, הכליות, הריאות והשרירים סובלים מהתקשות דומה, מה שהופך אותם למטרות אידיאליות לטיפול ב-CAR T.
"עם מחסור בטיפולים המכוונים ישירות לפיברוזיס, תאי CAR T עשויים לספק דרך חזקה וסלקטיבית לטיפול במחלות כאלה", אמרו המחברים.
אבל אולי השימוש הנועז ביותר בטיפול ב-CAR T הוא השמדת תאי "זומבי" מזדקנים. למרות שהם חיים, תאים אלה אינם ממלאים את חובותיהם הרגילות, במקום זאת מזרימים צוות של מולקולות רעילות אל סביבתם. טונות של עדות מופעים שהסרת תאים אלה באמצעות כימיקלים או הנדסה גנטית מגדילה את תוחלת הבריאות, אך עם יעילות משתנה.
כאן CAR T יכול לעזור. לתאים מזדקנים יש אנטיגנים ספציפיים, מה שהופך אותם למטרות מושלמות לטיפול. מחקר אחד שטיפל בעכברים עם סרטן ריאות ומחלות כבד גילה שהסרת תאי זומבים האריכה חיים.
סיכום? תאי CAR T מתרחבים במהירות מעבר לאונקולוגיה. נותרו חסימות דרכים: הטיפול יקר מאוד ועלול להיות מסוכן להפעלת סערות חיסוניות. אנחנו עדיין לא יודעים אם התאים יכולים להזיק - או להצעיר - רקמות בריאות בזמן שהם מנווטים בגוף.
אבל לכותבים, אנחנו נכנסים לפרק הבא של טיפול טרנספורמטיבי. "היישומים התיאורטיים הם עצומים, והפלטפורמה חזקה... אנחנו רק מתחילים לממש את מלוא הפוטנציאל של התרופה החיה הזו."
תמונת אשראי: לאבן / Shutterstock.com
- הפצת תוכן ויחסי ציבור מופעל על ידי SEO. קבל הגברה היום.
- PlatoData.Network Vertical Generative Ai. העצים את עצמך. גישה כאן.
- PlatoAiStream. Web3 Intelligence. הידע מוגבר. גישה כאן.
- PlatoESG. רכב / רכבים חשמליים, פחמן, קלינטק, אנרגיה, סביבה, שמש, ניהול פסולת. גישה כאן.
- BlockOffsets. מודרניזציה של בעלות על קיזוז סביבתי. גישה כאן.
- מקור: https://singularityhub.com/2023/07/28/the-living-drug-car-t-is-evolving-beyond-just-treating-cancer/
- :הוא
- :לֹא
- :איפה
- $ למעלה
- 000
- 15%
- 23
- a
- יכולת
- פעולה
- פעילות
- להוסיף
- מוסיף
- להשפיע על
- לאחר
- שוב
- נגד
- הזדקנות
- תעשיות
- מאפשר
- לבד
- לאורך
- גם
- למרות
- an
- ו
- אחר
- כל
- יישומים
- ARE
- סביב
- מאמר
- AS
- At
- המתקפות
- מחברים
- לְהִמָנַע
- בחזרה
- מחסומים
- קרב
- מִפרָץ
- BE
- היה
- ההתחלה
- להיות
- בֵּין
- מעבר
- מדמם
- דם
- לחץ דם
- גופים
- גוּף
- לְהַגבִּיר
- לשבור
- פריצת דרך
- לִבנוֹת
- אבל
- by
- נקרא
- CAN
- מחלת הסרטן
- תאים סרטניים
- מכונית
- זהיר
- , קרל
- מכוניות
- גרם
- גורמים
- גורם
- תאים
- מסוים
- סיכוי
- הפרק
- קליני
- ניסויים קליניים
- קוד
- עקיף
- עמיתים
- Common
- מורכב
- מושג
- מצב
- ליבה
- סדק
- אשראי
- משבר
- כתר
- נוֹכְחִי
- יומי
- מסוכן
- עָשׂוֹר
- עיצוב
- עיצובים
- להרוס
- הרסנית
- מפותח
- סוכרת
- קשה
- ישירות
- מַחֲלָה
- מחלות
- הפרעות
- מובהק
- do
- לא
- לא
- נקודה
- מטה
- dr
- לצייר
- נהיגה
- ירידה
- תרופה
- סמים
- בְּמַהֲלָך
- כל אחד
- קל יותר
- יעילות
- מַאֲמָצִים
- סוף
- אויבים
- הנדסה
- מהנדסים
- משופר
- הזנת
- אֲפִילוּ
- בסופו של דבר
- דוגמה
- להתקיים
- לְהַרְחִיב
- מורחב
- הרחבת
- יקר
- כשלון
- משפחה
- רחוק
- ה-FDA
- מעטים
- להלחם
- טביעת אצבעות
- ראשון
- בעד
- מבצר
- קדימה
- מצא
- חבר
- החל מ-
- הגשמה
- מלא
- בדרך כלל
- הנדסה גנטית
- לתת
- Goes
- טוב
- לתפוס
- לקרות
- קשה
- מזיק
- יש
- ראש
- בריא
- לֵב
- אִי סְפִיקַת הַלֵב
- לעזור
- כאן
- מאוד
- להחזיק
- איך
- HTTPS
- אנושיות
- מאות
- ציד
- הוריקן
- i
- רעיון
- אידאל
- if
- מערכת חיסונית
- משופר
- in
- באחר
- עליות
- יותר ויותר
- זיהומים
- מחלות זיהומיות
- מוסיף
- בתוך
- במקום
- אל תוך
- מסקרן
- מעורב
- מְבוּדָד
- IT
- שֶׁלָה
- עצמו
- יוני
- מפתח
- כליה
- לדעת
- מעבדה
- מחסל
- אחרון
- שנה שעברה
- מאוחר יותר
- מוביל
- למד
- עזבו
- פחות
- החיים
- כמו
- צמוד
- כבד
- חי
- מקומי
- ארוך
- עוד
- ראשי
- עושה
- עשייה
- מאי..
- משמעות
- רפואי
- טעות
- מודלים
- חודשים
- יותר
- רוב
- המהלך
- mr
- mRNA
- מספר
- טרשת נפוצה
- טבעי
- טבע
- נווט
- חדש
- חדשות
- הבא
- NIH
- נוֹרמָלִי
- בדרך כלל
- of
- כבוי
- לעתים קרובות
- on
- ONE
- יחידות
- רק
- עַל גַבֵּי
- מיטוב
- אפשרויות
- or
- אחר
- אחרים
- שלנו
- הַחוּצָה
- בחוץ
- יותר
- שֶׁלוֹ
- מסוים
- חלקים
- נתיב
- חולה
- חולים
- פנסילבניה
- אֲנָשִׁים
- אוּלַי
- לצמיתות
- עַמוּד
- חלוץ
- פלטפורמה
- אפלטון
- מודיעין אפלטון
- אפלטון נתונים
- פוטנציאל
- פוטנציאל
- לחץ
- קוֹדֶם
- ייצור
- פּרוֹפִיל
- בולטות
- בולט
- מבטיח
- הוכחה
- הוכחה של רעיון או תאוריה
- אבטחה
- מָגֵן
- חֶלְבּוֹן
- חלבונים
- לספק
- לאור
- לִשְׁאוֹב
- שאיבה
- רכס
- מהיר
- מהר
- להבין
- עיצוב מחדש
- לשחרר
- להשאר
- הסרת
- חוקר
- תוצאה
- תוצאות
- לִשְׁמוֹר
- לַחֲזוֹר
- מחסומים
- שורש
- רוז
- s
- אמר
- לחפש
- סֶלֶקטִיבִי
- קשה
- לִשְׁפּוֹך
- Shutterstock
- דומה
- יחיד
- קטן
- So
- עד כה
- מוצק
- כמה
- ספציפי
- במיוחד
- מְהִירוּת
- עומד
- יציב
- סופות
- כזה
- סוּפֶּר
- משטח
- סֶקֶר
- תסמינים
- מערכת
- מערכתי
- תאי T
- לְהִתְמוֹדֵד
- התמודדות
- לוקח
- נטילת
- ברזים
- יעד
- מיקוד
- מטרות
- נבחרת
- טכנולוגיה
- לספר
- זמני
- בדיקות
- זֶה
- השמיים
- שֶׁלָהֶם
- אותם
- תיאורטי
- שם.
- אלה
- הֵם
- לחשוב
- זֶה
- השבוע
- אלפים
- שְׁלוֹשָׁה
- דרך
- ל
- טון
- טרנספורמטיבית
- התמרות
- בטיפול
- טיפול
- מִשׁפָּט
- ניסויים
- מפעילה
- באמת
- מנהרה
- תור
- פנייה
- סוג
- בעיצומה
- אוניברסיטה
- בניגוד
- להשתמש
- מְשׁוּמָשׁ
- באמצעות
- בְּדֶרֶך כְּלַל
- Vast
- נגיפי
- משכורת
- מִלחָמָה
- היה
- דֶרֶך..
- we
- שבוע
- מה
- אשר
- רָחָב
- טווח רחב
- בר
- עם
- לְלֹא
- גרוע
- שנה
- עוד
- אתה
- זפירנט