生細胞の蛍光顕微鏡は、生物系のダイナミクスを研究するための不可欠なツールを提供します。 しかし、細菌の細胞分裂やミトコンドリアの分裂など、多くの生物学的プロセスは散発的に発生するため、それらを捉えるのは困難です。
高いフレーム レートでサンプルを継続的にイメージングすることで、このような分割が発生した場合に確実に記録されます。 しかし、過剰な蛍光イメージングは光退色を引き起こし、生きているサンプルを早期に破壊する可能性があります。 一方、フレーム レートが遅いと、関心のあるイベントを見逃すリスクがあります。 必要なのは、イベントがいつ発生するかを予測し、顕微鏡に高速イメージングを開始するよう指示する方法です。
スイス連邦工科大学ローザンヌ校の研究者 (EPFL) はまさにそのようなシステムを作成しました。 チームは、サンプルへのストレスを制限しながら生物学的イベントを詳細に画像化する顕微鏡制御を自動化するイベント駆動型取得 (EDA) フレームワークを開発しました。 EDA は、ニューラル ネットワークを使用して、関心のあるイベントの微妙な前兆を検出し、それに応じて、画像処理速度や測定時間などの取得パラメーターを調整します。

「インテリジェントな顕微鏡は、自動運転車のようなものです。 特定の種類の情報、微妙なパターンを処理する必要があり、その後、その動作を変更することで応答します」と主任研究員は説明します。 スリアナ・マンリー プレス声明で。 「ニューラル ネットワークを使用することで、はるかに微妙なイベントを検出し、それらを使用して取得速度を変化させることができます。」
で説明されている EDA フレームワーク ネイチャーメソッドは、ライブ画像ストリームと顕微鏡制御の間のフィードバック ループで構成されます。 研究者は、Micro-Manager ソフトウェアを使用して顕微鏡から画像をキャプチャし、ラベル付きデータでトレーニングされたニューラル ネットワークを使用してそれらを分析しました。 画像ごとに、ネットワーク出力は、低速イメージングと高速イメージングを切り替えるための意思決定パラメーターとして機能します。
イベント認識
新しい技術を実証するために、Manley と同僚は、EDA をインスタント構造化照明顕微鏡に統合し、それを使用して、ミトコンドリアと細菌の分裂の超解像タイムラプス ムービーをキャプチャしました。
ミトコンドリアの分裂は予測不可能で、通常は数分に 1 回、数十秒続きます。 分裂の開始を予測するために、研究チームはニューラル ネットワークを訓練して、自発的な分裂に必要な DRPXNUMX と呼ばれるタンパク質の存在と組み合わせて、分裂につながるミトコンドリアの形状の変化である収縮を検出しました。
ニューラル ネットワークは「イベント スコア」のヒート マップを出力し、高い値 (収縮と DRP1 レベルの両方が高い場合) は、分割が発生する可能性が高い画像内の場所を示します。 イベントスコアが閾値を超えると、分割イベントを詳細に捉えるために撮影速度が速くなります。 スコアが XNUMX 番目のしきい値まで低下すると、顕微鏡は低速イメージングに切り替わり、サンプルが過剰な光にさらされるのを防ぎます。
研究者らは、ミトコンドリアを標的とする蛍光標識を発現する細胞に対して EDA を実行しました。 各 EDA 測定中に、ネットワークは細菌分裂の前駆体を平均 0.2 回認識しました。 これにより、平均 3.8 秒間、イメージング速度が低速 (10 フレーム/秒) から高速 (18 フレーム/秒) に切り替わり、フレームの 1% で高速イメージングが行われました。 彼らは、多くのサイトが DRPXNUMX を蓄積したが、分裂には至らなかったことに注目しています。 これらのサイトはネットワークをトリガーせず、関心のあるイベントを識別する能力を示しています。
比較のために、チームは一定の低速および高速で画像も収集しました。 EDA は、固定レートの高速イメージングよりもサンプルの光退色が少なく、各サンプルのより長い観察を可能にし、まれなミトコンドリア分裂イベントを捕捉する可能性を高めます。 場合によっては、サンプルは遅いイメージング段階で光退色から回復し、より高い累積光量を可能にしました。
一定の遅いイメージングよりもEDAの方が漂白が高かったが、多くのEDAセッションはサンプルの健康状態を損なうことなく10分に達した。 研究者はまた、高速画像のバーストによってキャプチャされたように、EDA が分裂に先立つ狭窄、および分裂につながる膜状態の進行をよりよく解決することも発見しました。
「インテリジェントな顕微鏡検査の可能性には、標準的な取得では見逃されるものを測定することが含まれます」とマンリーは説明します。 「より多くのイベントをキャプチャし、小さなくびれを測定し、各分割をより詳細に追跡できます。」
細菌分裂の検出
次に、研究者は EDA を使用して細菌の細胞分裂を研究しました。 C. クレセントス。 細菌の細胞周期は数十分のタイムスケールで発生し、生細胞顕微鏡法に明確な課題をもたらします。 彼らは、6.7 フレーム/時間の低速イメージング速度、20 フレーム/時間の高速イメージング速度、または EDA によって切り替えられる可変速度でデータを収集しました。
チームは、ミトコンドリア収縮のために開発されたイベント検出ネットワークが、追加のトレーニングなしで細菌分裂の最終段階を認識できることを発見しました。これはおそらく、収縮形状の類似性と機能的に類似した分子マーカーの存在によるものです。
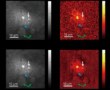
改良された顕微鏡技術により、生きた細胞を XNUMX 倍の感度で見ることができます
繰り返しになりますが、EDA はコンスタント ファスト イメージングと比較して光退色を低減し、コンスタント スロー イメージングよりも平均直径が大幅に小さい収縮を測定しました。 EDA により、細胞周期全体のイメージングが可能になり、固定のイメージング速度では捉えにくい細菌細胞分裂の詳細が得られました。.
マンリーは言う 物理学の世界 チームはまた、ニューラル ネットワークをトレーニングしてさまざまな種類のイベントを検出し、これらを使用してさまざまなハードウェア応答を呼び出すことも計画しています。 「たとえば、光遺伝学的摂動を利用して、細胞分化の重要な瞬間に転写を調節することを想定しています」と彼女は説明します。 「また、イベント検出をデータ圧縮の手段として使用し、特定の研究に最も関連のあるデータを保存または分析するために選択することも考えています。」
- 研究者がさまざまな顕微鏡に EDA を実装できるようにするために、チームは制御フレームワークを オープンソースのプラグイン Micro-Manager ソフトウェア用。