粒子線治療 - 陽子または重イオンのビームを使用するがん治療 - は、従来の光子ベースの放射線治療よりも高度に適合した線量送達と正常組織へのより大きな温存を提供します。 しかし、がんの長期生存者にとって、放射線誘発性二次がん (SC) のリスクは重要であり、治療法を選択する際に考慮する必要があります。
陽子線治療や炭素線治療などの新しい治療法の疫学的データが不足しているため、チームは 重イオン研究所のGSIヘルムホルツセンター 粒子線治療法間の SC リスクを比較するモデルを開発中です。 によって記述されたモデル アントニア・フフナグル と同僚 医学物理学、追加の最適化基準としてSCリスクを含めるために、最終的に治療計画システムに組み込むことができます。
致死的イベントと発がん性イベント
SC リスク モデルは通常、細胞死 (がんの抑制につながる) と細胞の形質転換 (最終的にがんにつながる突然変異の誘導) のバランスを考慮することによって機能します。 照射された体積が癌を発症する確率は、細胞の生存と送達された光子線量との間の単純な関係を提供する線形二次 (LQ) モデルを使用して定義されます。
この研究では、研究者は局所効果モデル (LEM) を使用して、粒子療法後の SC 誘導の相対的生物学的有効性 (RBE) を予測しました。 粒子放射の増加した RBE を説明するために、彼らはリスクモデルの光子 LQ パラメータを LEM によって予測されたイオンビーム LQ パラメータに置き換えました。 彼らのアプローチの重要な特徴は、細胞殺傷と癌誘導の両方の用語で LEM を使用することです。

「LEM を二重に使用することは、SC の発生を決定する XNUMX つの主要なプロセス、つまり細胞の形質転換と細胞の死滅の競合を反映しています」と上級著者は説明します。 マイケル・ショルツ. 「用量および/または効果の増加に伴い、細胞死は形質転換細胞の生存率を抑制する可能性があります。 これは複雑な相互作用につながり、他の方法ではワンステップの手順に単純に反映することはできません。」
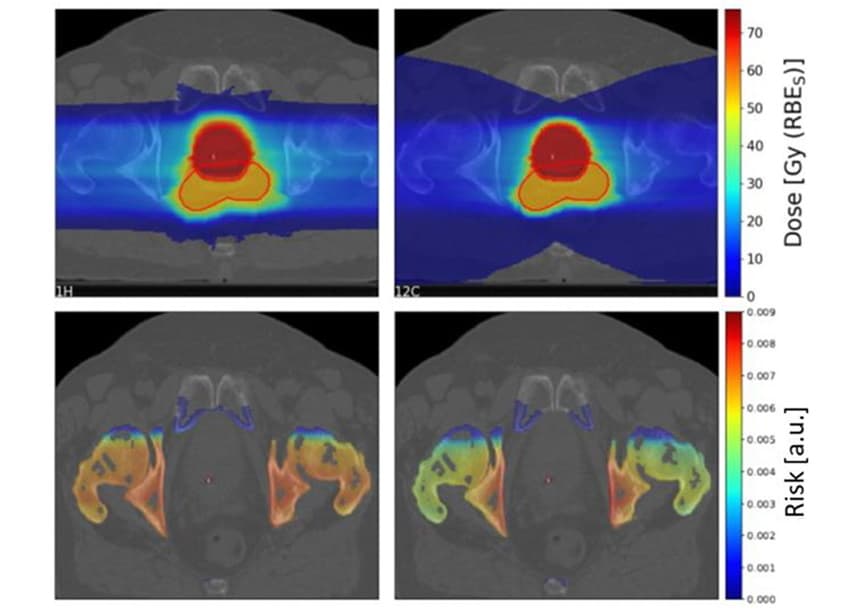
どの要因が SC リスクに影響を与えるかを調査するために、研究者は TPS TRiP98 計画システムを使用して、理想化されたジオメトリに基づいて生物学的に最適化された炭素イオンおよび陽子治療計画を作成しました。 計画では、ターゲットの前に 4x4x4 cm の危険臓器 (OAR) を配置して、4 つの粒子ビームまたは 4 つの対向するビームで 1xXNUMXxXNUMX cm のターゲットを照射しました。 LEM の入力として使用される光子 LQ パラメーターの不確実性のため、個々のリスク値ではなく、プロトン対炭素イオンのリスク比を推定しました。
これらの理想化された設定では、モデルは陽子イオンまたは炭素イオンのどちらに対しても明確な優先順位を示しませんでしたが、さまざまなパラメーターへの複雑な依存性を明らかにしました。 炭素イオンの横方向の散乱が減少すると、入口チャネルの陽子よりも SC リスクが低くなります。 ただし、炭素イオンは、フラグメンテーション テールのためにターゲットの背後に高線量を沈着させ、炭素イオン照射後に腫瘍の背後にある OAR の SC リスクを増加させます。
シングルビーム計画の場合、全 SC リスクは陽子よりも炭素イオンの方が約 1.5 倍高かった。 1.16 つの対向するビームでは、合計 SC リスクは陽子の XNUMX 倍高かったが、これはターゲット ボリュームに対する想定される高感度ボリュームの空間的位置に応じて大きく変化した。
組織の放射線感受性 (光子に対する) は、SC リスク比に大きな影響を与え、放射線耐性 OAR は炭素イオン処理の恩恵を受け、敏感な OAR は陽子ビームから恩恵を受けました。 対照的に、分割スキームは、期待されるリスク値にほとんど影響を与えませんでした。
患者の形状
臨床シナリオを調査するために、ショルツと同僚は、カロリンスカ大学病院で以前に光子放射線療法で治療された 10 人の前立腺癌患者の SC リスクを推定しました。 彼らは、横方向に対向する XNUMX つのスキャンされた陽子および炭素イオン フィールドを使用して、患者の治療計画を作成しました。
前に見たように、炭素イオンのフラグメンテーション テールにより、ターゲットの背後に大きな低線量領域が生じました。 ただし、高線量のターゲット領域は、陽子計画よりも炭素イオンに対してより等角的でした。
チームは、10 人の患者の 1.19 つの OAR (膀胱、直腸、骨、および皮膚) のプロトン対炭素イオン SC リスク比を計算しました。 骨と皮膚の場合、陽子線計画は炭素イオン計画よりもわずかに高い SC リスクをもたらし、骨と皮膚のリスク比の中央値はそれぞれ 1.06 と 0.68 でした。 しかし、膀胱と直腸の場合、プロトン計画はSCリスクを大幅に低下させ、膀胱と直腸のリスク比はそれぞれ0.49とXNUMXでした。
研究者は、このモデルによって得られた洞察が将来の治療を最適化するのに役立つ可能性があると結論付けています。 現在、相対リスク モデリングは主に、さまざまな患者コホートのさまざまな治療シナリオを比較するためのツールとして適しています。 しかし Scholz 氏は、そのようなモデルを個々の患者の治療計画に組み込むのは簡単だと指摘しています。

炭素イオン グリッド療法は健康な組織を救う
「必要なのは、それぞれ細胞死滅と細胞形質転換プロセスを表す 3 つの異なる生物学的パラメーター セットを使用して、特定の線量分布の計画を実行することだけです」と彼は説明します。 「その後、対応するリスク比分布を導出するために、標準的な数学ツールを使用して、結果の XNUMXD 効果分布を後処理するだけで済みます。」
次のステップは、臨床データと比較してモデルを検証することだと彼は言います。 「現時点ではこれらのデータが不足しているため、光子治療も含むようにアプローチを拡張し、陽子対光子および炭素イオン対光子の対応するリスク比を決定することが、重要な次のステップになるでしょう」と Scholz 氏は語っています。 物理学の世界.