脳機能の進行性喪失を特徴とする神経変性疾患は、主に中枢神経系におけるシナプス喪失と神経細胞死によって引き起こされます。 アルツハイマー 疾患(AD)はおそらく、認知症を引き起こす最も一般的な神経変性疾患です。
治療法の欠点は、科学者がアルツハイマー病がどのように発症するかを完全に理解していないことを反映しています。科学者たちはまた、なぜ女性が症例の3分の2近くを占めるのかも分かっていない。
研究者は マサチューセッツ工科大学(MIT) および スクリップスリサーチ アルツハイマー病の分子病因論へのヒントを発見した。この手がかりは、女性が病気にかかりやすい理由も説明できるかもしれません。
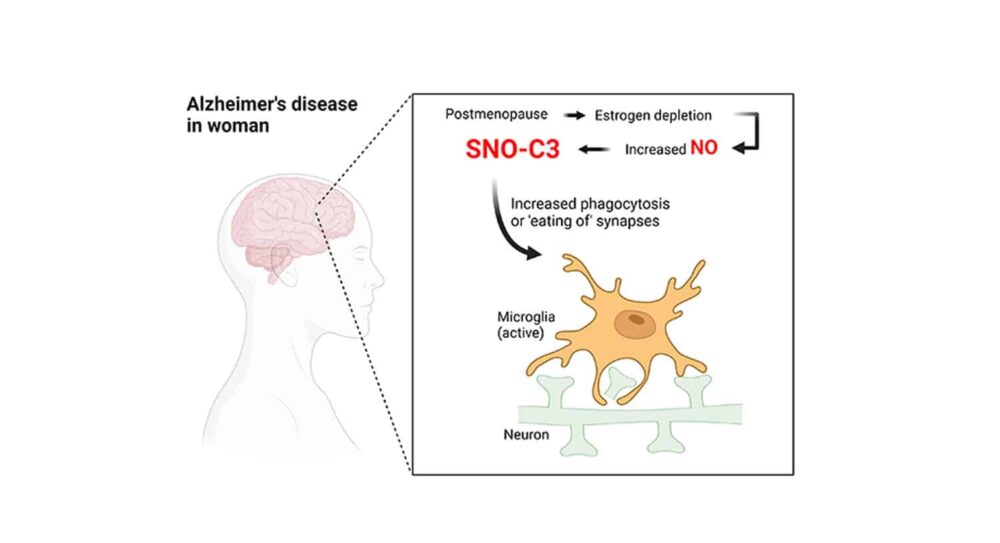
研究者らは、補体C3と呼ばれる特に有害で化学的に修飾された炎症性免疫タンパク質が、この病気で死亡した男性と比較して、この病気で死亡した女性の脳内にはるかに高いレベルで存在していることを発見した。彼らはまた、それを示しました エストロゲン—その間に生産が低下します 更年期障害- 通常、この形態の補体 C3 の生成を防ぎます。
研究の主著者であるスチュアート・リプトン医学博士、スクリップス・リサーチ分子医学科教授、ステップ・ファミリー財団寄附理事長であり、カリフォルニア州ラホーヤの臨床神経内科医は次のように述べた。 「私たちの新たな発見は、補体系の構成要素の化学修飾がアルツハイマー病の発症に寄与していることを示唆しており、この病気が主に女性に影響を与える理由を少なくとも部分的に説明できる可能性があります。」
リプトンの研究室では、プロテイン S ニトロシル化などの生化学的および分子的プロセスを研究しています。これにより、補体 C3 の修飾バージョンが生成され、これが原因となる可能性があります。 神経変性疾患。一酸化窒素 (NO) 関連分子がタンパク質の特定のアミノ酸構成要素上の硫黄原子 (S) にしっかりと結合すると、修飾された「SNO タンパク質」が生成されるこの化学プロセスは、リプトンと彼の同僚によって最初に発見されました。 。
NO のような小さな原子クラスターは頻繁に修飾されます。 細胞内のタンパク質。これらの変化は通常、標的タンパク質の機能を活性化または不活性化します。技術的な困難のため、S-ニトロシル化は他のタンパク質修飾ほど注目されていません。それでもリプトン氏は、これらのタンパク質の「SNOストーム」がアルツハイマー病やその他の神経変性疾患の発症に重要な役割を果たしている可能性があると仮説を立てている。
リプトンの研究室では、プロテイン S ニトロシル化などの生化学的および分子的プロセスを研究しています。これにより、神経変性疾患の原因となる可能性のある補体 C3 の修飾バージョンが生成されます。一酸化窒素 (NO) 関連分子がタンパク質の特定のアミノ酸構成要素上の硫黄原子 (S) にしっかりと結合すると、修飾された「SNO タンパク質」が生成されるこの化学プロセスは、リプトンと彼の同僚によって最初に発見されました。 。
NO のような小さな原子クラスターは、細胞内のタンパク質を頻繁に修飾します。これらの変化は通常、標的タンパク質の機能を活性化または不活性化します。技術的な困難のため、S-ニトロシル化は他のタンパク質修飾ほど注目されていません。それでもリプトン氏は、これらのタンパク質の「SNOストーム」がアルツハイマー病やその他の神経変性疾患の発症に重要な役割を果たしている可能性があると仮説を立てている。
最新の研究では、科学者らは、S-ニトロシル化を特定するための最新の技術を使用して、40人の死後の人間の脳で変化したタンパク質の量を測定しました。脳は男性と女性に均等に分割され、半分はアルツハイマー病で死亡した人のもので、残りの半分はアルツハイマー病ではなかった人のものでした。
研究者らは、これらの脳内で S-ニトロシル化された 1,449 個の異なるタンパク質を発見しました。補体C3など、すでにアルツハイマー病と関連している多くのタンパク質が最も頻繁に変化したタンパク質の中に含まれていた。驚くべきことに、女性のアルツハイマー病の脳には、男性のアルツハイマー病の脳よりも3倍以上高いS-ニトロシル化C3(SNO-CXNUMX)レベルがあった。
補体系は進化的に古い人類の一部です 免疫システム。これは、C3 を含むタンパク質ファミリーで構成されており、相互に活性化して「補体カスケード」で炎症を引き起こすことができます。
研究者らは30年以上前から、神経学的に健康な脳と比較して、アルツハイマー病の脳は補体タンパク質やその他の炎症指標の量が多いことを知っていた。より最近の研究では、特に、補体タンパク質がミクログリアとして知られる脳常在免疫細胞にどのようにシナプスを分解させるのかが実証されています。これらの交差点では、 ニューロンは互いに通信します.
現在、多くの研究者は、このシナプス破壊メカニズムがアルツハイマー病の根底にあるのではないかと疑っている。シナプスの喪失は、アルツハイマー病の脳における認知機能の低下と有意な相関関係があることが実証されています。
なぜアルツハイマー病の女性の脳ではSNO-C3の有病率が高いのでしょうか?研究者らは、エストロゲンが女性の脳をC3 S-ニトロシル化から保護しており、閉経に伴ってエストロゲンレベルが急激に低下すると、この保護が失われるという仮説を提案した。女性ホルモンのエストロゲンには、状況によっては脳を保護する効果があるという証拠が長年にわたって存在しています。この理論は培養された人間を使った実験によって検証されました 脳細胞この研究は、脳細胞内で NO を生成する酵素の活性化によりエストロゲン (-エストラジオール) レベルが低下すると、SNO-C3 が増加することを示しました。 SNO-C3レベルが上昇すると、シナプスはミクログリアによって破壊されます。
リプトン 言う, 「なぜ女性がアルツハイマー病になりやすいのかは長い間謎でしたが、今回の研究結果は、女性が年齢を重ねるにつれて脆弱になることをメカニズム的に説明するパズルの重要なピースを示していると思います。」
ジャーナルリファレンス:
- ヤン・ホンメイ、オ・チャンギ 他C3の異常なプロテインS-ニトロシル化に基づく、アルツハイマー病における女性優位性の機構的洞察。 科学の進歩。 DOI: 10.1126/sciadv.ade0764