생물학적 환경에서 화학 반응을 원격으로 제어하면 다양한 범위의 의료 응용이 가능해집니다. 예를 들어, 신체의 표적에 화학요법 약물을 방출하는 능력은 이러한 독성 화합물과 관련된 해로운 부작용을 우회하는 데 도움이 될 수 있습니다. 이러한 목표를 위해 캘리포니아 공과대학(California Institute of Technology)의 연구원들은대학원생)은 초음파를 사용하여 진단 또는 치료 화합물을 필요할 때 정확하게 필요한 곳에 방출하는 완전히 새로운 약물 전달 시스템을 만들었습니다.
연구소에서 개발된 플랫폼 맥스웰 롭 및 미하일 샤피로는 물리적인 힘을 가할 때 화학적 변화를 겪고 더 작은 화물 분자를 방출하는 기계포(mechanophore)로 알려진 힘에 민감한 분자를 기반으로 합니다. 기계적 자극은 생물학적 조직 깊숙이 침투하여 밀리미터 미만의 정밀도로 적용될 수 있는 집중 초음파(FUS)를 통해 제공될 수 있습니다. 그러나 이 방법에 대한 이전 연구에서는 가열을 유발하고 근처 조직을 손상시킬 수 있는 높은 음향 강도가 필요했습니다.
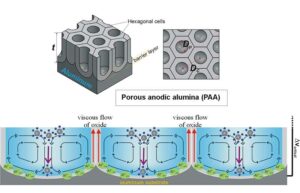
더 낮고 더 안전한 초음파 강도를 사용하기 위해 연구진은 초음파 조영제로 사용할 수 있는 공기로 채워진 단백질 나노구조인 기포(GV)로 전환했습니다. 그들은 GV가 초음파 에너지를 집중시키는 음향-기계 변환기로 기능할 수 있다는 가설을 세웠습니다. FUS에 노출되면 GV가 캐비테이션을 겪고 그 결과 에너지가 기계단을 활성화합니다.
공동 제XNUMX저자는 “초음파를 통해 힘을 가하는 것은 일반적으로 작은 용해된 기포의 파열을 촉발하는 매우 강렬한 조건에 의존합니다”라고 설명합니다. 몰리 맥파든 언론 성명에서. “그들의 붕괴는 메카노포어를 활성화하는 기계적 힘의 원천입니다. 소포는 초음파에 대한 민감도가 높아졌습니다. 이를 사용하여 우리는 훨씬 약한 초음파에서도 동일한 기계적 활성화가 달성될 수 있음을 발견했습니다."
결과를 보고합니다. 과학 국립 아카데미의 절차, 연구자들은 이 접근법이 생체적합성 FUS를 사용하여 기계적 기능화된 폴리머로부터 화물 분자의 방출을 원격으로 촉발할 수 있음을 보여줍니다.
약물 전달 개발
McFadden과 동료들은 처음으로 생리학적 응용을 위한 안전한 초음파 매개변수를 식별했습니다. 330kHz FUS를 사용한 실험에서는 1.47% 듀티 사이클(펄스당 4.5사이클)에서 생체 적합성 상한인 3000MPa 피크 음압이 밝혀져 음향 강도가 3.6W/cmXNUMX가 되었습니다.2. 조직 모방 젤 팬텀에서 이러한 매개변수는 최대 온도 증가를 3.6°C로 가져왔습니다.
그런 다음 연구원들은 FUS가 이러한 생체 적합성 매개 변수를 사용하여 기계 운반체 함유 폴리머를 활성화할 수 있는지 조사했습니다. 그들은 형광성 소분자가 탑재된 사슬 중심 기계단을 포함하는 고분자 PMSEA를 연구했습니다. GV가 있는 상태에서 이 폴리머의 희석 용액을 생체 적합성 FUS에 노출하면 형광이 크게 증가하여 페이로드가 성공적으로 방출되었음을 나타냅니다. FUS 노출 15분 후 약 10%가 방출되었습니다. 중요한 것은 GV가 없는 FUS 노출은 형광성 반응을 유발하지 않았으며 GV가 음향 기계적 변환기로서 필수적인 역할을 한다는 것을 확인했습니다.
다음으로 연구진은 시스템이 기계적으로 유발되는 약물 방출에 적합한지 여부를 조사했습니다. 그들은 화학요법제인 캄프토테신을 기계단에 결합시킨 후 중합하여 PMSEA-CPT를 생성하고 FUS를 사용하여 제어 방출을 제공했습니다. 생체적합성 FUS + GV에 10분 동안 노출된 후 약 8%의 캄프토테신이 방출되었습니다. 형광생성 분자에서 발견된 바와 같이, GV가 없는 경우에는 약물 방출이 검출되지 않았습니다.
공동 제XNUMX저자에 따르면 야오 유싱, FUS가 생물학적 환경에서 특정 화학 반응을 제어하는 것으로 입증된 것은 이번이 처음입니다. Yao는 "이전에는 초음파를 사용하여 사물을 파괴하거나 이동시켰습니다."라고 말했습니다. "그러나 이제 기계화학을 사용하여 우리에게 새로운 길을 열어주고 있습니다."
환자의 표적 화학요법에 대한 플랫폼의 미래 잠재력을 평가하기 위해 연구진은 플랫폼의 세포독성을 조사했습니다. 체외에서 림프모세포와 유사한 Raji 세포에 대해. 이전에 FUS 및 GV에 노출된 PMSEA-CPT와 함께 XNUMX일 동안 배양한 세포는 생존력이 크게 감소한 것으로 나타났습니다. 대조적으로, FUS에 노출되지 않은 PMSEA-CPT 또는 FUS에 노출되었지만 GV 없이 PMSEA-CPT와 함께 배양된 세포에서는 유의미한 세포독성이 관찰되지 않았습니다.

프로그래밍 가능한 약물 전달을 제공하는 광 트리거 이식형 장치
연구진은 “수성 매질에서 고분자로부터 분자 페이로드가 기계적으로 촉발되어 방출되는 것은 비침습적 생체 영상화 및 고분자 기계화학의 치료 적용을 위한 이러한 접근법의 힘을 보여줍니다.”라고 썼습니다. "보다 광범위하게, 이 연구는 FUS가 제공하는 시공간적 정확성과 조직 침투를 통해 생물의학 관련 조건에서 특정 화학 반응의 원격 제어를 달성하기 위한 접근 방식을 보여줍니다."
통제된 실험실 조건에서 이러한 초기 테스트를 마친 후, 연구원들은 이제 살아있는 유기체에서 플랫폼을 테스트할 계획입니다. “우리는 이 근본적인 발견을 다음으로 번역하기 위해 노력하고 있습니다. 생체내에서 약물 전달 및 기타 생물의학 기술을 위한 응용 프로그램입니다."라고 Robb은 말합니다. 물리 세계.
- SEO 기반 콘텐츠 및 PR 배포. 오늘 증폭하십시오.
- PlatoData.Network 수직 생성 Ai. 자신에게 권한을 부여하십시오. 여기에서 액세스하십시오.
- PlatoAiStream. 웹3 인텔리전스. 지식 증폭. 여기에서 액세스하십시오.
- 플라톤ESG. 탄소, 클린테크, 에너지, 환경, 태양광, 폐기물 관리. 여기에서 액세스하십시오.
- PlatoHealth. 생명 공학 및 임상 시험 인텔리전스. 여기에서 액세스하십시오.
- 출처: https://physicsworld.com/a/biocompatible-focused-ultrasound-delivers-cancer-drugs-on-target/
- :있다
- :이다
- :아니
- :어디
- 1
- 10
- 15%
- 3000
- a
- 능력
- Academy
- 달성
- 달성
- 활성화
- 활성화
- 제공
- 후
- 에이전트
- 자치령 대표
- 겨냥
- an
- 및
- 어플리케이션
- 적용된
- 접근
- 대략
- 있군요
- 약
- AS
- 평가하다
- 관련
- At
- 저자
- 기반으로
- BE
- 된
- 생물 의학
- 몸
- 경계
- 대체로
- 비자 면제 프로그램에 해당하는 국가의 시민권을 가지고 있지만
- by
- 캘리포니아
- CAN
- 게자리
- 원인
- 셀
- 변경
- 화학
- 축소
- 동료
- 조건
- 이 포함되어 있습니다
- 대조
- 제어
- 통제
- 수
- 만들
- 만든
- 주기
- 주기
- 손상
- 일
- 감소
- 깊은
- 제공
- 배달
- 보여
- 시연
- 보여줍니다
- 탐지 된
- 개발
- 장치
- 진단
- DID
- 발견
- 혼란
- 몇몇의
- 마약
- 약물
- 이전
- 효과
- 가능
- 에너지
- 전적으로
- 환경
- 필수
- 예
- 실험
- 설명
- 드러난
- 노출 시간
- 결과
- 먼저,
- 처음으로
- 초점
- 집중
- 다음에
- 럭셔리
- 힘
- 발견
- 에
- 기능
- 기본적인
- 미래
- 가스
- 했다
- 있다
- 고조 된
- 도움
- 높은
- 그러나
- HTTPS
- 확인
- 설명하다
- 영상
- 내파
- 중요하게
- in
- 증가
- 배양
- 정보
- 처음에는
- 학회
- 으로
- 발행물
- 그
- JPG
- 알려진
- 실험실
- 실험실
- 지도
- 왼쪽 (left)
- 제한
- 링크드인
- 생활
- 절감
- 최대 폭
- 최고
- 기계적인
- 미디어
- 의료
- 의료 응용
- 방법
- 분
- 분자의
- 분자
- 움직임
- 많은
- 국가의
- 필요
- 부정
- 신제품
- 아니
- 지금
- of
- on
- 만
- 열기
- or
- 기타
- 매개 변수
- 통로
- 환자
- 피크 (캐노피 지붕쪽)
- 침투
- 용
- 환상
- 물리적
- 물리학
- 물리 세계
- 계획
- 플랫폼
- 플랫폼
- 플라톤
- 플라톤 데이터 인텔리전스
- 플라토데이터
- 연극
- ...을 더한
- 폴리머
- 가능성
- 힘
- 정밀하게
- Precision
- 존재
- 키를 눌러
- 압박
- 이전에
- 프로그램
- 단백질
- 제공
- 제공
- 제공
- 펄스
- 범위
- 반응
- 반응
- 공개
- 출시
- 관련된
- 먼
- 필수
- 연구원
- 응답
- 결과
- 공개
- 연락해주세요
- 직위별
- 가장 안전한 따뜻함
- 안전
- 같은
- 라고
- 본
- 감도
- 설정
- 측면
- 상당한
- 작은
- 작은
- 해결책
- 출처
- 구체적인
- 성명서
- 자극
- 강한
- 연구
- 연구
- 교육과정
- 성공한
- 적당한
- 체계
- 목표
- 대상
- 기술
- Technology
- 말하다
- test
- 테스트
- 그
- XNUMXD덴탈의
- 소스
- 그들의
- 그들
- 그때
- Bowman의
- 그들
- 일
- 이
- 을 통하여
- 미리보기
- 시간
- 에
- 번역
- 트리거
- 방아쇠를 당긴
- 참된
- 돌린
- 두
- 아래에
- 받다
- us
- 사용
- 익숙한
- 사용
- 사용
- 보통
- 대단히
- 를 통해
- 생존 능력
- 였다
- we
- 언제
- 여부
- 어느
- 과
- 이내
- 없이
- 일하는
- 세계
- 쓰다
- 제퍼 넷