전자 장치와 광학 센서를 단일 세포 수준에서 인체와 통합하는 능력을 통해 언젠가 개별 세포를 실시간으로 원격 모니터링하고 제어할 수 있게 될 것입니다. 전자 제조 기술의 발전으로 나노 규모 해상도의 트랜지스터와 센서를 만드는 것이 가능해졌으며, 혁신적인 나노패터닝 기술을 통해 이러한 장치를 유연한 기판에 조립할 수 있습니다. 그러나 이러한 공정에는 일반적으로 살아있는 세포와 조직에 적합하지 않은 가혹한 화학 물질, 고온 또는 진공 기술이 필요합니다.
이러한 장애물을 극복하기 위해 Johns Hopkins University의 연구팀은 살아있는 조직과 세포에 금 나노 패턴을 인쇄하는 무독성, 고해상도, 비용 효율적인 프로세스를 개발했습니다. 결과 보고 나노 편지, 그들은 새로운 기술이 금 나노점과 나노와이어의 유연한 배열로 살아있는 세포와 조직에 "문신"을 할 수 있음을 보여줍니다. 궁극적으로 이 방법은 생체 공학 및 바이오 센싱과 같은 응용 분야를 위해 스마트 장치를 생체 조직과 통합하는 데 사용될 수 있습니다.
"분리된 세포의 건강을 추적하는 기술이 있다면 질병을 훨씬 더 일찍 진단하고 치료할 수 있으며 전체 장기가 손상될 때까지 기다리지 않을 수 있습니다."라고 팀 리더는 설명합니다. 데이비드 그라시아스 언론 성명에서. “우리는 핀 머리보다 수십 배 작은 생명체에 전자 문신 같은 것을 붙이는 것에 대해 이야기하고 있습니다. 이는 살아있는 세포에 센서와 전자 장치를 부착하는 첫 번째 단계입니다.”
감사합니다, 구 루오 연구진은 금 나노패턴을 살아있는 세포에 결합시키는 XNUMX단계 나노전사 인쇄 공정을 설계했습니다. 첫 번째 단계에서 그들은 기존의 나노임프린트 리소그래피(NIL)를 사용하여 금 나노점 또는 나노와이어 배열을 폴리머 코팅 실리콘 웨이퍼에 인쇄했습니다. 그런 다음 그들은 폴리머를 용해시켜 유리 커버슬립으로 옮길 수 있는 나노어레이를 확보했습니다.
다음으로, 연구진은 시스테아민으로 금 표면을 기능화하고 금 NIL 배열을 알지네이트 하이드로겔 전달 층으로 코팅했습니다. 그들은 이 접근법이 유리에서 부드럽고 유연한 하이드로겔로 8×8mm 나노점과 나노와이어 배열을 안정적으로 전달할 수 있음을 보여주었습니다. 마지막 단계에서 금 NIL 배열은 젤라틴과 결합되어 살아있는 세포나 조직으로 전달됩니다. 하이드로겔 전사층을 분리하면 금 패턴이 노출됩니다.
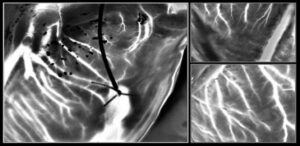
연구진은 알기네이트 하이드로겔에 직경 250nm의 금점(중심간 간격 550nm) 또는 폭 300nm의 금선(450nm 간격) 배열에 파종된 살아있는 섬유아세포의 행동을 조사했습니다. 파종 후 약 24시간 후에 나노와이어가 인쇄된 하이드로겔의 세포는 나노와이어와 평행하게 이동하는 것이 바람직했지만, 나노점의 세포는 무작위이지만 약간 더 빠른 이동을 보였습니다. 나노와이어의 세포는 또한 나노점의 세포보다 대략 두 배의 신장을 나타냈습니다. 이러한 발견은 금 NIL 어레이가 세포 방향 및 이동을 안내하는 능력을 보여줍니다.
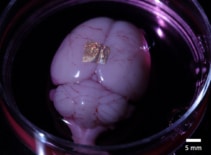
알지네이트 하이드로겔은 세포 및 조직과 생체적합성이 있을 뿐만 아니라 금 NIL 배열을 살아있는 기관 및 세포로 전달할 수도 있습니다. 이를 입증하기 위해 연구진은 전체 뇌의 대뇌 피질과 관상 뇌 절편에 나노와이어 인쇄 하이드로겔을 배치했습니다.
배양 배지에서 2시간 동안 하이드로겔을 분리한 후, 나노와이어는 전체 뇌 표면에 결합된 상태로 유지되었습니다. 대조적으로, 뇌 슬라이스의 나노와이어는 부착되지 않았으며, 이는 부착 강도가 세포 유형 및 배양 방법에 따라 다르다는 것을 시사합니다. 연구진은 견고한 장기 결합을 위한 접착 메커니즘을 특성화하고 최적화하기 위해서는 추가 연구가 필요하다고 지적합니다.
마지막으로, 단일 세포 수준에서 생체전이 인쇄를 평가하기 위해 연구진은 금 NIL 배열로 인쇄된 알기네이트 하이드로겔에서 단층 세포 시트를 배양했습니다. 24시간 후, 그들은 섬유아세포가 심어진 하이드로겔을 젤라틴 코팅된 커버슬립 위에 뒤집고 세포가 밤새 커버슬립에 부착되도록 했습니다.
알기네이트 하이드로겔을 분리한 후 형광 현미경 검사를 통해 금 나노점으로 패턴화된 섬유아세포의 생존율은 약 97%인 반면, 나노와이어로 패턴화된 섬유아세포의 생존율은 약 98%로 나타났습니다. 이는 인쇄 과정이 살아있는 세포와 생체적합성이 있음을 나타냅니다. 패턴화된 섬유아세포 세포 시트에 보이는 반사 색상은 금 NIL 배열의 모양이 유지되었음을 나타냅니다.
제조 공정은 또한 연구자들이 금 NIL 어레이의 200μm 너비의 육각형 및 삼각형 패치를 만들 수 있는 마이크로 스케일 포토리소그래피와 호환됩니다. 그런 다음 그들은 이를 세포 시트에 생체전이하여 인쇄하여 마이크로패치에서 섬유아세포의 선택적인 성장을 유도했습니다. 16시간 이상 녹화된 영상에서는 상단에 인쇄된 나노와이어 패치가 있는 세포가 건강해 보이고 이동이 가능하며 배열이 이동하는 동안에도 연질 세포에 남아 있는 것으로 나타났습니다.

초소형 센서로 심장 세포의 전기적 및 기계적 활동을 동시에 측정
Gracias는 “우리는 복잡한 나노패턴을 살아있는 세포에 부착하면서 세포가 죽지 않도록 할 수 있다는 것을 보여주었습니다.”라고 말했습니다. "세포가 문신과 함께 살고 움직일 수 있다는 것은 매우 중요한 결과입니다. 왜냐하면 살아있는 세포와 엔지니어가 전자 장치를 제조하는 데 사용하는 방법 사이에는 상당한 비호환성이 있기 때문입니다."
Gracias와 동료들은 표준 미세 가공 기술과 결합된 나노패터닝 공정이 "새로운 세포 배양 기판, 바이오하이브리드 재료, 생체 공학 장치 및 바이오 센서 개발의 기회를 열어준다"고 결론지었습니다. 다음으로, 그들은 더 오랜 기간 동안 제자리에 머물 수 있는 더 복잡한 나노회로를 부착하고 다양한 유형의 세포를 실험할 계획입니다.
- SEO 기반 콘텐츠 및 PR 배포. 오늘 증폭하십시오.
- PlatoData.Network 수직 생성 Ai. 자신에게 권한을 부여하십시오. 여기에서 액세스하십시오.
- PlatoAiStream. 웹3 인텔리전스. 지식 증폭. 여기에서 액세스하십시오.
- 플라톤ESG. 자동차 / EV, 탄소, 클린테크, 에너지, 환경, 태양광, 폐기물 관리. 여기에서 액세스하십시오.
- PlatoHealth. 생명 공학 및 임상 시험 인텔리전스. 여기에서 액세스하십시오.
- 차트프라임. ChartPrime으로 트레이딩 게임을 향상시키십시오. 여기에서 액세스하십시오.
- BlockOffsets. 환경 오프셋 소유권 현대화. 여기에서 액세스하십시오.
- 출처: https://physicsworld.com/a/researchers-tattoo-gold-nanopatterns-onto-live-cells/
- :있다
- :이다
- :아니
- $UP
- 16
- 200
- 24
- 8
- a
- 능력
- 할 수 있는
- 소개
- 활동
- 가입 한
- 발전하다
- 후
- 또한
- 중
- an
- 및
- 등장
- 어플리케이션
- 접근
- 대략
- 있군요
- 약
- 배열
- AS
- 조립
- 평가하다
- At
- 붙이다
- BE
- 때문에
- 존재
- 사이에
- 몸
- 증서
- 뇌
- 비자 면제 프로그램에 해당하는 국가의 시민권을 가지고 있지만
- CAN
- 셀
- 특징
- 클릭
- 동료
- 결합 된
- 호환
- 복잡한
- 결론
- 대조
- 제어
- 전통적인
- 비용 효율적인
- 수
- 만들
- 문화
- 일
- 보여
- 설계
- 개발
- 개발
- 디바이스
- DID
- Mourir
- 다른
- 질병
- 하지 않습니다
- 이전
- 전자
- 전자
- 가능
- 사용 가능
- 엔지니어
- 보장
- 전체의
- 조차
- 설명
- 빠른
- 최후의
- 결과
- 먼저,
- 융통성있는
- 럭셔리
- 에
- 추가
- GAO
- 일반적으로
- 유리
- 덴탈
- 성장
- 안내
- 했다
- 있다
- 머리
- 건강
- 건강은 물론, 경제성까지!
- 심장
- 높은
- 높은 해상도
- 홉킨스
- 그러나
- HTTPS
- 사람의
- 영상
- 중대한
- in
- 개인
- 정보
- 혁신적인
- 통합
- 외딴
- 발행물
- IT
- 존스
- 존스 홉킨스 대학
- JPG
- 층
- 리더
- 지도
- 하자
- 레벨
- 처럼
- 살고있다
- 생활
- 장기
- 이상
- 만든
- 재료
- 최대 폭
- 아마도
- 조치들
- 기계적인
- 메커니즘
- 미디어
- 병합
- 방법
- 방법
- 현미경 사용
- 이전
- 이주한
- 이주
- 모니터링
- 배우기
- 움직임
- 움직이는
- 영화 산업
- 많은
- 필요
- 신제품
- 다음 것
- 대상
- 장애물
- of
- 자주
- on
- ONE
- ~에
- 열 수
- 기회
- 최적화
- or
- 위에
- 극복하다
- 밤새
- 평행
- 패치
- 무늬
- 미문
- 물리학
- 물리 세계
- 장소
- 계획
- 플라톤
- 플라톤 데이터 인텔리전스
- 플라토데이터
- 위치하는
- 가능한
- 키를 눌러
- 인쇄
- 인쇄
- 방법
- 프로세스
- 입고
- 닥치는대로의
- 쥐
- 현실
- 실시간
- 기록
- 남은
- 나머지
- 먼
- 통계 보고서
- 필요
- 연구
- 연구원
- 분해능
- 결과
- 공개
- 강력한
- 거칠게
- 라고
- 본
- 선택적
- 센서
- 셰이프
- 시트
- 보여
- 표시
- 상당한
- 규소
- 동시에
- 일부분
- 작은
- 스마트 한
- 부드러움
- 무언가
- 표준
- 성명서
- 유지
- 단계
- 힘
- 연구
- 이러한
- 제안
- 표면
- 말하는
- 팀
- 기법
- 기술
- 수십
- 보다
- 그
- XNUMXD덴탈의
- 그들의
- 그때
- Bowman의
- 그들
- 이
- 그
- 미리보기
- 시간
- 시대
- 에
- 상단
- 에 대한
- 선로
- 이전
- 치료
- 참된
- 시도
- 두번
- 유형
- 궁극적으로
- 대학
- 까지
- 사용
- 익숙한
- 진공
- 대단히
- 생존 능력
- 기다리다
- 였다
- we
- 잘
- 이므로
- 어느
- 동안
- 모든
- 넓은
- 과
- 세계
- 제퍼 넷